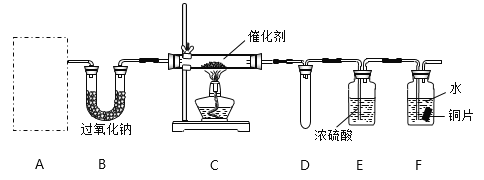
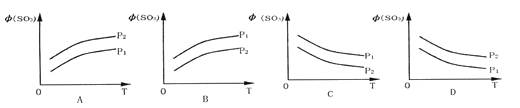
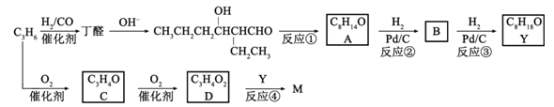
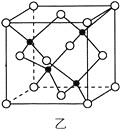
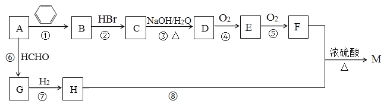
【题目】SO2的催化氧化是工业制取硫酸的关键步骤之一:2SO2 + O2![]() 2SO3 在容积均为2L,有相同催化剂的a、b、c、d、e五个密闭容器中均充入2molSO2和1molO2混合气体,控制不同的反应温度。反应进行5min时,测得相关数据如下表:
2SO3 在容积均为2L,有相同催化剂的a、b、c、d、e五个密闭容器中均充入2molSO2和1molO2混合气体,控制不同的反应温度。反应进行5min时,测得相关数据如下表:
容器温度 物质的量(mol) | a容器 400℃ | b容器 425℃ | c容器 450℃ | d容器 475℃ | e容器 500℃ |
O2 | x | 0.6 | 0.3 | 0.5 | 0.7 |
SO3 | y | 0.8 | 1.4 | 1.0 | 0.6 |
(1)5min时测得a容器中混合气体的物质的量减少了0.2mol,计算5min内SO3的平均反应速率____________。
(2)反应进行到5min时,b容器中的反应是否达到平衡状态?_______(填“是”或“否”),理由是:_____________________________________________________________________________。
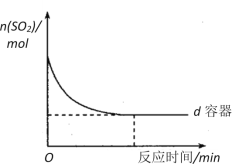
(3)在图中画出e容器中SO2物质的量随时间的变化曲线_______________________。
(4)工业上常用Na2SO3溶液来吸收SO2,该反应的离子方程式是:___________________。
(5)已知NaHSO3溶液呈酸性,溶液中c(H2SO3)_______ c(SO32—)(选填<、>或=);NaHSO3既能和强酸反应也能和强碱溶液反应。用平衡移动原理说明NaHSO3能和强碱溶液反应的原因:_______________
【题目】氨气是重要的化工原料。
(1)检验氨气极易溶于水的简单操作是:收集一试管氨气,______________。
(2)往饱和食盐水中依次通入足量的NH3和足量的CO2,生成沉淀的化学式为_________;过滤后,使余液尽可能析出较多NH4Cl晶体的方法是:再通入足量的NH3、冷却并加入________,请说明这样操作为什么可以析出较多NH4Cl的原因:_________________。某NaHCO3晶体中含有NaCl杂质,某同学在测定其中NaHCO3的含量时,称取5.000g试样,定容成100mL溶液,用标准盐酸溶液滴定(用甲基橙做指示剂),测定数据记录如下:
滴定次数 | 待测液(mL) | 0.5000mol/L盐酸溶液的体积(mL) | |
初读数 | 终读数 | ||
第一次 | 20.00 | 1.00 | 21.00 |
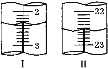
第二次 | 20.00 | 如图Ⅰ | 如图Ⅱ |
(3)定容过程中需要用到的仪器有烧杯、玻璃棒、___________和____________。
(4)当滴定至__________________________,即为滴定终点;第二次滴定,从图I图II显示消耗的盐酸溶液体积为_________mL。
(5)该实验测定样品中NaHCO3的质量分数为__________(保留2位小数)。
(6)若该同学测定结果偏大,请写出一个造成该误差的原因_____________。