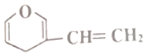��Ŀ����
����Ŀ��ʵ����������ͼ��ʾװ�����Ʊ���Ȳ������֤��Ȳ��ijЩ��ѧ���ʣ��Ʊ��� ��Ȳ�������������������� H2S ��PH3���壬�밴����Ҫ����գ�
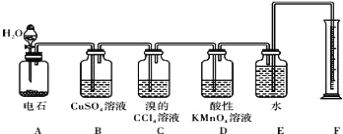
(1)ʵ��������Ȳ�Ļ�ѧ����ʽ�ǣ�_________________��Ϊ�˵õ���Ϊƽ�ȵ���Ȳ������ װ�� A �ķ�Һ©���г���______________������ˮ��
(2) װ�� D �й۲쵽�������� ___________________________________________
(3) װ�� B ��CuSO4��Һ��������_______________________________��
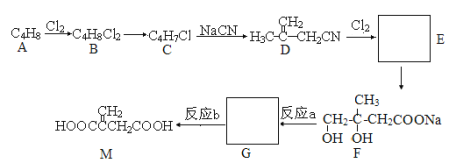
(4)д������Ȳ��HClΪԭ�ϣ��ϳɾ�����ϩ�ķ���ʽ��________________��___________________ ��
(5)����ȡm g ��ʯ����Ӧ��ȫ�����ɵ���Ȳn g����CaC2�Ĵ���Ϊ_____(��m��n��ʾ)��
���𰸡�CaC2+2H2O��CH��CH��+Ca(OH)2 ����ʳ��ˮ ��ɫ���Ϻ�ɫ��ȥ ��ȥ H2S��PH3 ���ʣ��Է����ź���ʵ�� CH��CH+HCl��CH2=CHCl ![]()
![]()
��������
ʵ�����õ�ʯ��ˮ��Ӧ�Ʊ���Ȳ�����к������ʣ�Ϊ�˾����ͼ�����Ȳ���壬�ⶨ�������������Ҫ��װ������Ϊ�������Ʊ�װ�á�����װ�ã������⣩������װ�á�����ʵ��װ�á���ˮ�������װ�ã�
��1��ʵ�����Ʊ���Ȳ�����õ�ʯ��ˮ��Ӧ������Ȳ���������ƣ�̼������ˮ��Ӧ�ܾ��ң��ñ���ʳ��ˮ���Լ�����Ӧ��
��2����Ȳͨ�����������Һ�ᱻ�������ɶ�����̼����Һ��ɫ��
��3���Ʊ�����Ȳ��������������������H2S���壬ͨ������ͭ��Һ��ȥ���⣬��ֹӰ����Ȳ�ļ��飻
��4����Ȳ���Ȼ��ⷢ���ӳɷ�Ӧ��Ȼ�����Ӿ۷�Ӧ��
��5�����ݷ���ʽ����Ȳ���������̼���Ƶ������������CaC2�Ĵ��ȡ�
��1��ʵ�����Ʊ���Ȳ�����õ�ʯ��ˮ��Ӧ������Ȳ���������ƣ���Ӧ�Ļ�ѧ����ʽΪ��CaC2+2H2O��CH��CH��+Ca(OH)2��̼������ˮ��Ӧ�ܾ��ң��ñ���ʳ��ˮ���Լ�����Ӧ������Ϊ�˵õ�ƽ�ȵ��������ñ���ʳ��ˮ����ˮ���ʴ�Ϊ��CaC2+2H2O��CH��CH��+Ca(OH)2������ʳ��ˮ��
��2����Ȳͨ�����������Һ����Ȳ���в����ͼ��������������Һ�������ɶ�����̼��װ��D�й۲쵽����������ɫ���Ϻ�ɫ��ȥ���ʴ�Ϊ����ɫ���Ϻ�ɫ��ȥ��
��3������������л�ԭ�ԣ�Ҳ�ᵼ����ˮ�����������Һ��ɫ��װ��B��CuSO4��Һ�������dz�ȥ��Ȳ�е�H2S ��PH3���壬��ֹ���ź�������ʵ�飻�ʴ�Ϊ����ȥ H2S��PH3 ���ʣ��Է����ź���ʵ�飻
��4����Ȳ���Ȼ��ⷢ���ӳɷ�Ӧ��Ȼ�����Ӿ۷�Ӧ������ʽΪ��CH��CH+HCl��CH2=CHCl��![]() ���ʴ�Ϊ��CH��CH+HCl��CH2=CHCl��
���ʴ�Ϊ��CH��CH+HCl��CH2=CHCl��![]() ��
��
��5������ȡmg��ʯ����Ӧ��ȫ�����ɵ���Ȳng����μӷ�Ӧ��̼����Ϊxg��

![]() ��n=
��n=![]() ����CaC2�Ĵ���Ϊ��
����CaC2�Ĵ���Ϊ��![]() =
=![]() ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��
��

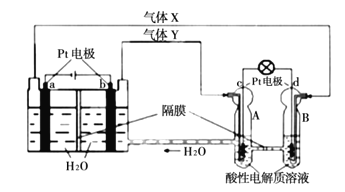
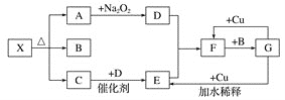
����Ŀ����I����ͼ�����ڼ��л���������Ʊ������롢���ʱȽϵȵij�������װ�á�����ݸ�װ�ûش��������⣺
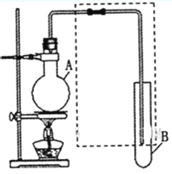
��1�������Ҵ������ᷴӦ��ȡ��������������ƿA�м�����Լ��ڻ��ʱ�IJ���������___________����Ӧ�Ļ�ѧ����ʽΪ___________���Թ�B��Ӧ����___________�����߿��еĵ��ܳ����ڵ����⣬������___________���á�
��2�����ø�װ�÷��������1-������������ƿA�г�����1�������������⣬��Ӧ�ȼ����������Լ�___________�����ȵ�һ���¶ȣ��Թ�B���ռ������ǣ���д��ѧʽ��___________����ȴ��������ƿ�м����Լ�___________�ټ��ȵ�һ���¶ȣ��Թ�B���ռ�������___________����д��ѧʽ����
��3�����ø�װ�ã����ü��ȣ�֤�����ԣ�����>̼��>���ӣ�������ƿA�м���___________���Թ�B��Ӧ����___________��
��II������ȩ��һ�ֻ���ԭ�ϡ�ijʵ��С����������װ�úϳ�����ȩ,����:CH3CH2CH2CH2OH��![]() CH3CH2CH2CHO��
CH3CH2CH2CHO��
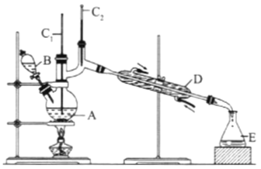
��Ӧ��Ͳ������������б�:
�е�/�� | �ܶ�/(g��cm-3) | ˮ���ܽ��� | |
������ | 11.72 | 0.8109 | �� |
����ȩ | 75.7 | 0.8017 | �� |
ʵ�鲽������:
��6.0gNa2Cr2O7����100mL�ձ���,��30mLˮ�ܽ�,�ٻ�������5mLŨ����,��������ҺС��ת����B�С���A�м���4.0g�������ͼ�����ʯ,����.������������ʱ,��ʼ�μ�B����Һ���μӹ����б��ַ�Ӧ�¶�Ϊ90-95��,��E���ռ�90�����µ���֡�������ﵹ���Һ©����,��ȥˮ��,�л�����������,�ռ�75-77�����,����2.0g��
�ش���������:
��1��ʵ����,�ܷ�Na2Cr2O7��Һ�ӵ�Ũ������,˵������:__________��
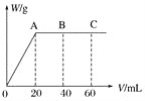
��2�������ʯ��������__________�������Ⱥ���δ�ӷ�ʯ,Ӧ��ȡ����ȷ������__________��
��3������װ��ͼ��,B������������__________,D������������__________��
��4����Һ©��ʹ��ǰ������еIJ�����(����ĸ)__________��
A.��ʪ B.���� C.��© D.�궨
��5��������ȩ�ֲ�Ʒ���ڷ�Һ©���з�Һʱ,ˮ��__________��(��������,��������)��
��6����Ӧ�¶�Ӧ������90~95��,��ԭ����__________��
��7����ʵ����,����ȩ�IJ���Ϊ__________%��.