题目内容
【题目】Na2S常用作皮革脱毛剂,工业上用反应Na2SO4 +2C ![]() Na2S+2CO2↑ 进行制取。
Na2S+2CO2↑ 进行制取。
(1)上述反应中涉及的各元素中原子半径最小的是_______(填元素符号),该原子有_____种不同能量的电子。
(2)羰基硫的化学式为COS,结构和CO2 相似,请写出COS的电子式_________,判断羰基硫分子属于________(选填“极性”或“非极性”)分子。
(3)写出一个能比较S和O非金属性强弱的化学事实_____________________ ;请从原子结构解释原因_____________________________。
(4)将Na2S溶液滴入AlCl3溶液中,产生白色沉淀,同时有臭鸡蛋气味的气体生成,用平衡移动原理解释上述现象__________________________。
【答案】O 3 ![]() 极性 水的热稳定性比硫化氢强 S 和 O为同主族元素,最外层电子数相同,原子半径越小,原子核对最外层电子的吸引力越大,使得H-O键比H-S稳定 Na2S溶液中S2-水解显碱性:S2-+H2OHS-+OH-,AlCl3溶液中Al3+水解显酸性:Al3++H2OAl(OH)3+3H+,两个水解反应相互促进,使水解进行到底,产生白色沉淀,同时有臭鸡蛋气味的气体产生
极性 水的热稳定性比硫化氢强 S 和 O为同主族元素,最外层电子数相同,原子半径越小,原子核对最外层电子的吸引力越大,使得H-O键比H-S稳定 Na2S溶液中S2-水解显碱性:S2-+H2OHS-+OH-,AlCl3溶液中Al3+水解显酸性:Al3++H2OAl(OH)3+3H+,两个水解反应相互促进,使水解进行到底,产生白色沉淀,同时有臭鸡蛋气味的气体产生
【解析】
(1)一般而言,电子层数越多半径越大,电子层数相同,核电荷数越大,半径越小,据此判断涉及的各元素中原子半径的大小;根据原子的电子排布式分析判断;
(2)根据羰基硫分子中所有原子的最外层都满足8电子结构判断其电子式;根据羰基硫的分子结构及羰基硫中碳硫双键与碳氧双键的极性进行判断;
(3)根据非金属性强弱的判断方法分析解答;
(4)根据硫离子和铝离子的水解方程式分析解答。
(1)上述反应涉及的原子有Na、S、O、C,一般而言,电子层数越多半径越大,电子层数相同,核电荷数越大,半径越小,则涉及的各元素中原子半径最小的是O,O原子有1s、2s、2p三种能量不同的电子;故答案为:O;3;
(2)羰基硫中分子中所有原子的最外层都满足8电子结构,碳原子能形成4个共价键,硫原子能形成2个共价键,氧原子能形成2个共价键,所以其电子式为![]() ;羰基硫中碳氧双键与碳硫双键的极性不同,电荷分布不均匀,所以羰基硫分子为极性分子,故答案为:
;羰基硫中碳氧双键与碳硫双键的极性不同,电荷分布不均匀,所以羰基硫分子为极性分子,故答案为:![]() ;极性;
;极性;
(3)比较 S 和 O 非金属性强弱的化学事实是,水的稳定性和硫化氢的稳定性强,S 和 O为同主族元素,最外层电子数相同,原子半径越小,原子核对最外层电子的吸引力越大,使得H-O键比H-S稳定,故答案为:水的热稳定性比硫化氢强;S 和 O为同主族元素,最外层电子数相同,原子半径越小,原子核对最外层电子的吸引力越大,使得H-O键比H-S稳定;
(4)Na2S 溶液中 S2-水解显碱性:S2-+H2OHS-+OH-,AlCl3溶液中 Al3+水解显酸性:Al3++H2OAl(OH)3+3H+,将硫化钠溶液滴入氯化铝溶液中,两个水解反应相互促进,使水解进行到底,产生白色沉淀,同时有臭鸡蛋气味的气体产生,故答案为:Na 2S溶液中S2-水解显碱性:S2-+H2OHS-+OH-,AlCl3溶液中Al3+水解显酸性:Al3++H2OAl(OH)3+3H+,两个水解反应相互促进,使水解进行到底,产生白色沉淀,同时有臭鸡蛋气味的气体产生。

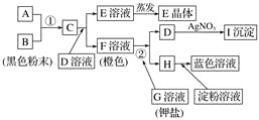
【题目】碱式氧化镍(NiOOH)可用作镍氢电池的正极材料,可用废镍催化剂(主要含Ni、Al,少量Cr、FeS 等)来制备,其工艺流程如下:

回答下列问题:
(1)“浸泡除铝”时,发生反应的离子反应方程式为_________________________;
(2)“溶解”时放出的气体为_______________ (填化学式);
(3)已知该条件下金属离子开始沉淀和完全沉淀的pH如下表:
开始沉淀的pH | 完全沉淀的pH | |
Ni2+ | 6.2 | 8.6 |
Fe2+ | 7.6 | 9.1 |
Fe3+ | 2.3 | 3.3 |
Cr3+ | 4.5 | 5.6 |
“调pH 1”时,溶液pH范围为______________________;
(4)在空气中加热Ni(OH)2可得NiOOH,请写出此反应的化学方程式_____________;

(5)金属铬在溶液中有多种存在形式, CrO42—和Cr2O72—在溶液中可相互转化。室温下,初始浓度为1.0mol/L的Na2CrO4溶液中c(Cr2O72—)随c(H+)的变化如图所示,用离子方程式表示Na2CrO4溶液中的转化反应________________,根据A点数据计算出该转化反应的平衡常数为______________,温度升高,溶液中CrO42—的平衡转化率减小,则该反应的△H____0(填“>”、“<”或“=”)。
【题目】石嘴山市打造“山水园林城市”,因此研究NOx、SO2等大气污染物的妥善处理具有重要意义。
(1)SO2的排放主要来自于煤的燃烧,工业上常用氨水吸收法处理尾气中的SO2。
已知吸收过程中相关反应的热化学方程式如下:
①SO2(g)+NH3·H2O(aq)= NH4HSO3(aq) ΔH1=a kJ/mol;
②NH3·H2O(aq)+ NH4HSO3(aq)=(NH4)2SO3(ag)+H2O(l) ΔH2=b kJ/mol;
③2(NH4)2SO3(aq)+O2(g)=2(NH4)2SO4(aq) ΔH3=c kJ/mol。
则反应2SO2(g)+4NH3·H2O(aq)+O2(g) =2(NH4)2SO4(aq)+2H2O(l)的ΔH=______kJ/mol。
(2)燃煤发电厂常利用反应2CaCO3(s)+2SO2(g)+O2(g)![]() 2CaSO4(s)+2CO2(g) ΔH =681.8 kJ/mol对煤进行脱硫处理来减少SO2的排放。对于该反应,在温度为TK时,借助传感器测得反应在不同时间点上各物质的浓度如下:
2CaSO4(s)+2CO2(g) ΔH =681.8 kJ/mol对煤进行脱硫处理来减少SO2的排放。对于该反应,在温度为TK时,借助传感器测得反应在不同时间点上各物质的浓度如下:
时间/min 浓度/mol·L1 | 0 | 10 | 20 | 30 | 40 | 50 |
O2 | 1.00 | 0.79 | 0.60 | 0.60 | 0.64 | 0.64 |
CO2 | 0 | 0.42 | 0.80 | 0.80 | 0.88 | 0.88 |
①0~10 min内,平均反应速率v(SO2)=_____mol/(L·min)。
②30min后,只改变某一条件,反应重新达到平衡。根据上表中的数据判断,改变的条件可能是_____(填字母)。
A.通入一定量的O2 B.加入一定量的粉状碳酸钙
C.适当缩小容器的体积 D.加入合适的催化剂
(3)NOx的排放主要来自于汽车尾气,有人利用反应C(s)+2NO(g)![]() N2(g)+CO2(g) ΔH=34.0 kJ/mol,用活性炭对NO进行吸附。已知在密闭容器中加入足量的C和一定量的NO气体,保持恒压测得NO的转化率随温度的变化如图所示:
N2(g)+CO2(g) ΔH=34.0 kJ/mol,用活性炭对NO进行吸附。已知在密闭容器中加入足量的C和一定量的NO气体,保持恒压测得NO的转化率随温度的变化如图所示:
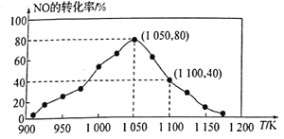
由图可知,1050K前反应中NO的转化率随温度升髙而增大,其原因为_______;在1100K时,CO2的体积分数为______。
(4)用某物质的平衡分压代替其物质的量浓度也可以表示化学平衡常数(记作Kp)。在1050K、1.1×106 Pa时,该反应的化学平衡常数Kp=____[已知:气体分压(P分)=气体总压(P)×体积分数]。
(5)汽车尾气还可利用反应2NO(g)+2CO(g)![]() N2(g)+2CO2(g) ΔH=746.8 kJ/mol,实验测得,v正=k正·c2(NO)·c2(CO),v逆=k逆·c(N2)·c2(CO2)(k正、k逆为速率常数,只与温度有关)。
N2(g)+2CO2(g) ΔH=746.8 kJ/mol,实验测得,v正=k正·c2(NO)·c2(CO),v逆=k逆·c(N2)·c2(CO2)(k正、k逆为速率常数,只与温度有关)。
①达到平衡后,仅升高温度,k正增大的倍数____(填“>”“<”或“=”)k逆增大的倍数。
②若在1L的密闭容器中充入1 molCO和1 mol NO,在一定温度下达到平衡时,CO的转化率为40%,则k正︰k逆=_____。
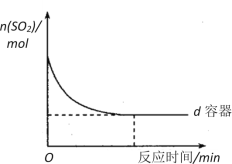
【题目】SO2的催化氧化是工业制取硫酸的关键步骤之一:2SO2 + O2![]() 2SO3 在容积均为2L,有相同催化剂的a、b、c、d、e五个密闭容器中均充入2molSO2和1molO2混合气体,控制不同的反应温度。反应进行5min时,测得相关数据如下表:
2SO3 在容积均为2L,有相同催化剂的a、b、c、d、e五个密闭容器中均充入2molSO2和1molO2混合气体,控制不同的反应温度。反应进行5min时,测得相关数据如下表:
容器温度 物质的量(mol) | a容器 400℃ | b容器 425℃ | c容器 450℃ | d容器 475℃ | e容器 500℃ |
O2 | x | 0.6 | 0.3 | 0.5 | 0.7 |
SO3 | y | 0.8 | 1.4 | 1.0 | 0.6 |
(1)5min时测得a容器中混合气体的物质的量减少了0.2mol,计算5min内SO3的平均反应速率____________。
(2)反应进行到5min时,b容器中的反应是否达到平衡状态?_______(填“是”或“否”),理由是:_____________________________________________________________________________。
(3)在图中画出e容器中SO2物质的量随时间的变化曲线_______________________。
(4)工业上常用Na2SO3溶液来吸收SO2,该反应的离子方程式是:___________________。
(5)已知NaHSO3溶液呈酸性,溶液中c(H2SO3)_______ c(SO32—)(选填<、>或=);NaHSO3既能和强酸反应也能和强碱溶液反应。用平衡移动原理说明NaHSO3能和强碱溶液反应的原因:_______________