题目内容
【题目】SO2的催化氧化是工业制取硫酸的关键步骤之一:2SO2 + O2![]() 2SO3 在容积均为2L,有相同催化剂的a、b、c、d、e五个密闭容器中均充入2molSO2和1molO2混合气体,控制不同的反应温度。反应进行5min时,测得相关数据如下表:
2SO3 在容积均为2L,有相同催化剂的a、b、c、d、e五个密闭容器中均充入2molSO2和1molO2混合气体,控制不同的反应温度。反应进行5min时,测得相关数据如下表:
容器温度 物质的量(mol) | a容器 400℃ | b容器 425℃ | c容器 450℃ | d容器 475℃ | e容器 500℃ |
O2 | x | 0.6 | 0.3 | 0.5 | 0.7 |
SO3 | y | 0.8 | 1.4 | 1.0 | 0.6 |
(1)5min时测得a容器中混合气体的物质的量减少了0.2mol,计算5min内SO3的平均反应速率____________。
(2)反应进行到5min时,b容器中的反应是否达到平衡状态?_______(填“是”或“否”),理由是:_____________________________________________________________________________。
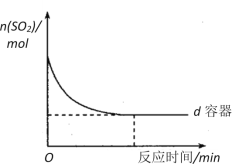
(3)在图中画出e容器中SO2物质的量随时间的变化曲线_______________________。
(4)工业上常用Na2SO3溶液来吸收SO2,该反应的离子方程式是:___________________。
(5)已知NaHSO3溶液呈酸性,溶液中c(H2SO3)_______ c(SO32—)(选填<、>或=);NaHSO3既能和强酸反应也能和强碱溶液反应。用平衡移动原理说明NaHSO3能和强碱溶液反应的原因:_______________
【答案】0.04mol/(Lmin) 否 abc中三氧化硫的物质的量是增大的,de中随温度升高三氧化硫的物质的量是减小的,温度越高,反应速率越快,建立平衡需要的时间越短,证明de是平衡状态,且温度越高,三氧化硫的物质的量越少,b容器的温度低于d,因此三氧化硫的物质的量应该大于d,因此b不是平衡状态 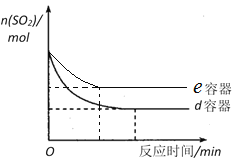 SO32-+SO2+H2O=2HSO3- < 强碱溶液中的氢氧根离子与HSO3-电离出的氢离子反应生成水,促进HSO3-的电离平衡正向移动,反应生成亚硫酸钠
SO32-+SO2+H2O=2HSO3- < 强碱溶液中的氢氧根离子与HSO3-电离出的氢离子反应生成水,促进HSO3-的电离平衡正向移动,反应生成亚硫酸钠
【解析】
(1)根据2SO2 + O2![]() 2SO3 可知,反应中气体的物质的量的减少量等于反应的氧气的物质的量,反应中气体的物质的量减少了0.2mol,即反应的氧气为0.2mol,据此计算5min内三氧化硫的反应速率;
2SO3 可知,反应中气体的物质的量的减少量等于反应的氧气的物质的量,反应中气体的物质的量减少了0.2mol,即反应的氧气为0.2mol,据此计算5min内三氧化硫的反应速率;
(2)五个容器中浓度变化可知,abc中三氧化硫浓度是增大的,de中随温度升高浓度减小,说明温度变化影响化学平衡移动,证明de是平衡状态;
(3)根据五个容器中气体的物质的量变化可知,de容器中是平衡状态,且e容器中反应温度高于d,建立平衡需要的时间少于d,平衡时,SO2物质的量大于d,据此画图;
(4)工业上常用Na2SO3溶液来吸收SO2,该反应生成亚硫酸氢钠;
(5)亚硫酸氢钠溶液中存在亚硫酸氢根离子电离和水解平衡,据此分析判断;强碱溶液中的氢氧根离子能够与HSO3-电离出的氢离子反应生成水,促进HSO3-的电离平衡正向移动,反应生成亚硫酸钠。
(1)根据2SO2 + O2![]() 2SO3 可知,反应中气体的物质的量的减少量等于反应的氧气的物质的量,反应中气体的物质的量减少了0.2mol,即反应的氧气为0.2mol,则生成的SO3 为0.4mol,5min内SO3的平均反应速率v(SO3)=
2SO3 可知,反应中气体的物质的量的减少量等于反应的氧气的物质的量,反应中气体的物质的量减少了0.2mol,即反应的氧气为0.2mol,则生成的SO3 为0.4mol,5min内SO3的平均反应速率v(SO3)=![]() =
=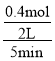 =0.04mol/(Lmin),故答案为:0.04mol/(Lmin);
=0.04mol/(Lmin),故答案为:0.04mol/(Lmin);
(2)根据五个容器中气体的物质的量变化可知,abc中三氧化硫浓度是增大的,de中随温度升高浓度减小,温度越高反应速率越快,建立平衡需要的时间越短,证明de是平衡状态,则反应进行到5min时,b容器中的反应未达到平衡状态,
故答案为:否;abc中三氧化硫的物质的量是增大的,de中随温度升高三氧化硫的物质的量是减小,温度越高反应速率越快,建立平衡需要的时间越短,证明de是平衡状态,且温度越高,三氧化硫的物质的量越少,b容器的温度低于d,因此三氧化硫的物质的量应该大于d;
(3)根据五个容器中气体的物质的量变化可知,de容器中是平衡状态,且e容器中反应温度高于d,建立平衡需要的时间少于d,平衡时,SO2物质的量大于d,变化图象为 ,故答案为:
,故答案为: ;
;
(4)工业上常用Na2SO3溶液来吸收SO2,反应生成亚硫酸氢钠,该反应的离子方程式是:SO32-+SO2+H2O=2HSO3-,故答案为:SO32-+SO2+H2O=2HSO3-;
(5)亚硫酸氢钠溶液中存在亚硫酸氢根离子电离:HSO3-SO32-+H+,电离使溶液显酸性,也存在亚硫酸氢根离子的水解:HSO3-+H2OH2SO3+OH-,水解使溶液显碱性,NaHSO3溶液呈酸性,说明电离程度大于水解程度,因此c(H2SO3)<c(SO32-);强碱溶液中的氢氧根离子能够与HSO3-电离出的氢离子反应生成水,促进HSO3-的电离平衡正向移动,反应生成亚硫酸钠,故答案为:<;强碱溶液中的氢氧根离子能够与HSO3-电离出的氢离子反应生成水,促进HSO3-的电离平衡正向移动,反应生成亚硫酸钠。