10.已知反应X(g)+Y(g)═nZ(g)△H<0,将X和Y以一定比例混合通入2L密闭容器中进行反应,各物质的物质的量随时间的改变如图.下列说法正确的是( )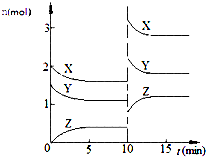

| A. | 反应方程式中n=2 | |
| B. | 该反应的△S>0 | |
| C. | 10 min时,曲线发生变化的原因是增大压强 | |
| D. | 0~5min内,平均反应速率v(X)=0.04 mol•L-1•min-1 |
9.溴化碘(IBr)的化学性质类似卤素单质,它与水反应的化学方程式是IBr+H2O=HBr+HIO.下列有关IBr的叙述不正确的是( )
| A. | IBr跟水的反应是非氧化还原反应 | |
| B. | 在很多反应中,IBr是强氧化剂 | |
| C. | IBr是共价化合物 | |
| D. | IBr跟NaOH稀溶液反应生成NaI、NaBrO和H2O |
8.化学工业与人类的生产生活息息相关,回答下列问题:
(1)已知反应:Fe(s)+CO2(g)?FeO(s)+CO(g)△H=a kJ?mol-1,平衡常数为K;
测得在不同温度下,K值如下:
①写出K的表达式$\frac{[CO]}{[CO2]}$.
②反应中的a大于0(填“大于”、“小于”或“等于”).
③若500℃时进行反应,CO2起始浓度为2mol?L-1,CO的平衡浓度为1mol?L-1.
④700℃反应达到平衡,此时增大反应中CO的浓度,该平衡移动后达到新的平衡,其它条件不变时,CO 和CO2的体积比值不变(填“增大”、“减小”或“不变”).
(2)工业固氮反应是:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol.在相同温度下,体积均为0.25L的两个恒容密闭容器中可发生上述可逆反应,测得反应的有关数据如表:
①容器a达平衡时N2的平衡浓度c(N2)=3mol?L-1.
②容器b达平衡时NH3的平衡浓度c(NH3)=2mol?L-1.
③下列叙述正确的是AB.
A.容器a达平衡时NH3的物质的量是0.5mol
B.容器b开始是向合成氨的逆反应方向进行
C.若容器a体积变为0.2L,则达平衡时放出的热量小于23.1kJ
D.不能利用已知数据计算容器b的平衡常数.
(1)已知反应:Fe(s)+CO2(g)?FeO(s)+CO(g)△H=a kJ?mol-1,平衡常数为K;
测得在不同温度下,K值如下:
| 温度/℃ | 500 | 700 | 900 |
| K | 1.00 | 1.47 | 2.40 |
②反应中的a大于0(填“大于”、“小于”或“等于”).
③若500℃时进行反应,CO2起始浓度为2mol?L-1,CO的平衡浓度为1mol?L-1.
④700℃反应达到平衡,此时增大反应中CO的浓度,该平衡移动后达到新的平衡,其它条件不变时,CO 和CO2的体积比值不变(填“增大”、“减小”或“不变”).
(2)工业固氮反应是:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol.在相同温度下,体积均为0.25L的两个恒容密闭容器中可发生上述可逆反应,测得反应的有关数据如表:
| 容器 编号 | 起始时各物质物质的量/mol | 达平衡时体系的 能量变化 | ||
| N2 | H2 | NH3 | ||
| a | 1 | 3 | 0 | 放热23.1kJ |
| b | 0.6 | 1.8 | 0.8 | 吸热Q kJ |
②容器b达平衡时NH3的平衡浓度c(NH3)=2mol?L-1.
③下列叙述正确的是AB.
A.容器a达平衡时NH3的物质的量是0.5mol
B.容器b开始是向合成氨的逆反应方向进行
C.若容器a体积变为0.2L,则达平衡时放出的热量小于23.1kJ
D.不能利用已知数据计算容器b的平衡常数.
5.25℃时,水中存在电离平衡:H2O?H++OH-.下列叙述正确的是( )
| A. | 将水加热,KW增大,pH变小,液体显酸性 | |
| B. | 向水中通入少量HCl气体,c(H+)增大,KW不变 | |
| C. | 向水中加入少量NaOH固体,平衡逆向移动,c(OH-)减小 | |
| D. | 向水中加入少量纯碱,平衡正向移动,c(H+)增大 |
4.下列有关电解质的说法正确的是( )
| A. | 离子化合物不一定是电解质,共价化合物可能是强电解质 | |
| B. | 强电解质都是离子化合物,而弱电解质都是共价化合物 | |
| C. | 电解质的水溶液都具有较强的导电性 | |
| D. | 易溶性强电解质的溶液中不存在溶质分子 |
3.在一密闭容器中充入1molH2和1molⅠ2,压强为p(Pa),保持温度不变,使其发生反应:H2(g)+I2(g)?2HI(g).一段时间后达平衡,下列关于该平衡的说法正确的是( )
| A. | 保持容器容积不变,向其中加入1molH2,平衡常数减小 | |
| B. | 保持容器容积不变,向其中加入1molHe,正逆反应速率均增大 | |
| C. | 保持容器内气体压强不变,向其中加入1molHe,反应速率均减小 | |
| D. | 保持容器内气体压强不变,再向其中加入1molH2和1molⅠ2,重新达平衡,H2的体积分数减小 |
2.若在加入铝粉能放出氢气的溶液中,分别加入下列各组离子,可能大量共存的是( )
| A. | NH4+、NO3-、CO32-、Na+ | B. | Na+、Ba2+、Mg2+、HCO3- | ||
| C. | NO3-、Ca2+、K+、Cl- | D. | NO3-、K+、ClO-、Ca2+ |
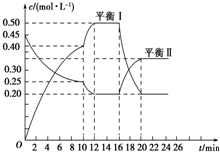
1.己知N2O4(g)?2NO2(g)△H=+57.20KJ•mol-1,t时,将一定量的NO2、N2O4,充入一个容器为2L的恒容密闭容器中,浓度随时间变化关系如下表所示:
①c( X)代表NO2(填化学式)的浓度,该反应的平衡常数K=0.9.(填具体数值)
②前10min内用NO2表示的反应速率为,20min时改变的条件是;重新达到平衡时,NO2的百分含量b(填选项前字母).
a.增大 b.减小 c.不变 d.无法判断.
0 173538 173546 173552 173556 173562 173564 173568 173574 173576 173582 173588 173592 173594 173598 173604 173606 173612 173616 173618 173622 173624 173628 173630 173632 173633 173634 173636 173637 173638 173640 173642 173646 173648 173652 173654 173658 173664 173666 173672 173676 173678 173682 173688 173694 173696 173702 173706 173708 173714 173718 173724 173732 203614
| 时间/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| c(X)/(mol/L) | 0.2 | c | 0.6 | 0.6 | 1.0 | c1 | c1 |
| c(Y)/(mol/L) | 0.6 | c | 0.4 | 0.4 | 0.4 | c2 | c2 |
②前10min内用NO2表示的反应速率为,20min时改变的条件是;重新达到平衡时,NO2的百分含量b(填选项前字母).
a.增大 b.减小 c.不变 d.无法判断.