题目内容
5.25℃时,水中存在电离平衡:H2O?H++OH-.下列叙述正确的是( )| A. | 将水加热,KW增大,pH变小,液体显酸性 | |
| B. | 向水中通入少量HCl气体,c(H+)增大,KW不变 | |
| C. | 向水中加入少量NaOH固体,平衡逆向移动,c(OH-)减小 | |
| D. | 向水中加入少量纯碱,平衡正向移动,c(H+)增大 |
分析 水的电离平衡:H2O?H++OH-中,要使平衡发生移动,应改变溶液c(H+)或c(OH-)的浓度,水的电离是吸热过程,升高温度,平衡向电离方向移动,K增大,c(H+),则pH减小.据此分析.
解答 解:解:A.水的电离是吸热过程,升高温度,平衡向电离方向移动,Kw增大,c(H+)增大,则pH减小,故A错误;
B.向水中加入少量HCl,导致c(H+)增大,平衡逆向移动,Kw只受温度的影响,温度不变,Kw不变,故B正确;
C.向水中加入少量固体NaOH,c(OH-)增大,平衡逆向移动,c(H+)降低,c(OH-)增大,故C错误;
D.向水中加入少量纯碱碳酸钠,碳酸根离子会和氢离子反应,c(H+)减小,导致平衡正向移动,c(OH-)增大,故D错误.
故选B.
点评 本题考查水的电离平衡移动,题目难度不大,注意从浓度、温度对平衡移动的影响角度分析,本题易错点为A,注意升高温度c(H+)增大,pH减小.

练习册系列答案
相关题目
16.三苯甲醇(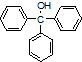 )是一种重要的化工原料和医药中间体,实 验室合成三苯
)是一种重要的化工原料和医药中间体,实 验室合成三苯
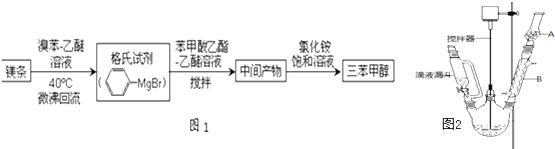
甲醇其合成流程如图1所示,装置如图2所示.
已知:(I)格氏试剂容易水解,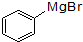 +H2O
+H2O +Mg(OH)Br(碱式溴化镁);
+Mg(OH)Br(碱式溴化镁);
(II)相关物质的物理性质如下:
(III)三苯甲醇的分子量是260,纯净固体有机物一般都有固定熔点.
请回答以下问题:
(1)图2中玻璃仪器B的名称:冷凝管;装有无水CaCl2的仪器A的作用是防止空气中的水蒸气进入装置,避免格氏试剂水解;
(2)图2中滴加液体未用普通分液漏斗而用滴液漏斗的作用是平衡压强,使漏斗内液体顺利滴下;制取格氏试剂时要保持微沸,可以采用水浴(方式)加热,优点是受热均匀,温度易于控制;
(3)制得的三苯甲醇粗产品中,含有乙醚、溴苯、苯甲酸乙酯等有机物和碱式溴化镁等杂质,可以设计如下提纯方案,请填写如下空白:
[粗产品]$\stackrel{①操作}{→}$ $\stackrel{②溶解、过滤}{→}$ $\stackrel{③洗涤、干燥}{→}$[三苯甲醇]其中,①操作为:蒸馏或分馏;洗涤液最好选用:A(从选项中选);
A、水 B、乙醚 C、乙醇 D、苯
检验产品已经洗涤干净的操作为:取少量最后一次洗涤液于试管中,滴加硝酸银溶液,若无沉淀生成,则已洗涤干净,反之则未洗涤干净.
(4)纯度测定:称取2.60g产品,配成乙醚溶液,加入足量金属钠(乙醚与钠不会反应),充分反应后,测得生成气体体积为100.80ml标准状况).产品中三苯甲醇质量分数为90%(保留两位有效数字).
 )是一种重要的化工原料和医药中间体,实 验室合成三苯
)是一种重要的化工原料和医药中间体,实 验室合成三苯甲醇其合成流程如图1所示,装置如图2所示.
已知:(I)格氏试剂容易水解,
 +H2O
+H2O +Mg(OH)Br(碱式溴化镁);
+Mg(OH)Br(碱式溴化镁);
(II)相关物质的物理性质如下:
| 物质 | 熔点 | 沸点 | 溶解性 |
| 三苯甲醇 | 164.2℃ | 380℃ | 不溶于水,溶于乙醇、乙醚等有机溶剂 |
| 乙醚 | -116.3℃ | 34.6℃ | 微溶于水,溶于乙醇、苯等有机溶剂 |
| 溴苯 | -30.7°C | 156.2°C | 不溶于水,溶于乙醇、乙醚等多数有机溶剂 |
| 苯甲酸乙酯 | -34.6°C | 212.6°C | 不溶于水 |
| Mg(OH)Br | 常温下为固体 | 能溶于水,不溶于醇、醚等有机溶剂 | |
请回答以下问题:
(1)图2中玻璃仪器B的名称:冷凝管;装有无水CaCl2的仪器A的作用是防止空气中的水蒸气进入装置,避免格氏试剂水解;
(2)图2中滴加液体未用普通分液漏斗而用滴液漏斗的作用是平衡压强,使漏斗内液体顺利滴下;制取格氏试剂时要保持微沸,可以采用水浴(方式)加热,优点是受热均匀,温度易于控制;
(3)制得的三苯甲醇粗产品中,含有乙醚、溴苯、苯甲酸乙酯等有机物和碱式溴化镁等杂质,可以设计如下提纯方案,请填写如下空白:
| 粗产品 | ① 操作 | ②溶解、过滤 | ③洗涤、干燥 | 三苯甲醇 |
A、水 B、乙醚 C、乙醇 D、苯
检验产品已经洗涤干净的操作为:取少量最后一次洗涤液于试管中,滴加硝酸银溶液,若无沉淀生成,则已洗涤干净,反之则未洗涤干净.
(4)纯度测定:称取2.60g产品,配成乙醚溶液,加入足量金属钠(乙醚与钠不会反应),充分反应后,测得生成气体体积为100.80ml标准状况).产品中三苯甲醇质量分数为90%(保留两位有效数字).
10.已知反应X(g)+Y(g)═nZ(g)△H<0,将X和Y以一定比例混合通入2L密闭容器中进行反应,各物质的物质的量随时间的改变如图.下列说法正确的是( )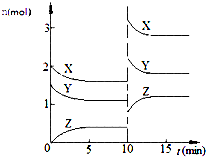

| A. | 反应方程式中n=2 | |
| B. | 该反应的△S>0 | |
| C. | 10 min时,曲线发生变化的原因是增大压强 | |
| D. | 0~5min内,平均反应速率v(X)=0.04 mol•L-1•min-1 |
17.下列关于苯的说法错误的是( )
| A. | 苯环中含有单双键交替的化学键 | |
| B. | 苯不能使酸性高锰酸钾溶液和溴水褪色 | |
| C. | 苯的化学性质没显示出极不饱和的性质,其性质与烯烃有很大的差别 | |
| D. | 苯在氢气气存在的情况下可以发生如下转化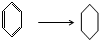 |
14.下列说法正确的是( )
| A. | 用30%的H2O2消除面部色斑 | |
| B. | 当不慎在皮肤上沾上少量的浓H2SO4时,应立即用大量水冲洗,并涂上2%的NaHCO3溶液 | |
| C. | 试样$\stackrel{BaCl_{2}}{→}$ 白色沉淀$\stackrel{HCl}{→}$白色沉淀不溶解,则试样中一定有SO42- | |
| D. | 不慎将浓盐酸洒在桌上,应立即用浓NaOH溶液冲洗 |