14.某溶液中,若忽略水的电离,只含有下表中所示的四种离子,试推测X离子及其个数b可能为( )
| 离子 | Na+ | Ba2+ | Cl- | X |
| 个数 | 3a | 2a | a | b |
| A. | NO3-、4a | B. | CO32-、3a | C. | OH-、6a | D. | SO42-、3a |
13.下列离子方程式书写正确的是( )
| A. | Na放入水中:Na+2H2O=Na++OH-+2H2↑ | |
| B. | 碳酸钙溶于醋酸中:CaCO3+2H+═Ca2++2H2O+CO2↑ | |
| C. | 硝酸银溶液中加入铜粉:2Ag++Cu═Cu2++2Ag | |
| D. | Ba(OH)2与稀H2SO4反应:Ba2++OH-+H++SO42-═BaSO4↓+H2O |
12.对于某些常见离子的检验及结论一定正确的是( )
| A. | 加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32- | |
| B. | 加入氯化钠溶液有白色沉淀产生,再加稀硝酸沉淀不消失,一定有Ag+ | |
| C. | 加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+ | |
| D. | 加入氯化钡溶液有白色沉淀产生,再加盐酸沉淀不消失,一定有SO42- |
11.对胶体的下列叙述不正确的是( )
| A. | 加电解质可使某种胶体聚沉,这是中和胶体粒子所带电荷的缘故 | |
| B. | 胶体粒子在直流电场中做定向移动,这是胶体粒子选择性吸附离子而带电荷的缘故 | |
| C. | 一束光线通过胶体时有丁达尔效应,这是胶体粒子对光散射的缘故 | |
| D. | 由于胶体粒子带电荷,所以胶体这种分散系不是电中性的 |
10.下列物质能导电,但属于电解质的是( )
| A. | 纯净的硫酸 | B. | KNO3 溶液 | C. | NH4HCO3固体 | D. | 熔融的KCl |
9.现有①液态氧 ②氢氧化铁胶体 ③食盐水 ④纯碱 ⑤氢氧化钾 ⑥空气 对上述物质的分类全部正确的是( )
0 172616 172624 172630 172634 172640 172642 172646 172652 172654 172660 172666 172670 172672 172676 172682 172684 172690 172694 172696 172700 172702 172706 172708 172710 172711 172712 172714 172715 172716 172718 172720 172724 172726 172730 172732 172736 172742 172744 172750 172754 172756 172760 172766 172772 172774 172780 172784 172786 172792 172796 172802 172810 203614
| A. | 盐 ③④ | B. | 混合物 ②③⑥ | C. | 纯净物 ④⑤⑥ | D. | 碱 ④⑤ |
 .
.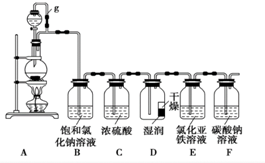 某探究小组为探究氯气的性质,并用装置F制取少量“漂白液”,设计了如下实验装置.请回答下列问题:
某探究小组为探究氯气的性质,并用装置F制取少量“漂白液”,设计了如下实验装置.请回答下列问题: