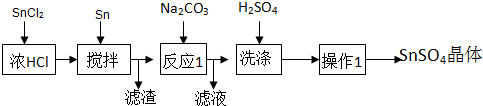
3.设NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 标准状况下,22.4 L己烷中共价键数目为19NA | |
| B. | 12.4g白磷晶体中含有的P-P键数是0.1NA | |
| C. | 2mol SO2和1mol O2混合在V2O5存在的条件下,密闭容器中加热反应后,容器内物质的分子数大于2NA | |
| D. | 将NO2和N2O4分子共NA个降温至标准状况下,其体积为22.4 L |
18. 将0.8mol I2(g)和1.2mol H2(g)置于某1L密闭容器中,在一定温度下发生反应:I2(g)+H2(g)?2HI(g)并达到平衡.HI的体积分数随时间的变化如表格所示:
将0.8mol I2(g)和1.2mol H2(g)置于某1L密闭容器中,在一定温度下发生反应:I2(g)+H2(g)?2HI(g)并达到平衡.HI的体积分数随时间的变化如表格所示:
(1)在条件I到达平衡时,计算该反应的平衡常数K=12.
(2)在条件I从开始反应到到达平衡时,H2的反应速率为0.12 mol/(L•min).
(3)为达到条件II的数据,对于反应体系可能改变的操作是降低温度.
(4)该反应的△H<0(填“>“,“<“或“=“)
(5)在条件I下达到平衡后,在7min时将容器体积压缩为原来的一半.请在图中画出c(HI)随时间变化的曲线.
 将0.8mol I2(g)和1.2mol H2(g)置于某1L密闭容器中,在一定温度下发生反应:I2(g)+H2(g)?2HI(g)并达到平衡.HI的体积分数随时间的变化如表格所示:
将0.8mol I2(g)和1.2mol H2(g)置于某1L密闭容器中,在一定温度下发生反应:I2(g)+H2(g)?2HI(g)并达到平衡.HI的体积分数随时间的变化如表格所示:| HI体积分数 | 1min | 2min | 3min | 4min | 5min | 6min | 7min |
| 条件I | 26% | 42% | 52% | 57% | 60% | 60% | 60% |
| 条件II | 20% | 33% | 43% | 52% | 57% | 65% | 65% |
(2)在条件I从开始反应到到达平衡时,H2的反应速率为0.12 mol/(L•min).
(3)为达到条件II的数据,对于反应体系可能改变的操作是降低温度.
(4)该反应的△H<0(填“>“,“<“或“=“)
(5)在条件I下达到平衡后,在7min时将容器体积压缩为原来的一半.请在图中画出c(HI)随时间变化的曲线.
14.已知反应2CH3OH(g)?CH3OCH3(g)+H2O(g)某温度下的平衡常数为400.此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
下列叙述中正确的是( )
0 172530 172538 172544 172548 172554 172556 172560 172566 172568 172574 172580 172584 172586 172590 172596 172598 172604 172608 172610 172614 172616 172620 172622 172624 172625 172626 172628 172629 172630 172632 172634 172638 172640 172644 172646 172650 172656 172658 172664 172668 172670 172674 172680 172686 172688 172694 172698 172700 172706 172710 172716 172724 203614
| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度(mol•L-1) | 0.44 | 0.6 | 0.6 |
| A. | 该反应的平衡常数表达式为:K=[c(CH3OCH3)×c(H2O)]/c(CH3OH) | |
| B. | 此时正、逆反应速率的大小:v正<v逆 | |
| C. | 若加入CH3OH后,经10 min达到平衡,此时c(CH3OH)=0.04 mol/L | |
| D. | 10 min达到平衡时,反应速率v(CH3OH)=1.6 mol/(L•min) |
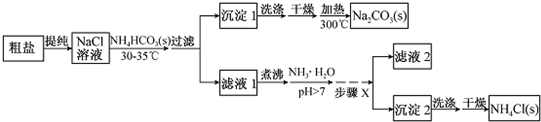
 在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应).生成物中含有Cl-、C1O-、C1O3-三种含氯元素的离子,其中C1O-、C1O3-两种离子的物质的量(n)与反应时间(t)的曲线如图所示.
在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应).生成物中含有Cl-、C1O-、C1O3-三种含氯元素的离子,其中C1O-、C1O3-两种离子的物质的量(n)与反应时间(t)的曲线如图所示.