��Ŀ����
20��I�����¡���ѹ�£���һ���ɱ��ݻ��������з������·�Ӧ��A������+B������?C��������1������ʼʱ����1molA��1molB������ƽ�������a molC����ʱA�����ʵ���Ϊ��1-a��mol��
��2������ʼʱ����3molA��3molB������ƽ�������C�����ʵ���Ϊ3amol��
��3������ʼʱ����x molA��2molB��1molC������ƽ���A��C�����ʵ����ֱ���ymol��3a mol����x=2mol��y=3��1-a��mol��ƽ��ʱ��B�����ʵ�����������ѡ��һ����ţ�
���ף�����2mol ���ң�����2mol
������С��2mol ���������ܴ��ڡ����ڻ�С��2mol
�������жϵ�������ƽ��ʱBΪ3��1-a��mol������0��a��1����3��1-a�����ܴ��ڡ����ڻ�С��2��
��4�����ڣ�3����ƽ���������ټ���3molC�����ٴε���ƽ���C�����ʵ���������$\frac{a}{2-a}$��
II����ά���¶Ȳ��䣬��һ���루1����Ӧǰ��ʼ�����ͬ�����ݻ��̶��������з���������Ӧ��
��5����ʼʱ����1molA��1molB����ƽ�������b molC����b�루1��С���е�a���бȽ��ң�ѡ��һ����ţ���
���ף�a��b ���ң�a��b ������a=b ���������ܱȽ�a��b�Ĵ�С�������жϵ���������Ϊ��С���������ݻ����䣬����1��С�����������ݻ���С�����Ա�С��������е�ѹ��С�ڣ�1��С�������е�ѹ��������������Ӧ��
���� I����1���ɷ���ʽ��֪������C�����ʵ���=�μӷ�ӦA�����ʵ�����ƽ��ʱA�����ʵ���=A����ʼ���ʵ���-�μӷ�Ӧ��A�����ʵ�����
��2�����º�ѹ�£�����ʼʱ����3mol A��3mol B���루1����A��B�����ʵ���֮�Ⱦ�Ϊ1��1����Ϊ��Чƽ�⣬ƽ��ʱ��Ӧ���ת������ͬ��
��3������ʼʱ����x mol A��2mol B��1mol C����ȫת�����������3mol A��3mol B���루1����A��B�����ʵ���֮�Ⱦ�Ϊ1��1����Ϊ��Чƽ�⣬ƽ��ʱ��Ӧ���ת������ͬ�����Եõ�3amol C��ƽ��ʱA��B�����ʵ����ֱ�Ϊ��1����A��B��3�������a��1�жϣ�
��4���ɣ�3��������֪�����ڣ�3����ƽ���������ټ���3mol C����ЧΪ��ʼ����6mol A��6mol B���루1����ƽ��Ϊ��Чƽ�⣬ƽ��ʱ��Ӧ���ת������ͬ����ƽ��ʱC�����ʵ��������루1������ͬ��
��5����ӦA��g��+B��g��?C��g��������������ٵķ�Ӧ���ں��º��������У��淴Ӧ����ѹǿ��С�����ں��º�ѹ�������淴Ӧ���У������е�ѹǿΪ���ֺ�ѹ������������е�ѹ��С�ڣ�1��С�������е�ѹ��������������Ӧ��
��� �⣺I����1���ﵽƽ�������a mol C�����n��A��=��n��C��=amol����A�����ʵ���Ϊ1mol-amol=��1-a��mol��
�ʴ�Ϊ����1-a����
��2�����º�ѹ�£�����ʼʱ����3mol A��3mol B���루1����A��B�����ʵ���֮�Ⱦ�Ϊ1��1����Ϊ��Чƽ�⣬ƽ��ʱ��Ӧ���ת������ͬ����ƽ��ʱ����CΪ��1���е�3����������CΪ3amol��
�ʴ�Ϊ��3a��
��3������ʼʱ����x mol A��2mol B��1mol C����ȫת�����������3mol A��3mol B���루1����A��B�����ʵ���֮�Ⱦ�Ϊ1��1����Ϊ��Чƽ�⣬ƽ��ʱ��Ӧ���ת������ͬ�����Եõ�3amol C��1molCת�����Եõ�1molA��1molB����x=3-1=2����ƽ��ʱAΪ3��1-a��mol��ƽ��ʱB�����ʵ���Ϊ��1����B��3������Ϊ3��1-a��mol������0��a��1����3��1-a�����ܴ��ڡ����ڻ�С��2��
�ʴ�Ϊ��2��3��1-a������������ƽ��ʱBΪ3��1-a��mol������0��a��1����3��1-a�����ܴ��ڡ����ڻ�С��2��
��4���ɣ�3��������֪�����ڣ�3����ƽ���������ټ���3mol C����ЧΪ��ʼ����6mol A��6mol B���루1����ƽ��Ϊ��Чƽ�⣬ƽ��ʱ��Ӧ���ת������ͬ����ƽ��ʱC�����ʵ��������루1������ͬ����C�����ʵ�������Ϊ $\frac{amol}{��1-a��mol+��1-a��mol+amol}$=$\frac{a}{2-a}$��
�ʴ�Ϊ��$\frac{a}{2-a}$��
��5���ں��º�ѹ�����п�ʼʱ����1molA��1molB����ƽ�������amol C���ں��º��������п�ʼʱ����1molA��1molB����ƽ�������b molC����ӦA��g��+B��g��?C��g��������������ٵķ�Ӧ���ں��º��������У��淴Ӧ����ѹǿ��С���ں��º�ѹ�������淴Ӧ���У������е�ѹǿΪ���ֺ�ѹ�������С�����Ա���������е�ѹ��С�ڣ�1��С�������е�ѹ��������������Ӧ�����ƽ���b��a��
�ʴ�Ϊ���ң���Ϊ��С���������ݻ����䣬����1��С�����������ݻ���С�����Ա�С��������е�ѹ��С�ڣ�1��С�������е�ѹ��������������Ӧ��
���� ���⿼�黯ѧƽ���йؼ��㡢��Чƽ�����⣬������ø������������������ݵ�Чƽ������������DZ���Ĺؼ������ֺ��º��������ͺ��º�ѹ�����IJ�ͬ���ѶȽϴ�

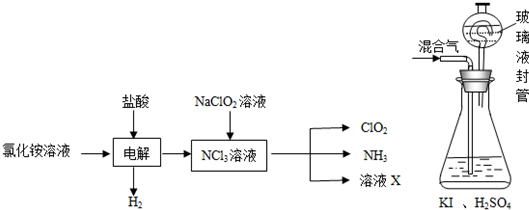
 A��B��C����ǿ����ʣ�������ˮ�е���������������ʾ��
A��B��C����ǿ����ʣ�������ˮ�е���������������ʾ��| ������ | Ag+������Na+ |
| ������ | NO3-����SO42-������Cl- |
��1��MΪ��Դ�ĸ������������������e�缫�ϲ������������Ϊ2.8L����״���£���
��2��e�缫�Ϸ����ĵ缫��ӦΪ2H++2e-=H2����
| A�� | ͭ����������Һ��Ӧ Cu+Ag+�TCu2++Ag | |
| B�� | CH3COOH��Һ��NaOH��Һ��Ӧ H++OH-�TH2O | |
| C�� | ̼��þ��ϡH2SO4��Ӧ MgCO3+2H+�TMg2++H2O+CO2�� | |
| D�� | ʯ������ϡ���ᷴӦ H++OH-�TH2O |
| A�� | 0.01mol | B�� | 0.1mol | C�� | 0.02mol | D�� | 0.2mol |