4. 实验室需配制0.2000mol•L -1Na2S2O3标准溶液450mL,并利用该溶液对某浓度的NaClO溶液进行标定.
实验室需配制0.2000mol•L -1Na2S2O3标准溶液450mL,并利用该溶液对某浓度的NaClO溶液进行标定.
(1)若用Na2S2O3固体来配制标准溶液,在如图所示的仪器中,不必要用到的仪器是AB(填字母),还缺少的玻璃仪器是烧杯、玻璃棒(填仪器名称).
(2)根据计算需用天平称取Na2S2O3固体的质量是15.8g.在实验中其他操作均正确,若容量瓶用蒸馏水洗涤后未干燥,则所得溶液浓度=(填“>”“<”或“=”,下同)0.2000mol•L-1.若还未等溶液冷却就定容了,则所得溶液浓度>0.2000mol•L-1.
(3)用滴定法标定的具体方法:量取20.00mL NaClO溶液于锥形瓶中,加入适量稀盐酸和足量KI固体,用0.2000mol•L -1 Na2S2O3标准溶液滴定至终点(淀粉溶液作指示剂),四次平行实验测定的V(Na2S2O3)数据如下:
(已知:I2+2Na2S2O3═2NaI+Na2S4O6)
①NaClO溶液中加入适量稀盐酸和足量KI固体时发生反应的离子方程式为ClO-+2I-+2H+═Cl-+I2+H2O.
②NaClO溶液的物质的量浓度是0.1060 mol•L -1.
 实验室需配制0.2000mol•L -1Na2S2O3标准溶液450mL,并利用该溶液对某浓度的NaClO溶液进行标定.
实验室需配制0.2000mol•L -1Na2S2O3标准溶液450mL,并利用该溶液对某浓度的NaClO溶液进行标定.(1)若用Na2S2O3固体来配制标准溶液,在如图所示的仪器中,不必要用到的仪器是AB(填字母),还缺少的玻璃仪器是烧杯、玻璃棒(填仪器名称).
(2)根据计算需用天平称取Na2S2O3固体的质量是15.8g.在实验中其他操作均正确,若容量瓶用蒸馏水洗涤后未干燥,则所得溶液浓度=(填“>”“<”或“=”,下同)0.2000mol•L-1.若还未等溶液冷却就定容了,则所得溶液浓度>0.2000mol•L-1.
(3)用滴定法标定的具体方法:量取20.00mL NaClO溶液于锥形瓶中,加入适量稀盐酸和足量KI固体,用0.2000mol•L -1 Na2S2O3标准溶液滴定至终点(淀粉溶液作指示剂),四次平行实验测定的V(Na2S2O3)数据如下:
(已知:I2+2Na2S2O3═2NaI+Na2S4O6)
| 测定次序 | 第一次 | 第二次 | 第三次 | 第四次 |
| V(Na2S2O3)/mL | 21.90 | 18.80 | 22.10 | 22.00 |
②NaClO溶液的物质的量浓度是0.1060 mol•L -1.
3.已知:5S2O82-+2Mn2++8H2O═2MnO4-+10SO42-+16X,对于该反应下列叙述不正确的是( )
| A. | 氧化剂和还原剂的物质的量之比为2:5 | |
| B. | 该反应体系不能用盐酸酸化 | |
| C. | 若有0.1 mol还原剂被氧化,则转移电子0.5 mol | |
| D. | 若把该反应设计为原电池,则正极反应为S2O82--2e-═2SO42- |
2.下列说法正确的是( )
| A. | 石油是烃的衍生物的混合物 | |
| B. | 核磁共振(1H-NMR)、红外光谱、质谱法等都是现代化学测定有机化合物结构的分析方法 | |
| C. | 有机物都易溶于有机溶剂,且熔、沸点低,容易燃烧,受热易分解 | |
| D. | 蛋白质溶液中加入重金属盐能够降低蛋白质的溶解性,使蛋白质转变为沉淀析出 |
1.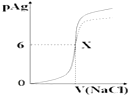 如图是向10mLAgNO3溶液中逐渐加入0.1mol/L的NaCl溶液时,溶液的pAg随着加入NaCl溶液的体积(单位mL)变化的图象(实线).已知:pAg=-lg{c(Ag+)},Ksp(AgCl)=1×10-12.根据图象所得下列结论正确的是( )(提示:Ksp(AgCl)>Ksp(AgI))
如图是向10mLAgNO3溶液中逐渐加入0.1mol/L的NaCl溶液时,溶液的pAg随着加入NaCl溶液的体积(单位mL)变化的图象(实线).已知:pAg=-lg{c(Ag+)},Ksp(AgCl)=1×10-12.根据图象所得下列结论正确的是( )(提示:Ksp(AgCl)>Ksp(AgI))
 如图是向10mLAgNO3溶液中逐渐加入0.1mol/L的NaCl溶液时,溶液的pAg随着加入NaCl溶液的体积(单位mL)变化的图象(实线).已知:pAg=-lg{c(Ag+)},Ksp(AgCl)=1×10-12.根据图象所得下列结论正确的是( )(提示:Ksp(AgCl)>Ksp(AgI))
如图是向10mLAgNO3溶液中逐渐加入0.1mol/L的NaCl溶液时,溶液的pAg随着加入NaCl溶液的体积(单位mL)变化的图象(实线).已知:pAg=-lg{c(Ag+)},Ksp(AgCl)=1×10-12.根据图象所得下列结论正确的是( )(提示:Ksp(AgCl)>Ksp(AgI))| A. | 原AgNO3溶液的物质的量浓度为0.1 mol•L-1 | |
| B. | 图中x点的坐标为(100,6 ) | |
| C. | 图中x点可认为溶液中Ag+被沉淀完全 | |
| D. | 把0.1 mol•L-1的NaCl换成0.1 mol•L-1NaI则图象在终点后变为虚线部分 |
19.下表是元素周期表的一部分,针对表中的①~⑧中元素,填空回答.
(1)在这些元素中,化学性质最不活泼的原子的原子结构示意图为 .
.
(2)③⑤⑦元素原子形成简单离子的离子半径由大到小的顺序是Cl->F->Al3+(填离子符号).
(3)某元素二价阳离子的核外有10个电子,该元素是镁(填元素名称).
(4)④的单质与水反应的化学方程式是 (并标出电子转移的方向与数目).
(并标出电子转移的方向与数目).
(5)⑦元素的单质常温下的颜色是黄绿色,用电子式表示⑦元素的氢化物形成过程为
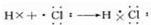 .
.
(6)已知某些不同族元素的性质也有一定的相似性,如元素①与⑤元素的氢氧化物有相似的性质,写出元素①的氢氧化物与NaOH溶液反应的化学方程式Be(OH)2+2NaOH=Na2BeO2+2H2O.
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | |||||
| 三 | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
 .
.(2)③⑤⑦元素原子形成简单离子的离子半径由大到小的顺序是Cl->F->Al3+(填离子符号).
(3)某元素二价阳离子的核外有10个电子,该元素是镁(填元素名称).
(4)④的单质与水反应的化学方程式是
 (并标出电子转移的方向与数目).
(并标出电子转移的方向与数目).(5)⑦元素的单质常温下的颜色是黄绿色,用电子式表示⑦元素的氢化物形成过程为
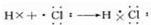 .
.(6)已知某些不同族元素的性质也有一定的相似性,如元素①与⑤元素的氢氧化物有相似的性质,写出元素①的氢氧化物与NaOH溶液反应的化学方程式Be(OH)2+2NaOH=Na2BeO2+2H2O.
18.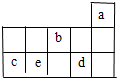 a、b、c、d、e为元素周期表前3周期中的部分元素,它们在元素周期表中的相对位置如图所示.下列叙述正确的是( )
a、b、c、d、e为元素周期表前3周期中的部分元素,它们在元素周期表中的相对位置如图所示.下列叙述正确的是( )
 a、b、c、d、e为元素周期表前3周期中的部分元素,它们在元素周期表中的相对位置如图所示.下列叙述正确的是( )
a、b、c、d、e为元素周期表前3周期中的部分元素,它们在元素周期表中的相对位置如图所示.下列叙述正确的是( )| A. | b元素除0价外,只有一种化合价 | |
| B. | 五种元素中,c元素的性质最稳定 | |
| C. | d气态氢化物溶于水,溶液显碱性 | |
| D. | e元素最高价氧化物对应的水化物和不同量的氢氧化钠反应,可能生成三种盐 |
17.表为元素周期表的一部分.
(1)表中元素F的非金属性最强;元素K的金属性最强;元素Br的单质室温下呈液态(填写元素符号);
(2)表中元素⑤的原子结构示意图是 ;
;
(3)表中元素⑥⑨⑩氢化物的稳定性顺序为HF>HCl>H2S(填化学式);
(4)表中元素⑨和⑩最高价氧化物对应水化物的酸性:HClO4>H2SO4(填化学式);
(5)表中元素②的最高价氧化物属于两性氧化物(选填“酸性氧化物、两性氧化物、碱性氧化物”).
0 171953 171961 171967 171971 171977 171979 171983 171989 171991 171997 172003 172007 172009 172013 172019 172021 172027 172031 172033 172037 172039 172043 172045 172047 172048 172049 172051 172052 172053 172055 172057 172061 172063 172067 172069 172073 172079 172081 172087 172091 172093 172097 172103 172109 172111 172117 172121 172123 172129 172133 172139 172147 203614
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 一 | ① | ||||||
| 二 | ③ | ④ | ⑤ | ⑥ | |||
| 三 | ⑦ | ⑧ | ② | ⑨ | ⑩ | ||
| 四 | ⑪ | ⑫ | |||||
(2)表中元素⑤的原子结构示意图是
 ;
;(3)表中元素⑥⑨⑩氢化物的稳定性顺序为HF>HCl>H2S(填化学式);
(4)表中元素⑨和⑩最高价氧化物对应水化物的酸性:HClO4>H2SO4(填化学式);
(5)表中元素②的最高价氧化物属于两性氧化物(选填“酸性氧化物、两性氧化物、碱性氧化物”).