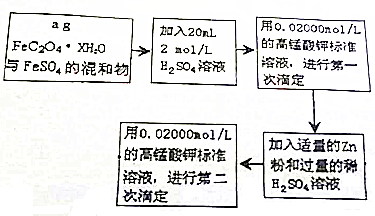
1.苯甲酸乙酯(C9H10O2)别名为安息香酸乙酯. 它是一种无色透明液体,不溶于水,稍有水果气味,用于配制香水香精和人造精油,大量用于食品工业中,也可用作有机合成中间体,溶剂等.其制备方法为:

已知:
*苯甲酸在100℃会迅速升华.
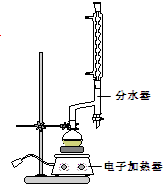 实验步骤如下:
实验步骤如下:
①在圆底烧瓶中加入12.20g苯甲酸,25mL 95%的乙醇(过量),20mL环己烷以及4mL浓硫酸,混合均匀并加入沸石,按图所示装好仪器,控制温度在65~70℃加热回流2h.利用分水器不断分离除去反应生成的水,回流环己烷和乙醇.
②反应结束,打开旋塞放出分水器中液体后,关闭旋塞,继续加热,至分水器中收集到的液体不再明显增加,停止加热.
③将烧瓶内反应液倒入盛有适量水的烧杯中,分批加入Na2CO3至溶液至呈中性.用分液漏斗分出有机层,水层用25mL乙醚萃取分液,然后合并至有机层,加入氯化钙,静置,过滤,对滤液进行蒸馏,低温蒸出乙醚和环己烷后,继续升温,接收210~213℃的馏分.
④检验合格,测得产品体积为12.86mL.
回答下列问题:
(1)在该实验中,圆底烧瓶的容积最适合的是(填入正确选项前的字母)C.
A.25mL B.50mL C.100mL D.250mL
(2)步骤①中使用分水器不断分离除去水的目的是使平衡不断地向正向移动.
(3)步骤②中应控制馏分的温度在C.
A.65~70℃B.78~80℃C.85~90℃D.215~220℃
(4)步骤③加入Na2CO3的作用是除去苯甲酸乙酯中的苯甲酸;若Na2CO3加入不足,在之后蒸馏时,蒸馏烧瓶中可见到白烟生成,产生该现象的原因是在苯甲酸乙酯中有未除净的苯甲酸,受热至100℃时升华.
(5)关于步骤③中的萃取分液操作叙述正确的是AD
A.水溶液中加入乙醚,转移至分液漏斗中,塞上玻璃塞,分液漏斗倒转过来,用力振摇
B.振摇几次后需打开分液漏斗上口的玻璃塞放气
C.经几次振摇并放气后,手持分液漏斗静置待液体分层
D.放出液体时,应打开上口玻璃塞或将玻璃塞上的凹槽对准漏斗口上的小孔
(6)计算本实验的产率为90.02%.

已知:
| 名称 | 相对分子质量 | 颜色,状态 | 沸点(℃) | 密度(g•cm-3) |
| 苯甲酸* | 122 | 无色片状晶体 | 249 | 1.2659 |
| 苯甲酸乙酯 | 150 | 无色澄清液体 | 212.6 | 1.05 |
| 乙醇 | 46 | 无色澄清液体 | 78.3 | 0.7893 |
| 环己烷 | 84 | 无色澄清液体 | 80.8 | 0.7318 |
 实验步骤如下:
实验步骤如下:①在圆底烧瓶中加入12.20g苯甲酸,25mL 95%的乙醇(过量),20mL环己烷以及4mL浓硫酸,混合均匀并加入沸石,按图所示装好仪器,控制温度在65~70℃加热回流2h.利用分水器不断分离除去反应生成的水,回流环己烷和乙醇.
②反应结束,打开旋塞放出分水器中液体后,关闭旋塞,继续加热,至分水器中收集到的液体不再明显增加,停止加热.
③将烧瓶内反应液倒入盛有适量水的烧杯中,分批加入Na2CO3至溶液至呈中性.用分液漏斗分出有机层,水层用25mL乙醚萃取分液,然后合并至有机层,加入氯化钙,静置,过滤,对滤液进行蒸馏,低温蒸出乙醚和环己烷后,继续升温,接收210~213℃的馏分.
④检验合格,测得产品体积为12.86mL.
回答下列问题:
(1)在该实验中,圆底烧瓶的容积最适合的是(填入正确选项前的字母)C.
A.25mL B.50mL C.100mL D.250mL
(2)步骤①中使用分水器不断分离除去水的目的是使平衡不断地向正向移动.
(3)步骤②中应控制馏分的温度在C.
A.65~70℃B.78~80℃C.85~90℃D.215~220℃
(4)步骤③加入Na2CO3的作用是除去苯甲酸乙酯中的苯甲酸;若Na2CO3加入不足,在之后蒸馏时,蒸馏烧瓶中可见到白烟生成,产生该现象的原因是在苯甲酸乙酯中有未除净的苯甲酸,受热至100℃时升华.
(5)关于步骤③中的萃取分液操作叙述正确的是AD
A.水溶液中加入乙醚,转移至分液漏斗中,塞上玻璃塞,分液漏斗倒转过来,用力振摇
B.振摇几次后需打开分液漏斗上口的玻璃塞放气
C.经几次振摇并放气后,手持分液漏斗静置待液体分层
D.放出液体时,应打开上口玻璃塞或将玻璃塞上的凹槽对准漏斗口上的小孔
(6)计算本实验的产率为90.02%.
19.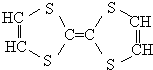 用于制造隐形飞机的物质具有吸收微波的功能,其主要成分的结构如图,关于该分子的说法正确的有( )
用于制造隐形飞机的物质具有吸收微波的功能,其主要成分的结构如图,关于该分子的说法正确的有( )
 用于制造隐形飞机的物质具有吸收微波的功能,其主要成分的结构如图,关于该分子的说法正确的有( )
用于制造隐形飞机的物质具有吸收微波的功能,其主要成分的结构如图,关于该分子的说法正确的有( )| A. | 分子中含有碳碳双键,属于烯烃 | |
| B. | 从碳骨架形状分析,应该属于环状烃 | |
| C. | 该分子属于高分子化合物 | |
| D. | 该分子中即有极性键,也有非极性键 |
15.一定条件下,可逆反应N2+3H2?2NH3,处于平衡状态的是( )
| A. | 单位时间内每消耗1molN2,同时消耗1molNH3 | |
| B. | 单位时间内每断裂3molH-H键,同时断裂2molN-H键 | |
| C. | N2、H2、NH3的浓度之比为1:3:2 | |
| D. | NH3的质量分数不再改变 |
14.根据化学反应的实质是旧键断裂、新键形成的观点,下列变化包含化学反应的是( )
0 171764 171772 171778 171782 171788 171790 171794 171800 171802 171808 171814 171818 171820 171824 171830 171832 171838 171842 171844 171848 171850 171854 171856 171858 171859 171860 171862 171863 171864 171866 171868 171872 171874 171878 171880 171884 171890 171892 171898 171902 171904 171908 171914 171920 171922 171928 171932 171934 171940 171944 171950 171958 203614
| A. | NaCl晶体溶于水 | B. | 氯原子结合成氯分子 | ||
| C. | 臭氧转化为氧气 | D. | 干冰气化 |
 肼是重要的化工原料.某探究小组利用下列反应制取水合肼(N2H4•H2O).
肼是重要的化工原料.某探究小组利用下列反应制取水合肼(N2H4•H2O). 实验室采用MgCl2、AlCl3的混合溶液与过量氨水反应制备MgAl2O4二主要流程如下:
实验室采用MgCl2、AlCl3的混合溶液与过量氨水反应制备MgAl2O4二主要流程如下: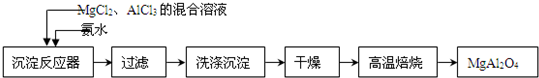
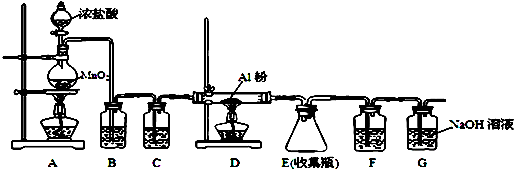
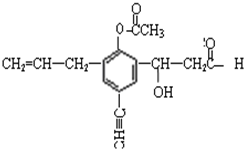 某有机物的结构如下,分析其结构并回答下列问题:
某有机物的结构如下,分析其结构并回答下列问题: