题目内容
14.根据化学反应的实质是旧键断裂、新键形成的观点,下列变化包含化学反应的是( )| A. | NaCl晶体溶于水 | B. | 氯原子结合成氯分子 | ||
| C. | 臭氧转化为氧气 | D. | 干冰气化 |
分析 既有旧化学键断裂,又有新化学键形成,说明物质间发生了化学反应,以此分析.
解答 解:A.NaCl晶体溶于水属于物理过程,只存在旧键的断裂,没有新键生成,故A错误;
B.氯原子结合成氯分子只存在新键形成,故B错误;
C.臭氧转化为氧气既有旧化学键断裂,又有新化学键形成,故C正确;
D.干冰气化是分子间距离增多,没有化学键的破坏与形成,是物理变化,故D错误.
故选C.
点评 本题考查化学键知识,题目难度不大,注意化学变化既有旧化学键断裂,又有新化学键形成.

练习册系列答案
相关题目
5.一元强酸HA溶液与一元碱MOH混合,溶液呈中性,下列判断正确的是( )
| A. | MA不可能是强酸弱碱盐 | |
| B. | 反应后溶液中c(A-)=c(M+) | |
| C. | MOH一定是强碱 | |
| D. | 混合前酸与碱中溶质的物质的量相等 |
2.在下列自然资源的开发利用中,不涉及化学变化的是( )
| A. | 通过石油分馏获得汽油 | B. | 以海带为原料制取碘单质 | ||
| C. | 利用海水制取金属镁 | D. | 用CO还原褐铁矿制备铁 |
9.高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压.高铁电池的总反应为:3Zn+2K2FeO4+8H2O$?_{充电}^{放电}$3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是( )
| A. | 放电时,溶液中的OH-向负极移动 | |
| B. | 放电时,正极附近溶液的碱性增强 | |
| C. | 放电时,每转移3 mol电子,正极有1 mol K2FeO4被氧化 | |
| D. | 充电时,阳极反应为:Fe(OH)3-3e-+5OH-═FeO42-+4H2O |
19.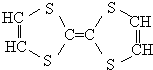 用于制造隐形飞机的物质具有吸收微波的功能,其主要成分的结构如图,关于该分子的说法正确的有( )
用于制造隐形飞机的物质具有吸收微波的功能,其主要成分的结构如图,关于该分子的说法正确的有( )
 用于制造隐形飞机的物质具有吸收微波的功能,其主要成分的结构如图,关于该分子的说法正确的有( )
用于制造隐形飞机的物质具有吸收微波的功能,其主要成分的结构如图,关于该分子的说法正确的有( )| A. | 分子中含有碳碳双键,属于烯烃 | |
| B. | 从碳骨架形状分析,应该属于环状烃 | |
| C. | 该分子属于高分子化合物 | |
| D. | 该分子中即有极性键,也有非极性键 |
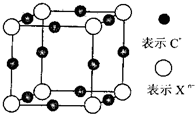 前四周期元素A、B、C、D、E、F,原子序数依次增大,其中A和B同周期,固态的AB2能升华;C和E原子都有一个未成对电子,C+比E-少一个电子层,E原子得到一个电子后3p轨道全充满;D最高价氧化物中D的质量分数为40%,且核内质子数等于中子数;F为红色单质,有F+和F2+两种离子.回答下列问题:
前四周期元素A、B、C、D、E、F,原子序数依次增大,其中A和B同周期,固态的AB2能升华;C和E原子都有一个未成对电子,C+比E-少一个电子层,E原子得到一个电子后3p轨道全充满;D最高价氧化物中D的质量分数为40%,且核内质子数等于中子数;F为红色单质,有F+和F2+两种离子.回答下列问题: