��Ŀ����
17��ijԭ����У��������ҺΪϡH2SO4���ֱ���ͨ��CO����CH4����H2S����������ͨ��O2����Cl2��������������⣺��1�����ֱ�ͨ��CO��O2ʱ��
��������Ӧ��O2+4e-+4H+=2H2O���ڸ�����Ӧ��2CO-4e-+2H2O=2CO2��+4H+���۵���ܷ�Ӧ��O2+2CO=2CO2���ܵ������ҺPH�ı仯���䣨��������١����䡱����ͬ����
��2�����ֱ�ͨ��CH4��O2ʱ��
��������Ӧ��O2+4e-+4H+=2H2O���ڸ�����Ӧ��CH4-8e-+2H2O=CO2+8H+���۵���ܷ�Ӧ��CH4+2O2=CO2+2H2O���ܵ������ҺPH�ı仯����
���� ��1��ԭ����У��������ҺΪϡH2SO4���ֱ���ͨ��CO��������ͨ��Ԫ����������CO�ڸ���ʧȥ���ӷ���������Ӧ���ɶ�����̼���壬�����������õ������������ӽ������ˮ�����ݵ缫��Ӧʽ���ܷ�Ӧ���жϣ�
��2������ȼ�ϵ����������Һ�У����ɶ�����̼��ˮ���ܷ�ӦΪ��CH4+2O2=CO2+2H2O���������������õ��ӵĻ�ԭ��Ӧ�����ø����缫����ʽ=�ܷ�Ӧ����ʽ-�����缫��Ӧʽ������ã�
��� �⣺��1��ԭ����У��������ҺΪϡH2SO4���ֱ���ͨ��CO��������ͨ����������CO�ڸ���ʧȥ���ӷ���������Ӧ���ɶ�����̼���壬�����������õ������������ӽ������ˮ����������ӦʽΪ��O2+4e-+4H+=2H2O��������ӦΪ��2CO-4e-+2H2O=2CO2��+4H+���ܷ�ӦʽΪ��O2+2CO=2CO2������Һ��pH���䣬�ʴ�Ϊ��O2+4e-+4H+=2H2O��2CO-4e-+2H2O=2CO2��+4H+��O2+2CO=2CO2�����䣻
��2������ȼ�ϵ����������Һ�У����ɶ�����̼��ˮ���ܷ�ӦΪ��CH4+2O2=CO2+2H2O�������缫��ӦʽΪ��O2+4e-+4H+=2H2O�����ܷ�Ӧ����ʽ-�����缫��Ӧʽ�ɵã�ͨ������һ���缫��ӦʽΪ��CH4-8e-+2H2O=CO2+8H+���õ�ط�Ӧ������ˮ����������Ũ�ȼ�С������pH����
�ʴ�Ϊ��O2+4e-+4H+=2H2O��CH4-8e-+2H2O=CO2+8H+��CH4+2O2=CO2+2H2O������
���� ���⿼���˵缫��Ӧʽ��д��ע���ܷ�Ӧ����ʽ=�����缫��Ӧʽ+�����缫��Ӧʽ����Ŀ�ѶȲ���

| A�� | ������������M��N | B�� | ԭ��������M��N | ||
| C�� | ���Ӳ�����M=N | D�� | �뾶��M��N��M2+��N2- |
| A�� | Al��OH��3����������� | B�� | NH3•H2O����� | ||
| C�� | HClO ��ǿ�ᣩ | D�� | CuSO4•5H2O������ |
| A�� | Al2O3 | B�� | NH4+ | C�� | Fe3+ | D�� | CO2 |
| A | B | ||
| C | D | E |
��2��B����̬�⻯����������������Ӧˮ������γ��Σ�������Һ�����ԣ�����ԡ��������ԡ����ԡ��������ӷ���ʽ��ʾ��ԭ��NH4++H2O?NH3��H2O+H+��
��3��д��CԪ��ԭ�ӵļ۵����Ų�ʽ��3s23p1�Ƚ�B��EԪ�ػ�̬ԭ�ӵĵ�һ�����ܴ�СN��S����Ԫ�ط�����գ���
��4��A����Ԫ���γ��������H����Ϊȼ�ϵ�ص�ԭ�ϣ�д����ȼ�ϵ�أ�������NaOH��Һ��Ϊ�������Һ�������缫��ӦCH4+10 OH--8e-=CO32-+7H2O��֪25��/101kPa�£�H��ȼ����Ϊ890kJ•mol-1��д��Hȼ���ȵĻ�ѧ����ʽ��CH4��g��+2O2��g��=CO2��g��+2H2O��l����H=-890kJ•mol-1��
��5����150ml��0.10•L-1���Ȼ�����Һ�м���40mLNaOH��Ҵ����ַ�Ӧ��õ�0.78g��������ԭNaOH��Һ�����ʵ���Ũ�ȿ�����0.75��1.5mol•L-1��
 ��������������ͷ�չ�����ʻ��������Ͽ�ѧ�ķ�չ�벻����ѧ��
��������������ͷ�չ�����ʻ��������Ͽ�ѧ�ķ�չ�벻����ѧ��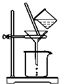 ʵ���Ҳ���MgCl2��AlCl3�Ļ����Һ�������ˮ��Ӧ�Ʊ�MgAl2O4����Ҫ�������£�
ʵ���Ҳ���MgCl2��AlCl3�Ļ����Һ�������ˮ��Ӧ�Ʊ�MgAl2O4����Ҫ�������£�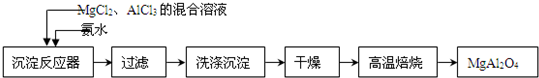
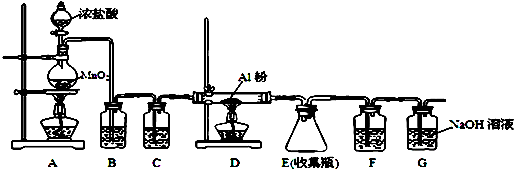
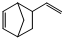 ��X��C5H6����Y��Diels-Aldeer��Ӧ�Ƶã�Diels-Aldeer��ӦΪ����˫ϩ�뺬��ϩ����Ȳ���Ļ����������������Ԫ��״������ķ�Ӧ����ķ�Ӧ��
��X��C5H6����Y��Diels-Aldeer��Ӧ�Ƶã�Diels-Aldeer��ӦΪ����˫ϩ�뺬��ϩ����Ȳ���Ļ����������������Ԫ��״������ķ�Ӧ����ķ�Ӧ��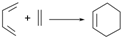
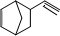 ��
��