8.常温下,在10mL 0.2mol/L氨水中,滴入0.2mol/L的稀盐酸,使溶液的pH=7.则下列说法正确的是( )
| A. | 加入盐酸的体积大于10 mL | B. | c(NH4+)=c(Cl-) | ||
| C. | 加入盐酸的体积等于10 mL | D. | c(NH4+)<c(Cl-) |
7.在恒温、恒容的密闭容器中反应.若反应物的浓度由2mol/L降到0.8mol/L需20s,那么反应物浓度由2mol/L降到1.4mol/L所需的时间( )
| A. | 10s | B. | 大于10s | C. | 小于10s | D. | 无法判断 |
5.下列方程式书写正确的是( )
| A. | NaHCO3═Na++H++CO32- | B. | Na2HPO4?2Na++HPO42- | ||
| C. | NH4++2H2O?NH3•H2O+H3O+ | D. | C(s)+O2(g)═CO2(g)△H=+393.5 kJ•mol-1 |
3.根据电离平衡原理,设计实验证明NH3•H2O是弱碱.
可选用的试剂:酚酞、石蕊、稀氨水、醋酸铵晶体和蒸馏水.
可选用的试剂:酚酞、石蕊、稀氨水、醋酸铵晶体和蒸馏水.
| 实验操作 | 实验现象 |
| ①取少量氨水于试管中,滴加酚酞试液 ②向试管中加入少量醋酸铵晶体,振荡 | 溶液呈红色 红色变浅 |
| 结论:氨水中存在电离平衡,证明氨水是弱碱 | |
2.下列电离方程式中,正确的是( )
| A. | BaSO4?Ba2++SO42- | B. | 2H2O?H3O++OH- | ||
| C. | NaHCO3═Na++H++CO32- | D. | NH3•H2O═NH4++OH- |
20.维生素C不具有的性质是( )
0 171337 171345 171351 171355 171361 171363 171367 171373 171375 171381 171387 171391 171393 171397 171403 171405 171411 171415 171417 171421 171423 171427 171429 171431 171432 171433 171435 171436 171437 171439 171441 171445 171447 171451 171453 171457 171463 171465 171471 171475 171477 171481 171487 171493 171495 171501 171505 171507 171513 171517 171523 171531 203614
| A. | 难溶于水 | B. | 易溶于水 | C. | 强还原性 | D. | 酸性 |
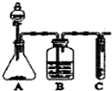 Ⅰ.实验室常用如图中的装置制备乙炔并检验乙炔的性质
Ⅰ.实验室常用如图中的装置制备乙炔并检验乙炔的性质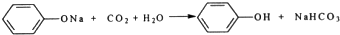

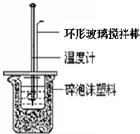 “中和热的测定”实验步骤为:
“中和热的测定”实验步骤为: