题目内容
2.下列电离方程式中,正确的是( )| A. | BaSO4?Ba2++SO42- | B. | 2H2O?H3O++OH- | ||
| C. | NaHCO3═Na++H++CO32- | D. | NH3•H2O═NH4++OH- |
分析 用化学式和离子符号表示电离过程的式子,称为电离方程式.方程式左边写化学式,右边写离子,所有阳离子带的正电荷总数与所有阴离子所带的负电荷总数相等,离子团不能拆开,强电解质用“=”连接,弱电解质用“?”连接.
解答 解:A.硫酸钡为强电解质,熔融完全电离出钡离子和硫酸根离子,用“=”连接,电离方程式为BaSO4?Ba2++SO42-,故A错误;
B.在水中:水电离出H+、OH-,H+和H2O结合成H3O+,水部分电离,部分电离用“?”连接,电离方程式为:2H2O?H3O++OH-,故B正确;
C.NaHCO3为强电解质,碳酸氢根离子为弱酸的酸酸式盐的酸根根离子,不能拆写,电离方程式为NaHCO3=Na++HCO3-,故C错误;
D.NH3•H2O为一元弱碱,部分电离,部分电离用“?”连接,电离方程式为:NH3•H2O?NH4++OH-,故D错误;
故选B.
点评 本题考查了电离方程式的书写判断,掌握正确书写电离方程式的方法,并会正确判断电离方程式的正误是解题的关键,题目难度不大.

练习册系列答案
 学业测评一课一测系列答案
学业测评一课一测系列答案
相关题目
10.石墨和金刚石都是碳的单质,石墨在一定条件下可转化为金刚石.已知把石墨完全转化为金刚石时,要吸收能量,下列说法正确的是( )
| A. | 石墨不如金刚石稳定 | |
| B. | 金刚石与石墨一样稳定 | |
| C. | 等质量的金刚石与石墨完全燃烧,放出的能量一样多 | |
| D. | 等质量的金刚石与石墨完全燃烧,石墨放出的能量少 |
17.抗酸药中既能与强酸反应,又能与强碱反应的物质是( )
| A. | CaCO3 | B. | Al(OH)3 | C. | Mg(OH)2 | D. | MgCO3 |
7.在恒温、恒容的密闭容器中反应.若反应物的浓度由2mol/L降到0.8mol/L需20s,那么反应物浓度由2mol/L降到1.4mol/L所需的时间( )
| A. | 10s | B. | 大于10s | C. | 小于10s | D. | 无法判断 |
11.下列说法正确的是( )
| A. | 强酸跟强碱反应放出的热量一定是中和热 | |
| B. | 1 mol酸与1 mol碱完全反应放出的热量是中和热 | |
| C. | 在稀溶液中,强酸与强碱发生中和反应生成1 mol H2O(l)时的反应热叫做中和热 | |
| D. | 表示中和热的离子方程式为H++OH-═H2O△H=-57.3 kJ/mol |
12.下列反应中,属于氧化还原反应的是( )
| A. | Fe+CuSO4═FeSO4+Cu | B. | Na2CO3+CaCl2═CaCO3↓+2NaCl | ||
| C. | 2H2O $\frac{\underline{\;电解\;}}{\;}$2H2↑+O2↑ | D. | MgSO4+2NaOH═Mg(OH)2↓+Na2SO4 |
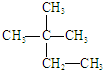 ③氧气 ④氯气 ⑤
③氧气 ④氯气 ⑤ ⑥${\;}_{17}^{37}$Cl ⑦${\;}_{17}^{35}$Cl ⑧臭氧.
⑥${\;}_{17}^{37}$Cl ⑦${\;}_{17}^{35}$Cl ⑧臭氧.