6.设阿伏加德罗常数为NA.则下列说法正确的是( )
| A. | 100 g 98%的浓硫酸中含氧原予总数为4NA | |
| B. | 常温常压下,18g重水(D2O)中所含的电子数为10 NA | |
| C. | 常温常压下,4.6 g NO2气体含有0.3 NA个原子 | |
| D. | 常温下,2.7g、铝片投入足量的浓硫酸中,产生的SO2,分子数为0.3NA |
5.写出下列反应的热化学方程式:
(1)由氢气和氧气反应生成1mol水蒸气放热241.8kJ,写出该反应的热化学方程式H2(g)+$\frac{1}{2}$O2(g)=H2O(g)△H=-241.8kJ/mol.若1g水蒸气转化成液态水放热2.444kJ,则反应2H2(g)+O2(g)═2H2O(l)的△H=-571.6kJ/mol,氢气的燃烧热为285.8kJ/mol.
(2)由气态基态原子形成1mol化学键释放的最低能量叫键能.从化学键的角度分析,化学反应的过程就是反应物的化学键的破坏和生成物的化学键的形成过程.在化学反应过程中,破坏旧化学键需要吸收能量,形成新化学键又会释放能量.
已知反应N2(g)+3H2(g)$?_{催化剂}^{高温、高压}$2NH3(g)△H=a kJ•mol-1.试根据表中所列键能数据计算a的数值(列出简单的计算式):a=945+3×436-6×391=-93.
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算.
已知:C(s,石墨)+O2(g)═CO2(g)△H1=-393.5kJ•mol-1
2H2(g)+O2(g)═2H2O(l)△H2=-571.6kJ•mol-1
2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H3=-2 599kJ•mol-1
根据盖斯定律,计算298K时由C(s,石墨)和H2(g)生成1mol C2H2(g)反应的焓变(列出简单的计算式):△H=2△H1+$\frac{1}{2}$△H2-$\frac{1}{2}$△H3=+226.7kJ•mol-1.
(1)由氢气和氧气反应生成1mol水蒸气放热241.8kJ,写出该反应的热化学方程式H2(g)+$\frac{1}{2}$O2(g)=H2O(g)△H=-241.8kJ/mol.若1g水蒸气转化成液态水放热2.444kJ,则反应2H2(g)+O2(g)═2H2O(l)的△H=-571.6kJ/mol,氢气的燃烧热为285.8kJ/mol.
(2)由气态基态原子形成1mol化学键释放的最低能量叫键能.从化学键的角度分析,化学反应的过程就是反应物的化学键的破坏和生成物的化学键的形成过程.在化学反应过程中,破坏旧化学键需要吸收能量,形成新化学键又会释放能量.
| 化学键 | H-H | N-H | N≡N |
| 键能/kJ•mol-1 | 436 | 391 | 945 |
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算.
已知:C(s,石墨)+O2(g)═CO2(g)△H1=-393.5kJ•mol-1
2H2(g)+O2(g)═2H2O(l)△H2=-571.6kJ•mol-1
2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H3=-2 599kJ•mol-1
根据盖斯定律,计算298K时由C(s,石墨)和H2(g)生成1mol C2H2(g)反应的焓变(列出简单的计算式):△H=2△H1+$\frac{1}{2}$△H2-$\frac{1}{2}$△H3=+226.7kJ•mol-1.
4.在恒容密闭容器中A(g)+3B(g)?2C(g)△H<0,达平衡后,将气体混合物的温度降低,下列叙述中不正确的是( )
| A. | 容器中混合气体的平均相对分子质量增大 | |
| B. | 正反应速率增大,逆反应速率减小,平衡向正反应方向移动 | |
| C. | 正反应速率和逆反应速率都变小,C的百分含量增加 | |
| D. | 混合气体密度的变化情况不可以作为判断反应是否再次达平衡的依据 |
3.下列说法不正确的是( )
0 171266 171274 171280 171284 171290 171292 171296 171302 171304 171310 171316 171320 171322 171326 171332 171334 171340 171344 171346 171350 171352 171356 171358 171360 171361 171362 171364 171365 171366 171368 171370 171374 171376 171380 171382 171386 171392 171394 171400 171404 171406 171410 171416 171422 171424 171430 171434 171436 171442 171446 171452 171460 203614
| A. | 如图所示正反应的活化能为E-E 1 | |
| B. | 活化分子具有比普通分子更高的能量 | |
| C. | 反应物的分子的每次碰撞都能发生化学反应 | |
| D. | 反应物分子间的有效碰撞是发生化学反应的充要条件 |
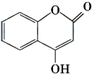 可用来制备抗凝血药,通过如图路线合成:
可用来制备抗凝血药,通过如图路线合成: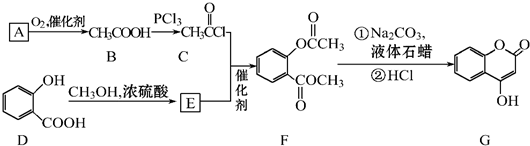
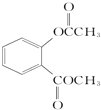 +3NaOH$\stackrel{△}{→}$
+3NaOH$\stackrel{△}{→}$ +CH3COONa+CH3OH+H2O.
+CH3COONa+CH3OH+H2O. 已知氮化铝的晶胞结构如图所示.请回答下列问题:
已知氮化铝的晶胞结构如图所示.请回答下列问题: CO(g)+3H2(g) ΔH>0。将1.0 mol CH4和2.0 mol H2O通入反应容器(假设容积为10L),10 min末有0.10 mol CO生成,则10 min内该反应的速率v(H2)= 。②已知甲烷燃料电池的工作原理如右图所示。该电池中甲烷从 进(填“a”、“b”、“c”、“d”),电极Ⅰ是 极,写出该电池负极的电极反应: 。
CO(g)+3H2(g) ΔH>0。将1.0 mol CH4和2.0 mol H2O通入反应容器(假设容积为10L),10 min末有0.10 mol CO生成,则10 min内该反应的速率v(H2)= 。②已知甲烷燃料电池的工作原理如右图所示。该电池中甲烷从 进(填“a”、“b”、“c”、“d”),电极Ⅰ是 极,写出该电池负极的电极反应: 。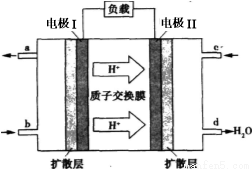
 =-483.6kJ/mol
=-483.6kJ/mol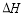 =+67.7kJ/mol
=+67.7kJ/mol
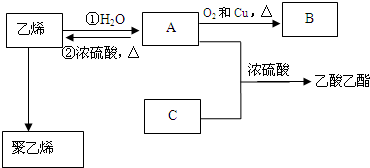
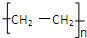 ,化合物C所含官能团的名称为羧基.
,化合物C所含官能团的名称为羧基.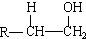 $→_{△}^{浓硫酸}$R-CH=CH2+H2O,写出反应②的反应方程式(标明反应条件):CH3CH2OH$→_{△}^{浓H_{2}SO_{4}}$H2O+CH2=CH2↑.
$→_{△}^{浓硫酸}$R-CH=CH2+H2O,写出反应②的反应方程式(标明反应条件):CH3CH2OH$→_{△}^{浓H_{2}SO_{4}}$H2O+CH2=CH2↑.