8. 反应2NO2(g)?N2O4(g)△H=-57kJ•mol-1,在条件下温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是( )
反应2NO2(g)?N2O4(g)△H=-57kJ•mol-1,在条件下温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是( )
 反应2NO2(g)?N2O4(g)△H=-57kJ•mol-1,在条件下温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是( )
反应2NO2(g)?N2O4(g)△H=-57kJ•mol-1,在条件下温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是( )| A. | 由状态B到状态A,可以用加热的方法 | |
| B. | A、C两点气体的颜色:A深,C浅 | |
| C. | A、C两点的反应速率:A>C | |
| D. | A、C两点气体的平均相对分子质量:A>C |
7.下列有关热化学方程式的叙述中,正确的是( )
| A. | 含20.0 g NaOH的稀溶液与稀盐酸完全中和,放出28.7 kJ的热量,该反应的热化学方程式是 NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=+57.4 kJ•mol-1 | |
| B. | 已知C(石墨,s)=C(金刚石,s)△H>0,则金刚石一定比石墨稳定 | |
| C. | 已知2H2O(g)═2H2(g)+O2(g)△H=+483.6 kJ•mol-1,则提供483.6 kJ热量时,一定会使2 mol H2O (g)发生分解 | |
| D. | 已知C(s)+O2(g)=CO2(g)△H=a kJ•mol-1,2C(s)+O2(g)═2CO(g),△H=b kJ•mol-1,则2CO(g)+O2(g)═2CO2(g)△H=(2a-b) kJ•mol-1 |
4.在一密闭容器中,反应aA(g)?bB(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的60%,则( )
| A. | 平衡向逆反应方向移动了 | B. | 物质A的转化率减少了 | ||
| C. | a>b | D. | 以上说法都不正确 |
1.下列不能表明醋酸是弱电解质的是( )
| A. | 0.1mol/L的醋酸水溶液中,c(H+)约为10-3mol/L | |
| B. | 常温下同浓度醋酸水溶液的导电性比盐酸弱 | |
| C. | 醋酸水溶液能使紫色石蕊试液变红 | |
| D. | 醋酸稀溶液中同时存在CH3COOH和CH3COO- |
20.下列关于强弱电解质的说法,错误的是( )
| A. | 强电解质在溶液中完全电离,不存在电离平衡 | |
| B. | 纯净的强电解质在液态时,有的导电,有的不导电 | |
| C. | 同一弱电解质的溶液,当温度、浓度不同时,其导电能力也不同 | |
| D. | 在溶液中,导电能力强的电解质为强电解质,导电能力弱的电解质是弱电解质 |
19.下列不能用勒沙特列原理解释的是( )
0 170720 170728 170734 170738 170744 170746 170750 170756 170758 170764 170770 170774 170776 170780 170786 170788 170794 170798 170800 170804 170806 170810 170812 170814 170815 170816 170818 170819 170820 170822 170824 170828 170830 170834 170836 170840 170846 170848 170854 170858 170860 170864 170870 170876 170878 170884 170888 170890 170896 170900 170906 170914 203614
| A. | 高压条件有利于合成氨反应 | |
| B. | 棕红色NO2加压后颜色先变深后变浅 | |
| C. | SO2催化氧化成SO3的反应,往往需要使用催化剂 | |
| D. | 增加氧气的量有利于SO2催化氧化成SO3 |
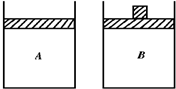 有两只相同的密闭容器A和B,A保持恒容,B保持恒压.起始时向这两只容器中分别充入等量的、物质的量比为4:5的NH3与O2的混合气体,并使A和B容积相等(如图所示),在保持500℃的条件下使之发生4NH3(g)+5O2(g)?4NO(g)+6H2O反应.填写下列空格:
有两只相同的密闭容器A和B,A保持恒容,B保持恒压.起始时向这两只容器中分别充入等量的、物质的量比为4:5的NH3与O2的混合气体,并使A和B容积相等(如图所示),在保持500℃的条件下使之发生4NH3(g)+5O2(g)?4NO(g)+6H2O反应.填写下列空格:
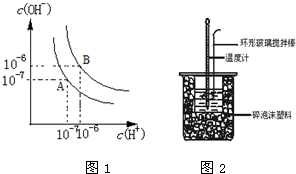 溶液的酸碱性对生产生活都有重要的影响.
溶液的酸碱性对生产生活都有重要的影响.