1.在实验室里可用右图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质.
图甲中:①为氯气发生装置;②的试管里盛有15mL 30% KOH溶液,并置于热水浴中;③的试管里盛有15mL 8% NaOH溶液,并置于冰水浴中;④的试管里加有紫色石蕊试液;⑤为尾气吸收装置.
请填写下列空白:
(1)制取氯气时,在烧瓶里加入一定量的二氧化锰,通过分液漏斗(填写仪器名称)向烧瓶中加入适量的浓盐酸.实验室制Cl2的化学方程式MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;实验时为了除去氯气中的HCl气体,可在①与②之间安装盛有C(填写下列编号字母)的净化装置.
A.碱石灰 B.氢氧化钠溶液 C.饱和食盐水 D.浓硫酸
(2)如果将过量二氧化锰与20mL 12mol•L-1的浓盐酸混合加热,充分反应后生成的氯气明显少于0.06mol.其主要原因有:①浓盐酸挥发变稀,②反应一段时间后,浓盐酸消耗变稀,无法被二氧化锰氧化.
(3)比较制取氯酸钾和次氯酸钠的条件,二者的差异是
①制取温度不同,制取氯酸钾需要较高温度,制取次氯酸钠需要较低温度;
②制取时,碱的浓度也不同,制取氯酸钾需要浓度较大的碱,制取次氯酸钠需要浓度较小的碱.
反应完毕经冷却后,②的试管中有大量晶体析出.图乙中符合该晶体溶解度曲线的是M(填写编号字母);
从②的试管中分离出该晶体的方法是过滤(填写实验操作名称).
(4)实验中可观察到④的试管里溶液的颜色发生了如下变化,请填写下表中的空白.

图甲中:①为氯气发生装置;②的试管里盛有15mL 30% KOH溶液,并置于热水浴中;③的试管里盛有15mL 8% NaOH溶液,并置于冰水浴中;④的试管里加有紫色石蕊试液;⑤为尾气吸收装置.
请填写下列空白:
(1)制取氯气时,在烧瓶里加入一定量的二氧化锰,通过分液漏斗(填写仪器名称)向烧瓶中加入适量的浓盐酸.实验室制Cl2的化学方程式MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;实验时为了除去氯气中的HCl气体,可在①与②之间安装盛有C(填写下列编号字母)的净化装置.
A.碱石灰 B.氢氧化钠溶液 C.饱和食盐水 D.浓硫酸
(2)如果将过量二氧化锰与20mL 12mol•L-1的浓盐酸混合加热,充分反应后生成的氯气明显少于0.06mol.其主要原因有:①浓盐酸挥发变稀,②反应一段时间后,浓盐酸消耗变稀,无法被二氧化锰氧化.
(3)比较制取氯酸钾和次氯酸钠的条件,二者的差异是
①制取温度不同,制取氯酸钾需要较高温度,制取次氯酸钠需要较低温度;
②制取时,碱的浓度也不同,制取氯酸钾需要浓度较大的碱,制取次氯酸钠需要浓度较小的碱.
反应完毕经冷却后,②的试管中有大量晶体析出.图乙中符合该晶体溶解度曲线的是M(填写编号字母);
从②的试管中分离出该晶体的方法是过滤(填写实验操作名称).
(4)实验中可观察到④的试管里溶液的颜色发生了如下变化,请填写下表中的空白.
| 实验现象 | 原因 |
| 溶液最初从紫色逐渐变为红色 | 氯气与水反应生成的H+使石蕊变色 |
| 随后溶液逐渐变为无色 | 氯气与水反应生成次氯酸具有漂白性 |
| 然后溶液从无色逐渐变为浅黄绿色 | 过量氯气溶解于水中 |
10.下列叙述正确的是( )
| A. | 由甲烷分子呈正四面体形结构可推知一氯甲烷分子也呈正四面体形结构 | |
| B. | 在甲烷的四种氯的取代物中,只有四氯甲烷是非极性分子 | |
| C. | 由甲烷(CH4)的氯代物有4种,可推知乙烷(结构式为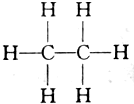 )的氯代物有6种 )的氯代物有6种 | |
| D. | 由于CH4是易燃易爆的气体,所以点燃CH4前一定要检验其纯度 |
6.1mol下列气体中所含原子数最多的是( )
| A. | H2 | B. | CO2 | C. | CH4 | D. | O2 |
4.用NA表示表示阿伏伽德罗常数的值,下列说法中正确的是( )
0 170618 170626 170632 170636 170642 170644 170648 170654 170656 170662 170668 170672 170674 170678 170684 170686 170692 170696 170698 170702 170704 170708 170710 170712 170713 170714 170716 170717 170718 170720 170722 170726 170728 170732 170734 170738 170744 170746 170752 170756 170758 170762 170768 170774 170776 170782 170786 170788 170794 170798 170804 170812 203614
| A. | 常温常压下,0.05NA个CO2分子所占的体积是1.12L | |
| B. | 1mol 氧气所含有的原子数为NA | |
| C. | 常温常压下,32g O2和34g H2S气体分子个数比为1:1 | |
| D. | 11.2L NH3中所含的质子数为5NA |
 实验室制取少量溴乙烷的装置如图所示.根据题意完成下列填空:
实验室制取少量溴乙烷的装置如图所示.根据题意完成下列填空: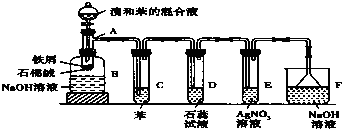

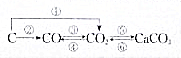 用化学方程式表示在一定条件下下列物质间的转化关系.指出哪些是氧化还原反应,哪些是非氧化还原反应.对于氧化还原反应,指出氧化剂和还原剂.
用化学方程式表示在一定条件下下列物质间的转化关系.指出哪些是氧化还原反应,哪些是非氧化还原反应.对于氧化还原反应,指出氧化剂和还原剂.