3.卤族元素随核电荷数的增加,下列叙述正确的是( )
| A. | 单质的颜色逐渐加深 | B. | 气态氢化物的稳定性逐渐增强 | ||
| C. | 单质的熔点逐渐升高 | D. | 单质的氧化性逐渐增强 |
2.现有六种元素,其中A、B、C、D为短周期主族元素,E、F为第四周期元素,它们的原子序数依次增大.请根据下列相关信息,回答问题.
(1)A基态原子中能量最高的电子,其电子云在空间有3个方向,原子轨道呈纺锤形.
(2)某同学根据上述信息,所画的B电子排布图如图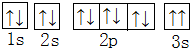 ,违背了泡利原理.
,违背了泡利原理.
(3)F位于周期表中第四周期、ⅦB族、d区,其基态原子有25种运动状态.
(4)CD3中心原子的杂化方式为sp3,用价层电子对互斥理论推测其分子空间构型为三角锥形,检验E元素的方法是焰色反应.
| A元素原子的核外p电子总数比s电子总数少1 |
| B元素原子核外s电子总数与p电子总数相等,且不与A元素在同一周期 |
| C原子核外所有p轨道全满或半满 |
| D元素的主族序数与周期数的差为4 |
| E是前四周期中电负性最小的元素 |
| F在周期表的第七列 |
(2)某同学根据上述信息,所画的B电子排布图如图
 ,违背了泡利原理.
,违背了泡利原理.(3)F位于周期表中第四周期、ⅦB族、d区,其基态原子有25种运动状态.
(4)CD3中心原子的杂化方式为sp3,用价层电子对互斥理论推测其分子空间构型为三角锥形,检验E元素的方法是焰色反应.
1.关于下列物质的结构或性质分析正确的是( )
| A. | CH2O和CO2分子中的中心原子均采用sp2杂化 | |
| B. | CH3SH 的相对分子质量比CH3OH大,因此前者的沸点高 | |
| C. | C6H6分子中含有6个σ键和1个大π键,C6H6是非极性分子 | |
| D. | 甲胺(分子式CH3NH2)的沸点比三甲胺[分子式(CH3)3N]的沸点高 |
20.下表为元素周期表的一部分,回答下列有关问题:
(1)在这些元素中:非金属性最强的元素是③,原子半径最大的是⑨(填数字序号)
(2)这些元素的最高价氧化物对应水化物中酸性最强的是HClO4,碱性最强的是KOH(填化学式)
(3)气态氢化物能与其最高价氧化物对应的水化物反应生成盐的化学方程式为:NH3+HNO3=NH4NO3.
(4)呈两性的氢氧化物分别与④和⑥的最高价氧化物对应的水化物反应的离子方程式为Al(OH)3+OH-=AlO2-+2H2O,Al(OH)3+3H+=Al3++3H2O.
| 周期 族 | IA | 0 | ||||||
| 1 | ① | IIA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ||||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ | ||||||
(2)这些元素的最高价氧化物对应水化物中酸性最强的是HClO4,碱性最强的是KOH(填化学式)
(3)气态氢化物能与其最高价氧化物对应的水化物反应生成盐的化学方程式为:NH3+HNO3=NH4NO3.
(4)呈两性的氢氧化物分别与④和⑥的最高价氧化物对应的水化物反应的离子方程式为Al(OH)3+OH-=AlO2-+2H2O,Al(OH)3+3H+=Al3++3H2O.
19.下列原子构成的单质中既能与稀硫酸反应又能与烧碱溶液反应,都产生H2的是( )
| A. | 核内无中子的原子 | |
| B. | 价电子构型为3s23p1 | |
| C. | 最外层电子数等于倒数第三层上的电子数的原子 | |
| D. | N层上无电子,最外层上的电子数等于电子层数的原子 |
18.铜板上铁铆钉处的吸氧腐蚀原理如图所示,下列说法正确的是( )
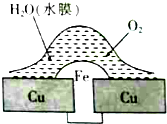

| A. | 此过程中铜被腐蚀 | |
| B. | 此过程中电子从Cu移向Fe | |
| C. | 铁铆钉表面发生的电极反应为Fe-3e-═Fe3+ | |
| D. | 在金属表面刷上一层油漆,能延缓铁铆钉的腐蚀 |
17.用CuSO4溶液电解精炼粗铜(含有Fe、Zn、Ag、Pt等杂质),下列叙述正确的是( )
| A. | 纯铜作阳极 | |
| B. | 阴极发生氧化反应 | |
| C. | 电解后后c(Cu2+)保持不变 | |
| D. | 电解槽底部会生成含有Ag、Pt的阳极泥 |
16.将一定量的有机物A溶于烧碱溶液中,滴入酚酞试液呈红色,煮沸5分钟后,溶液红色变浅,再向其中加入盐酸,显酸性,并析出白色晶体;取少量上述晶体放到FeCl3溶液中,溶液呈紫色.则有机物A可能是( )
| A. |  | B. |  | C. | 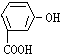 | D. |  |
15.Ⅰ.碱性锌锰干电池是最常见的化学电源之一,已知其电池总反应:
Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2,则负极发生反应的物质为Zn+2OHˉ-2eˉ=Zn(OH)2;发生在正极的电极反应为MnO2+H2O+e-=MnO(OH)+OH-.
Ⅱ.回收的废旧锌锰干电池经过处理后得到锰粉(含MnO2、MnOOH、Fe和炭黑等),由锰粉制取MnO2的步骤如图所示:
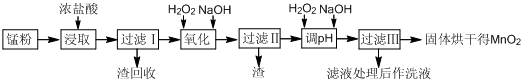
根据如图所示步骤并参考表格数据回答问题:
(1)在加热条件下用浓盐酸浸取锰粉,所得溶液中含有Mn2+、Fe2+等.加热的作用是加快反应速率.
(2)锰粉经浓盐酸浸取,过滤I除去不溶杂质后,向滤液中加入适量H2O2溶液,其作用是将Fe2+转化为Fe3+.
(3)将过滤I所得滤液经H2O2氧化后,再加入NaOH溶液调节pH的范围是:3.7<pH<8.3,其目的是使Fe3+完全沉淀,并防止Mn2+转化为Mn(OH)2沉淀.
(4)过滤Ⅱ所得滤液加入足量H2O2溶液并加入NaOH溶液调节pH约为9,使Mn2+氧化得到MnO2,反应的离子方程式为Mn2++H2O2+2OH-=MnO2↓+2H2O.
(5)实验室进行过滤操作时,需要用到的玻璃仪器有漏斗、烧杯、玻璃棒.
Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2,则负极发生反应的物质为Zn+2OHˉ-2eˉ=Zn(OH)2;发生在正极的电极反应为MnO2+H2O+e-=MnO(OH)+OH-.
Ⅱ.回收的废旧锌锰干电池经过处理后得到锰粉(含MnO2、MnOOH、Fe和炭黑等),由锰粉制取MnO2的步骤如图所示:

| 开始沉淀 | 沉淀完全 | |
| Fe(OH)3 | 2.7 | 3.7 |
| Fe(OH)2 | 7.6 | 9.6 |
| Mn(OH)2 | 8.3 | 9.8 |
(1)在加热条件下用浓盐酸浸取锰粉,所得溶液中含有Mn2+、Fe2+等.加热的作用是加快反应速率.
(2)锰粉经浓盐酸浸取,过滤I除去不溶杂质后,向滤液中加入适量H2O2溶液,其作用是将Fe2+转化为Fe3+.
(3)将过滤I所得滤液经H2O2氧化后,再加入NaOH溶液调节pH的范围是:3.7<pH<8.3,其目的是使Fe3+完全沉淀,并防止Mn2+转化为Mn(OH)2沉淀.
(4)过滤Ⅱ所得滤液加入足量H2O2溶液并加入NaOH溶液调节pH约为9,使Mn2+氧化得到MnO2,反应的离子方程式为Mn2++H2O2+2OH-=MnO2↓+2H2O.
(5)实验室进行过滤操作时,需要用到的玻璃仪器有漏斗、烧杯、玻璃棒.
14.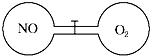 一定温度下,两个体积相等的连通容器用活塞分开,左右两室各充入一定量NO和O2,恰好使两容器内气体密度相同,打开活塞,充分混合反应.下列判断正确的是(不考虑NO2转化为N2O4)( )
一定温度下,两个体积相等的连通容器用活塞分开,左右两室各充入一定量NO和O2,恰好使两容器内气体密度相同,打开活塞,充分混合反应.下列判断正确的是(不考虑NO2转化为N2O4)( )
0 170589 170597 170603 170607 170613 170615 170619 170625 170627 170633 170639 170643 170645 170649 170655 170657 170663 170667 170669 170673 170675 170679 170681 170683 170684 170685 170687 170688 170689 170691 170693 170697 170699 170703 170705 170709 170715 170717 170723 170727 170729 170733 170739 170745 170747 170753 170757 170759 170765 170769 170775 170783 203614
 一定温度下,两个体积相等的连通容器用活塞分开,左右两室各充入一定量NO和O2,恰好使两容器内气体密度相同,打开活塞,充分混合反应.下列判断正确的是(不考虑NO2转化为N2O4)( )
一定温度下,两个体积相等的连通容器用活塞分开,左右两室各充入一定量NO和O2,恰好使两容器内气体密度相同,打开活塞,充分混合反应.下列判断正确的是(不考虑NO2转化为N2O4)( )| A. | 最终容器内无O2存在 | B. | 反应前、后左室气体压强不变 | ||
| C. | 反应前、后右室气体密度不变 | D. | 开始时左右两室气体分子数相同 |