3.关于原子结构的叙述中:
①所有原子核均由质子和中子构成;
②原子处于基态时,次外层电子不一定是8个;
③稀有气体元素,其基态原子最外层都是8个电子;
④最外层电子数为2的原子一定是金属原子;
其中正确的是( )
①所有原子核均由质子和中子构成;
②原子处于基态时,次外层电子不一定是8个;
③稀有气体元素,其基态原子最外层都是8个电子;
④最外层电子数为2的原子一定是金属原子;
其中正确的是( )
| A. | ①② | B. | ②③ | C. | 只有② | D. | 只有④ |
2.下列表述中正确的是( )
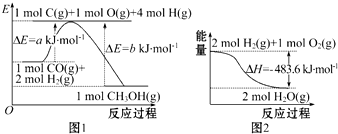

| A. | 根据图1可知合成甲醇的热化学方程式为CO(g)+2H2(g)═CH3OH(g)△H1=(b-a)kJ•mol-1 | |
| B. | 1 mol NaOH分别和1 mol CH3COOH、1 mol HNO3反应,后者比前者△H小 | |
| C. | 图2表示2 mol H2(g)所具有的能量比2 mol气态水所具有的能量多483.6 kJ | |
| D. | 汽油燃烧时将全部的化学能转化为热能 |
20.下列叙述正确的是( )
| A. | 推广使用太阳能、风能、海洋能、氢能,有利于缓解温室效应 | |
| B. | 乙醇和汽油都是可再生能源,应大力推广“乙醇汽油” | |
| C. | 废电池需回收,主要是要利用电池外壳的金属材料 | |
| D. | 升高温度可降低活化能,增大反应速率 |
18.NaNO2是一种食品添加剂,具有致癌作用.酸性KMnO4溶液与NaNO2的反应为MnO4-+NO2-+H+→Mn2++NO3-+H2O (未配平).下列叙述正确的是( )
| A. | 上述反应中NO2- 是氧化剂 | |
| B. | 反应过程中溶液的pH增大 | |
| C. | 该反应可以说明氧化性NO3->MnO4- | |
| D. | 上述反应中,1 mol KMnO4可以消耗2.5 mol NaNO2 |
17.下列各组中的两种物质作用时,反应条件或反应物的用量比改变,不会引起产物种类改变的是( )
| A. | Na与O2 | B. | NaOH与CO2 | C. | Na2O与CO2 | D. | Na2O2与H2O |
16.某非金属单质A和氧气恰好完全发生化合反应生成B,B为气体,其体积是氧气体积的两倍(同温同压).以下对B分子组成的推测一定正确的是( )
| A. | 有2个A原子 | B. | 有2个氧原子 | C. | 有1个A原子 | D. | 有1个氧原子 |
15.下列物质的制备方法正确的是( )
| A. | 用铝粉和MnO2制得锰 | |
| B. | 用电解熔融氯化铝的方法制得单质铝 | |
| C. | 氯化铝溶液和过量氢氧化钠溶液反应制备Al(OH)3 | |
| D. | 用镁粉和空气反应制备Mg3N2 |
14.下列实验现象预测或实验操作或实验原理正确的是( )

0 170217 170225 170231 170235 170241 170243 170247 170253 170255 170261 170267 170271 170273 170277 170283 170285 170291 170295 170297 170301 170303 170307 170309 170311 170312 170313 170315 170316 170317 170319 170321 170325 170327 170331 170333 170337 170343 170345 170351 170355 170357 170361 170367 170373 170375 170381 170385 170387 170393 170397 170403 170411 203614

| A. | 实验Ⅰ:左边的棉球呈橙色,右边的棉球呈蓝色,证明氧化性:Cl2>Br2>I2 | |
| B. | 实验Ⅱ:当溶液至红褐色,停止加热,让光束通过体系时可产生丁达尔现象 | |
| C. | 实验Ⅲ:可通过铜丝的上下移动来控制NO2的制取并收集NO2气体 | |
| D. | 实验Ⅳ:振荡后静置,溶液不再分层,且保持无色透明 |



