题目内容
2.下列表述中正确的是( )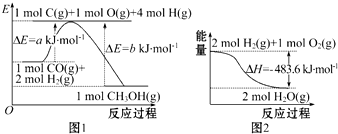
| A. | 根据图1可知合成甲醇的热化学方程式为CO(g)+2H2(g)═CH3OH(g)△H1=(b-a)kJ•mol-1 | |
| B. | 1 mol NaOH分别和1 mol CH3COOH、1 mol HNO3反应,后者比前者△H小 | |
| C. | 图2表示2 mol H2(g)所具有的能量比2 mol气态水所具有的能量多483.6 kJ | |
| D. | 汽油燃烧时将全部的化学能转化为热能 |
分析 A.该反应是放热反应,△H为负值;
B.弱酸的电离是吸热过程;
C.应为反应物的总能量大于生成物的总能量;
D.汽油燃烧时产生热和光.
解答 解:A.该反应是放热反应,△H为负值,△H1=(a-b)kJ•mol-1,故A错误;
B.弱酸的电离是吸热过程,后者比前者△H小,故B正确;
C.图2表示2 mol H2(g)和1molO2(g)所具有的能量比2 mol气态水所具有的能量多483.6 kJ,故C错误;
D.汽油燃烧时产生热和光,将化学能转化为热能和光能,故D错误.
故选B.
点评 本题考查常见的能量转化形式、吸热反应和放热反应,题目难度不大,注意汽油燃烧时产生热和光.

练习册系列答案
相关题目
12.下列除去杂质的方法正确的是( )
| A. | 除去BaSO4中的少量BaCO3加入足量盐酸,充分反应后,过滤、洗涤、干燥 | |
| B. | 除去KCl溶液中的少量MgCl2,加入适量NaOH溶液,过滤 | |
| C. | 除去CO2气体中混有的HCl气体:通过饱和碳酸氢钠溶液,洗气 | |
| D. | 除去碘水中的碘,加入乙醇萃取后分液 |
13.常温下,由水电离出的c(H+)=1×10-14 mol/L的溶液中,下列各组离子一定能大量共存的是( )
| A. | K+、Ba2+、NO3-、Cl- | B. | Ca2+、Al3+、Br-、NO3- | ||
| C. | Na+、ClO-、SO42-、HCO3- | D. | Mg2+、Cl-、NH4+、SO42- |
10.下列化合物中既含有离子键又含有极性共价键的是( )
| A. | KBr | B. | NaOH | C. | HBr | D. | Na2O2 |
17.下列各组中的两种物质作用时,反应条件或反应物的用量比改变,不会引起产物种类改变的是( )
| A. | Na与O2 | B. | NaOH与CO2 | C. | Na2O与CO2 | D. | Na2O2与H2O |
7.某能使石蕊试液变红的溶液中,能大量存在的离子是( )
| A. | Al3+ NH4+ SO42-Cl- | B. | Na+Mg2+ HCO3- NO3- | ||
| C. | K+ Na+ AlO2-Cl- | D. | Fe2+ K+NO3-Cl- |
14.下列说法中没有错误的是( )
| A. | 14C16O和12C18O两个分子所含质子数、中子数和原子个数均相等 | |
| B. | 1H2和2H2互为同位素,它们的质子数相等 | |
| C. | 14C和14N的质量数相等,它们是同素异形体 | |
| D. | NH4+和H3O+两个离子的电子数、质子数和中子数均相等 |
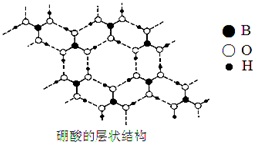 硼(B)及其化合物在化学中有重要的地位.请回答下列问题:
硼(B)及其化合物在化学中有重要的地位.请回答下列问题: