20.下列物质的水溶液呈碱性的是( )
| A. | FeCl3 | B. | KSCN | C. | CH3COOH | D. | NH4Al(SO4)2 |
19.下列金属的冶炼方法与钠相同的是( )
| A. | 铁 | B. | 铜 | C. | 银 | D. | 铝 |
18.将下列物质注入水中,振荡后静置,能分层且浮于水面上的是( )
| A. | 溴苯 | B. | 苯 | C. | 乙醇 | D. | 硝基苯 |
17.原子序数依次增大的A、B、C、D、E五种非0族元素组成了某化合物M,其中A是元素周期表中原子半径最小的元素,B元素原子最外层p能级比s能级多一个电子,C、D元素同主族且原子序数D为C的二倍,E元素的原子外围电子排布为(n-1)dn+6ns1.下列关于M的说法不正确的是( )
| A. | 若化合物M其原子个数比为14:4:5:1:1,则其化学式为[Cu(NH3)4]SO4•H2O | |
| B. | 若该化合物为配合物,则E离子给出孤对电子 | |
| C. | C元素与D元素形成的一种具有较强还原性的分子的VSEPR模型为平面三角形 | |
| D. | DC42-空间构型为正四面体 |
16.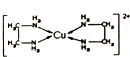 CuCl2溶液与乙二胺(H2N-CH2-CH2-NH2)可形成配离子[Cu(En)2]2+(En是乙二胺的简写),其结构如图所示.则配离子[Cu(En)2]2+的配位数和该微料含有的微料间的作用力类型均正确的是( )
CuCl2溶液与乙二胺(H2N-CH2-CH2-NH2)可形成配离子[Cu(En)2]2+(En是乙二胺的简写),其结构如图所示.则配离子[Cu(En)2]2+的配位数和该微料含有的微料间的作用力类型均正确的是( )
 CuCl2溶液与乙二胺(H2N-CH2-CH2-NH2)可形成配离子[Cu(En)2]2+(En是乙二胺的简写),其结构如图所示.则配离子[Cu(En)2]2+的配位数和该微料含有的微料间的作用力类型均正确的是( )
CuCl2溶液与乙二胺(H2N-CH2-CH2-NH2)可形成配离子[Cu(En)2]2+(En是乙二胺的简写),其结构如图所示.则配离子[Cu(En)2]2+的配位数和该微料含有的微料间的作用力类型均正确的是( )| A. | 4,配位键、极性键、非极性键 | B. | 2,极性键、非极性键、氢键 | ||
| C. | 4,离子键、配位键、氢键 | D. | 2,配位键、非极性键、极性键、氢键 |
15.下列离子方程式正确的是( )
| A. | 氯化铝溶液中加入过量氨水:Al3++3NH3.H2O=Al(OH)3↓+3NH4+ | |
| B. | 碳酸钙和盐酸反应:CO32-+2H+=CO2↑+H2O | |
| C. | 三氯化铁溶液与氢氧化钠溶液反应:FeCl3+3OH-=Fe(OH)3↓+3Cl- | |
| D. | 铜加入稀硝酸中:Cu+4H++NO3-=Cu2++NO↑+2H2O |
14. 实验室通常以乙醇、乙酸和浓硫酸混合加热制备乙酸乙酯,装置如图所示
实验室通常以乙醇、乙酸和浓硫酸混合加热制备乙酸乙酯,装置如图所示
(1)请用同位素示踪法表示乙酸和乙醇发生酯化反应的反应原理
(2)装置中,b的名称为球形冷凝管(冷凝管),其主要作用是冷凝回流;加热前,通常需要在a中加入碎瓷片,目的是防止暴沸
(3)为了证明浓硫酸的作用,某同学进行了以下4个实验,实验开始先用酒精灯微热3min,再加热使之微微沸腾3min,实验结束后测分水器中有机物的厚度,实验记录如表:
①为更好地测定酯层厚度,可预先向饱和Na2CO3溶液中滴加1滴酚酞试液,每次实验结束后可观察到分水器中的现象是液体分层,上层呈无色,下层呈红色
②分析实验A、B、C的数据,可以得出浓硫酸在反应中的作用是催化剂、吸水剂;实验D和实验C对照,你又能得出的结论是对该反应起催化作用的实际上为H+
(4)本实验制备乙酸乙酯的装置与教材装置相比较突出的优点是一是增加了温度计,有利于控制发生装置中反应液的温度,二是增加了冷凝装置,有利于收集产物,三是增加了分水器,能够在反应进行时很容易的把水分离出来,从而使平衡正向移动,提高乙酸乙酯的产率(至少答出两点)
 实验室通常以乙醇、乙酸和浓硫酸混合加热制备乙酸乙酯,装置如图所示
实验室通常以乙醇、乙酸和浓硫酸混合加热制备乙酸乙酯,装置如图所示(1)请用同位素示踪法表示乙酸和乙醇发生酯化反应的反应原理

(2)装置中,b的名称为球形冷凝管(冷凝管),其主要作用是冷凝回流;加热前,通常需要在a中加入碎瓷片,目的是防止暴沸
(3)为了证明浓硫酸的作用,某同学进行了以下4个实验,实验开始先用酒精灯微热3min,再加热使之微微沸腾3min,实验结束后测分水器中有机物的厚度,实验记录如表:
| 实验编号 | 试管Ⅰ中试剂 | 试管Ⅱ中试剂 | 有机层厚度/cm |
| A | 3mL乙醇、2mL乙酸、1mL 18mol•L-1浓硫酸 | 饱和Na2CO3溶液 | 5.0 |
| B | 3mL乙醇、2mL乙酸 | 饱和Na2CO3溶液 | 0.1 |
| C | 3mL乙醇、2mL乙酸、6mL 3mol•L-1硫酸 | 饱和Na2CO3溶液 | 1.2 |
| D | 3mL乙醇、2mL乙酸、6mL6mol•L-1盐酸 | 饱和Na2CO3溶液 | 1.2 |
②分析实验A、B、C的数据,可以得出浓硫酸在反应中的作用是催化剂、吸水剂;实验D和实验C对照,你又能得出的结论是对该反应起催化作用的实际上为H+
(4)本实验制备乙酸乙酯的装置与教材装置相比较突出的优点是一是增加了温度计,有利于控制发生装置中反应液的温度,二是增加了冷凝装置,有利于收集产物,三是增加了分水器,能够在反应进行时很容易的把水分离出来,从而使平衡正向移动,提高乙酸乙酯的产率(至少答出两点)
13.某兴趣小组为研究电池原理,设计如图装置.以下叙述不正确的是( )
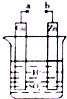

| A. | a和b不连接时,无电流产生,Zn片表面有气泡逸出 | |
| B. | a和b用导线连接,有电流产生,Cu片表面有气泡逸出 | |
| C. | 无论a和b是否连接,Zn片均被腐蚀,溶液的pH均减小 | |
| D. | 若将装置中H2SO4溶液换成CuSO4溶液仍然可以设计成原电池 |
12.已知锌与稀盐酸反应放热.某学生为了探究其反应过程中的速率变化,用排水集气法收集反应放出的氢气.
所用稀盐酸浓度为1.00mol•L-1、2.00mol•L-1,锌有细颗粒与粗颗粒两种规格,用量为6.50g.实验温度为298K、308K,每次实验稀盐酸的用量为25.0mL.
(1)完成以下实验设计(填写表格中空白项),并在实验目的一栏中填出对应的实验编号:
(2)实验①记录如下:
①计算在30-40s范围内盐酸的平均反应速率v(HCl)=0.056mol/(L•s).(忽略溶液体积变化,不需要写出计算过程).
②反应速率最大的时间段(即0~10S、10~20S、20~30S、30~40S、40~50S、…)为40~50s,可能原因是反应放热;
③反应速率最小的时间段为90~100s,可能原因是盐酸浓度降低.
(3)另一学生也做同样的实验,由于反应太快,测量氢气的体积时不好控制,他就事先在硫酸溶液中分别加入等体积的下落溶液以减慢反应速率:
A.蒸馏水B.CuCl2溶液C.NaCl溶液
你认为他上述做法中可行的是AC(填相应字母).
0 170200 170208 170214 170218 170224 170226 170230 170236 170238 170244 170250 170254 170256 170260 170266 170268 170274 170278 170280 170284 170286 170290 170292 170294 170295 170296 170298 170299 170300 170302 170304 170308 170310 170314 170316 170320 170326 170328 170334 170338 170340 170344 170350 170356 170358 170364 170368 170370 170376 170380 170386 170394 203614
所用稀盐酸浓度为1.00mol•L-1、2.00mol•L-1,锌有细颗粒与粗颗粒两种规格,用量为6.50g.实验温度为298K、308K,每次实验稀盐酸的用量为25.0mL.
(1)完成以下实验设计(填写表格中空白项),并在实验目的一栏中填出对应的实验编号:
| 编号 | T/K | 锌规格 | 盐酸浓度/mol•L-1 | 实验目的 |
| ① | 298 | 粗颗粒 | 2.00 | (Ⅰ)实验①和②探究盐酸浓度对该反应速率的影响;(Ⅱ)实验①和 ③探究温度对该反应速率的影响;(Ⅲ)实验①和 ④探究锌规格(粗、细)对该反应速率的影响. |
| ② | 298 | |||
| ③ | 308 | |||
| ④ | 298 |
| 时间(S) | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| 氢气体积(mL) | 16.8 | 39.2 | 67.2 | 224 | 420 | 492.8 | 520.8 | 543.2 | 554.4 | 560 |
②反应速率最大的时间段(即0~10S、10~20S、20~30S、30~40S、40~50S、…)为40~50s,可能原因是反应放热;
③反应速率最小的时间段为90~100s,可能原因是盐酸浓度降低.
(3)另一学生也做同样的实验,由于反应太快,测量氢气的体积时不好控制,他就事先在硫酸溶液中分别加入等体积的下落溶液以减慢反应速率:
A.蒸馏水B.CuCl2溶液C.NaCl溶液
你认为他上述做法中可行的是AC(填相应字母).