题目内容
11.短周期元素A、B、C、D、E位于同周期且原子序数依次增大.已知A、C、E三种元素的原子的最外层共有10个电子,且这三种元素的最高价氧化物所对应的水化物之间两两皆能反应.D原子最外层的电子数的次外层的一半.请完成下列各小题:(1)A、B、C三种元素最高价氧化物对应水化物中,碱性最强的是NaOH(用化学式表示)
(2)指出元素E在元素周期表中的位置:第三周期第ⅥA族.
(3)元素C的氯化物属于共价化合物(填“离子”或“共价”)
(4)A、C元素的最高价氧化物对应水化物之间反应的离子方程式为OH-+Al(OH)3=AlO2-+2H2O.
(5)在生活中,常利用C的单质与Fe2O3在高温下的反应来进行焊接钢轨.请写出该反应的化学方程式2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$Al2O3+2Fe.该反应属于放热反应(填“吸热”或“放热”)
(6)D元素的单质在生产和生活中有广泛的应用,请写出工业上制备D单质(粗产品)的化学方程式:SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑.请举出D的单质在生产和生活中的一种应用半导体材料、太阳能电池.
分析 短周期元素A、B、C、D、E位于同周期且原子序数依次增大.A、C、E三种元素原子的最外层共有10个电子,且这三种元素的最高价氧化物所对应的水化物之间两两皆能反应,均生成盐和水,为氢氧化铝、强碱、强酸的反应,故A为Na、C为Al,B为Mg元素,E原子最外层电子数为10-1-3=6,则E为硫元素;D原子最外层的电子数是次外层的一半,处于第三周期,最外层电子数为4,故D为Si.
(1)金属性越强,最高价氧化物对应水化物的碱性越强;
(2)主族元素周期数=电子层数、主族族序数=最外层电子数;
(3)氯化铝属于共价化合物;
(4)氢氧化钠与氢氧化铝反应生成偏铝酸钠与水;
(5)Al与氧化铁在高温下反应生成氧化铝与Fe,该反应为铝热反应,放出大量的热;
(6)工业上制备Si,用碳与二氧化硅反应生成Si与CO,硅是良好的半导体材料、可以用作太阳能电池等.
解答 解:短周期元素A、B、C、D、E位于同周期且原子序数依次增大.A、C、E三种元素原子的最外层共有10个电子,且这三种元素的最高价氧化物所对应的水化物之间两两皆能反应,均生成盐和水,为氢氧化铝、强碱、强酸的反应,故A为Na、C为Al,B为Mg元素,E原子最外层电子数为10-1-3=6,则E为硫元素;D原子最外层的电子数是次外层的一半,处于第三周期,最外层电子数为4,故D为Si.
(1)金属性Na>Mg>Al,金属性越强,最高价氧化物对应水化物的碱性越强,故碱性:NaOH>Mg(OH)2>Al(OH)3,故答案为:NaOH;
(2)E为硫元素,原子有3个电子层,最外层电子数为6,处于周期表第三周期第ⅥA族,故答案为:第三周期第ⅥA族;
(3)氯化铝属于共价化合物,故答案为:共价;
(4)氢氧化钠与氢氧化铝反应生成偏铝酸钠与水,反应离子方程式为:OH-+Al(OH)3=AlO2-+2H2O,故答案为:OH-+Al(OH)3=AlO2-+2H2O;
(5)Al与氧化铁在高温下反应生成氧化铝与Fe,反应方程式为:2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$Al2O3+2Fe,该反应为铝热反应,放出大量的热,属于放热反应,
故答案为:2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$Al2O3+2Fe;放热;
(6)工业上用碳与二氧化硅反应制备硅,反应生成Si与CO,反应方程式为:SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑,硅是良好的半导体材料、可以用作太阳能电池等,
故答案为:SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑;半导体材料、太阳能电池.
点评 本题考查结构性质位置关系应用等,难度不大,推断元素是解题的关键,注意基础知识的理解掌握.

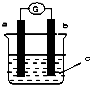
| A. | a是锌,b 是铜,c 是H2SO4 溶液 | B. | a是铁,b 是银,c 是 AgNO3溶液 | ||
| C. | a是银,b 是铁,c是AgNO3 溶液 | D. | a是铁,b是碳,c 是CuCl2 溶液 |
①硅是构成岩石和许多矿物的基本元素
②水泥、玻璃、玛瑙饰物都是硅酸盐制品
③高纯度的硅单质广泛用于光纤通讯
④陶瓷、玻璃、水泥是人类使用量最大的无机非金属材料
⑤硅胶既可做干燥剂也可做催化剂的载体.
| A. | ①④⑤ | B. | ②③ | C. | ②④⑤ | D. | ①③④ |
| A. | 晶体的熔、沸点高,硬度大 | |
| B. | 该物质的化学式为CO4 | |
| C. | 晶体中C原子数与C-O化学键数之比为1:4 | |
| D. | 晶体的空间最小环由12个原子构成 |
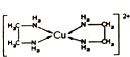 CuCl2溶液与乙二胺(H2N-CH2-CH2-NH2)可形成配离子[Cu(En)2]2+(En是乙二胺的简写),其结构如图所示.则配离子[Cu(En)2]2+的配位数和该微料含有的微料间的作用力类型均正确的是( )
CuCl2溶液与乙二胺(H2N-CH2-CH2-NH2)可形成配离子[Cu(En)2]2+(En是乙二胺的简写),其结构如图所示.则配离子[Cu(En)2]2+的配位数和该微料含有的微料间的作用力类型均正确的是( )| A. | 4,配位键、极性键、非极性键 | B. | 2,极性键、非极性键、氢键 | ||
| C. | 4,离子键、配位键、氢键 | D. | 2,配位键、非极性键、极性键、氢键 |
 W、M、X、Y、Z五种短周期元素在周期表中的位置如表所示,其中只有M为金属元素.请回答下列问题:
W、M、X、Y、Z五种短周期元素在周期表中的位置如表所示,其中只有M为金属元素.请回答下列问题:| W | ||||
| M | X | Y | Z |
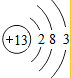 ,比较Y与Z两种元素的简单离子的半径大小:S2->Cl-(用离子符号表示)
,比较Y与Z两种元素的简单离子的半径大小:S2->Cl-(用离子符号表示)(2)写出X的氧化物与W的氢化物的水溶液反应的化学方程式:SiO2+4HF=SiF4↑+2H2O.
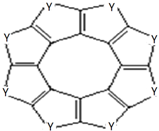
(3)科学家研制出一种英文名为sulflower的新型分子C16Y8(结构如图所示).1mol C16Y8最多能与8mol H2发生加成反应.
(4)托帕石是一种名贵黄玉,其组成为M2[XO4]WOH,托帕在强碱溶液中会发生腐蚀,写出托帕石粉末与过量NaOH溶液反应的化学方程式:Al2[SiO4]FOH+5NaOH=2NaAlO2+Na2SiO3+NaF+3H2O.
| A. | 用SO2漂白食品 | B. | 用硅制作太阳能电池 | ||
| C. | 工业上用氮气和氢气合成氨 | D. | 可用氢氟酸蚀刻玻璃 |