5.下列物质中,水解的最终产物中为葡萄糖的是( )
| A. | 乙酸钠 | B. | 纤维素 | C. | 油脂 | D. | 蛋白质 |
3.下列说法正确的是( )
| A. | 甲烷和乙醇均能发生取代反应 | |
| B. | 蛋白质、淀粉、油脂均能发生水解反应 | |
| C. | 溴乙烷与NaOH水溶液共热生成乙烯 | |
| D. | 油脂和淀粉都是高分子化合物 |
2.下列除杂质(括号里物质为杂质)的方法正确的是( )
| A. | 甲醛(甲酸):加入NaOH溶液加热,分液 | |
| B. | 苯(苯酚):溴水,过滤 | |
| C. | 乙酸乙酯(乙酸):加入饱和Na2CO3溶液,分液 | |
| D. | 乙烷(乙烯):酸性高锰酸钾溶液,洗气 |
1.关于下列各组物质说法正确的是( )
| A. | 苯和甲苯不互为同系物 | B. | 淀粉和纤维素互为同分异构体 | ||
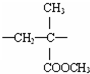
| C. | 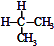 与 与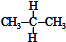 互为同分异构体 互为同分异构体 | D. | 异丁烷与2-甲基丙烷互为同种物质 |
20.下列说法正确的是( )
| A. | 聚乙烯能使溴水褪色 | |
| B. | 油脂是天然高分子化合物 | |
| C. | 葡萄糖分子结构中只有一个醛基,所以是单糖 | |
| D. | 生成高分子化合物的常见反应是加聚反应和缩聚反应 |
18.下列有关Na2CO3溶液说法不正确的是( )
0 170063 170071 170077 170081 170087 170089 170093 170099 170101 170107 170113 170117 170119 170123 170129 170131 170137 170141 170143 170147 170149 170153 170155 170157 170158 170159 170161 170162 170163 170165 170167 170171 170173 170177 170179 170183 170189 170191 170197 170201 170203 170207 170213 170219 170221 170227 170231 170233 170239 170243 170249 170257 203614
| A. | 溶液呈碱性 | |
| B. | C(Na+)+C(H+)=C(OH-)+C(CO32-)+C(HCO3-) | |
| C. | 溶液中存在两个水解平衡关系:CO32-+H2O?HCO3-+OH-(主要)HCO3-+H2O?H2CO3+OH-(次要) | |
| D. | 溶液中离子浓度大小关系为:C(Na+)>C(CO32-)>C(OH-)>C(HCO3-)>C(H+) |
 某产品只含C、H、O三种元素,分子模型如图所示(图中球与球之间的连线代表化学键,如单键、双键等).
某产品只含C、H、O三种元素,分子模型如图所示(图中球与球之间的连线代表化学键,如单键、双键等). 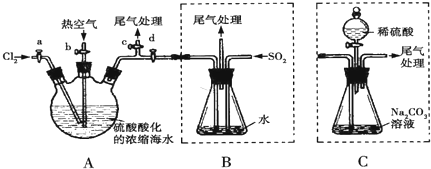

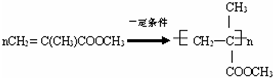
 Ⅰ:A、B、W、D、E为短周期元素,且原子序数依次增大,质子数之和为39,B、W同周期,A、D同主族,A、W能形成两种液态化合物A2W和A2W2,E元素的周期序数与主族序数相等.
Ⅰ:A、B、W、D、E为短周期元素,且原子序数依次增大,质子数之和为39,B、W同周期,A、D同主族,A、W能形成两种液态化合物A2W和A2W2,E元素的周期序数与主族序数相等.
 .
.