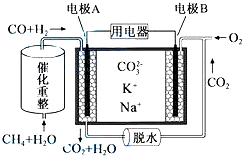
10.通过NO传感器可监测NO的含量,其工作原理如图所示.下列说法错误的是( )


| A. | 该装置实现化学能向电能的转化 | |
| B. | 该电池的总反应为2NO+O2═2NO2 | |
| C. | NiO电极的电极反应式:NO+O2--2e-═NO2 | |
| D. | 当有2.24L的O2参与反应时,转移了0.4mole- |
9.铝硅合金具有熔点低、凝固时收缩率小等优点,适合铸造.现取试样10.0mg,放在纯净氧气中完全燃烧,燃烧后的固体经称量发现比原来试样增重9.23mg,由此计算硅铝合金中硅的质量分数为( )
| A. | 12.3% | B. | 15.4% | C. | 13.4% | D. | 17.0% |
6.已知:
C(s)+H2O(g)=CO(g)+H2(g)△H=+130kJ•mol-1
2C(s)+O2(g)=2CO(g)△H=-220kJ•mol-1
H-H、O=O键能分别为436、496kJ•mol-1,则O-H键能为( )
C(s)+H2O(g)=CO(g)+H2(g)△H=+130kJ•mol-1
2C(s)+O2(g)=2CO(g)△H=-220kJ•mol-1
H-H、O=O键能分别为436、496kJ•mol-1,则O-H键能为( )
| A. | 222 kJ•mol-1 | B. | 444 kJ•mol-1 | C. | 462 kJ•mol-1 | D. | 924 kJ•mol-1 |
5.铝粉和铁红的混合物分成两等份,一份直接放入足量的烧碱溶液中;另一份在高温下恰好完全反应,产物再与足量盐酸充分反应.则两种情况下生成的气体体积比(相同条件)是( )
| A. | 2:3 | B. | 3:2 | C. | 1:1 | D. | 2:1 |
4.在一定温度下,10mL0.50mol/L H2O2发生催化分解.不同时刻测定生成O2的体积(已折算为标准状况)如下表.
下列叙述正确的是(溶液体积变化忽略不计)( )
| t/min | 0 | 2 | 4 | 6 | 8 | 10 |
| V(O2)/mL | 0.0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.1 |
| A. | 0~6 min的平均反应速率:v(H2O2)≈0.33 mol/(L•min) | |
| B. | 6~10 min的平均反应速率:v(H2O2)>3.3×10-2 mol/(L•min) | |
| C. | 反应到6 min时,H2O2分解了60% | |
| D. | 反应到10 min时,c(H2O2)≈0.24 mol/L |
3.铜的冶炼大致可分为:
①富集,将硫化物矿进行浮选;
②焙烧,主要反应为2CuFeS2+4O2═Cu2S+3SO2+2FeO(炉渣);
③制粗铜,在1200℃发生的主要反应为2Cu2S+3O2═2Cu2O+2SO2,2Cu2O+Cu2S═6Cu+SO2↑;
④电解精炼铜.
下列说法不正确的是( )
①富集,将硫化物矿进行浮选;
②焙烧,主要反应为2CuFeS2+4O2═Cu2S+3SO2+2FeO(炉渣);
③制粗铜,在1200℃发生的主要反应为2Cu2S+3O2═2Cu2O+2SO2,2Cu2O+Cu2S═6Cu+SO2↑;
④电解精炼铜.
下列说法不正确的是( )
| A. | 上述灼烧过程的尾气回收后可用来制硫酸 | |
| B. | 上述过程中,由6 mol CuFeS2制取6 mol Cu时共消耗15 mol O2 | |
| C. | 在反应2Cu2O+Cu2S═6Cu+SO2↑中,只有Cu2O作氧化剂 | |
| D. | 1200℃灼烧Cu2S得Cu2O而不是CuO,可能是高温下+1价铜更稳定 |
2.一种有机玻璃的结构简式为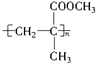 关于它的叙述不正确的是( )
关于它的叙述不正确的是( )
 关于它的叙述不正确的是( )
关于它的叙述不正确的是( )| A. | 该有机玻璃的化学名称为聚甲基丙烯酸甲酯 | |
| B. | 该有机玻璃可用2-甲基丙烯酸和甲醇为原料,通过酯化反应、加聚反应制得 | |
| C. | 它在一定条件下发生水解反应时,可得到另外一种高分子化合物 | |
| D. | 等物质的量的有机玻璃和2-甲基丙烯酸甲酯耗氧量相同 |
1.工业上以铝土矿(主要成分是Al2O3,含杂质Fe2O3和SiO2)为原料生产铝,其生产流程如下:
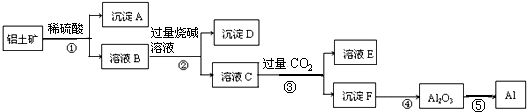
下列叙述错误的是( )
0 170011 170019 170025 170029 170035 170037 170041 170047 170049 170055 170061 170065 170067 170071 170077 170079 170085 170089 170091 170095 170097 170101 170103 170105 170106 170107 170109 170110 170111 170113 170115 170119 170121 170125 170127 170131 170137 170139 170145 170149 170151 170155 170161 170167 170169 170175 170179 170181 170187 170191 170197 170205 203614

下列叙述错误的是( )
| A. | 沉淀A主要是SiO2 | B. | 步骤②的目的是分离Fe3+和Al3+ | ||
| C. | 溶液E溶质主要有碳酸钠和硫酸钠 | D. | ⑤主要是把电能转化为化学能 |
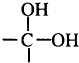 →
→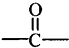 +H2O图中B和
+H2O图中B和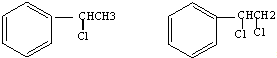 等都是A和Cl2发生反应生成的产物,E是一种高分子化合物,透光性能好,常用作一些灯饰外壳(过程中一些小分子未写出).
等都是A和Cl2发生反应生成的产物,E是一种高分子化合物,透光性能好,常用作一些灯饰外壳(过程中一些小分子未写出).
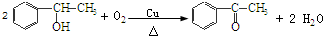 ’,该反应类型为氧化反应
’,该反应类型为氧化反应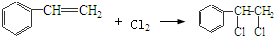 ,该反应类型为加成反应
,该反应类型为加成反应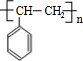
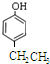 、
、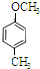 、
、