10.聚四氟乙烯的耐热性和化学稳定性超过其他塑料,被称为“塑料王”.其合成路线如下:
三氯甲烷$\stackrel{HF,SbCl_{3}}{→}$二氟一氯甲烷$\stackrel{△}{→}$四氟乙烯$\stackrel{引发剂}{→}$聚四氟乙烯
下列说法中,不正确的是( )
三氯甲烷$\stackrel{HF,SbCl_{3}}{→}$二氟一氯甲烷$\stackrel{△}{→}$四氟乙烯$\stackrel{引发剂}{→}$聚四氟乙烯
下列说法中,不正确的是( )
| A. | 二氟一氯甲院 (CHClF2)中所有原子最外层都达到了8电子稳定结构 | |
| B. | “塑料王”不能使酸性高锰酸钾溶液褪色 | |
| C. | 四氟乙烯 (CF2=CF2)中所有的原子都在同一个平面上 | |
| D. | 三氯甲烷(CHCl3)可以用甲院与氯气的取代反应来制取 |
9.能用于鉴别乙醇、己烷、己烯、乙酸溶液、苯酚溶液等五种无色液体的试剂组是( )
| A. | FeCl3溶液、NaOH溶液 | B. | Cu(OH)2悬浊液、紫色石蕊试液 | ||
| C. | 紫色石蕊试液、溴水 | D. | FeCl3溶液、溴水引发剂 |
8.L-多巴是一种有机物,它可用于帕金森综合症的治疗,其结构简式如图所示,这种药物的研制是基于获得2000年诺贝尔生理学和医学奖、2001年诺贝尔化学奖的研究成果.下列关于 L-多巴酸性质的叙述正确的是( )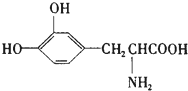

| A. | 只能与碱反应,不能与酸反应 | B. | 1mol该物质最多可与4molNaOH反应 | ||
| C. | 该物质不能使酸性KMnO4褪色 | D. | 1mol该物质最多可与1molHBr反应 |
5.铁单质及其化合物在生活、生产中应用广泛.请回答下列问题:
(1)钢铁在空气中发生吸氧腐蚀时,正极的电极反应式为O2+2H2O+4e-=4OH-.
(2)由于氧化性Fe3+>Cu2+,氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式是Cu+2Fe3+=2Fe2++Cu2+.
(3)硫酸铁可作絮凝剂,常用于净水,其原理是Fe3++3H2O?Fe(OH)3+3H+(用离子方程式表示).在使用时发现硫酸铁不能使酸性废水中的悬浮物沉降而除去,其原因是酸性环境中,氢离子抑制了铁离子的水解,无法生成氢氧化铁胶体.
(4)磁铁矿是工业上冶炼铁的原料之一,其原理是Fe3O4+4CO═3Fe+4CO2,若有1.5mol Fe3O4参加反应,转移电子的物质的量是12mol.
(5)下表中,对陈述Ⅰ、Ⅱ的正确性及其有无因果关系的判断都正确的是B(填字母).
(1)钢铁在空气中发生吸氧腐蚀时,正极的电极反应式为O2+2H2O+4e-=4OH-.
(2)由于氧化性Fe3+>Cu2+,氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式是Cu+2Fe3+=2Fe2++Cu2+.
(3)硫酸铁可作絮凝剂,常用于净水,其原理是Fe3++3H2O?Fe(OH)3+3H+(用离子方程式表示).在使用时发现硫酸铁不能使酸性废水中的悬浮物沉降而除去,其原因是酸性环境中,氢离子抑制了铁离子的水解,无法生成氢氧化铁胶体.
(4)磁铁矿是工业上冶炼铁的原料之一,其原理是Fe3O4+4CO═3Fe+4CO2,若有1.5mol Fe3O4参加反应,转移电子的物质的量是12mol.
(5)下表中,对陈述Ⅰ、Ⅱ的正确性及其有无因果关系的判断都正确的是B(填字母).
| 选项 | 陈述Ⅰ | 陈述Ⅱ | 判断 |
| A | 铁是地壳中含量最高的 金属元素 | 铁是人类最早使用的金属材料 | Ⅰ对;Ⅱ对;有 |
| B | 常温下铁与稀硫酸反应 生成氢气 | 高温下氢气能还原氧化 铁得到铁 | Ⅰ对;Ⅱ对;无 |
| C | 铁属于过渡元素 | 铁和铁的某些化合物可用作催化剂 | Ⅰ错;Ⅱ对;无 |
| D | 在空气中铁的表面能形 成致密的氧化膜 | 铁不能与氧气反应 | Ⅰ对;Ⅱ对;有 |
4.某乙醇水溶液的质量分数为w%,物质的量浓度为cmol/L,密度为dg/mL,1Kg这种溶液中含有的乙醇是( )
| A. | 46C | B. | $\frac{c}{d}$mol | C. | c mol | D. | 1000dw g |
3.下列排列顺序正确的是( )
①固体热稳定性:Na2CO3>CaCO3>NaHCO3
②微粒半径:F->Na+>Mg2+>S2-
③燃烧热:S(气体)>S(液体)>S(固体)
④物质的熔点:植物油>动物油.
①固体热稳定性:Na2CO3>CaCO3>NaHCO3
②微粒半径:F->Na+>Mg2+>S2-
③燃烧热:S(气体)>S(液体)>S(固体)
④物质的熔点:植物油>动物油.
| A. | ①③④ | B. | ①③ | C. | ①②③④ | D. | ②③④ |
2.下列各组物质中,都能与盐酸反应放出气体,并且后者与盐酸反应比前者与盐酸反应放出气体更迅速的是(溶液的浓度均相同)( )
| A. | Na2CO3和NaHCO3 | B. | Na和Mg | C. | KHCO3和K2CO3 | D. | Si和Al |
1.已知白磷(P4)与CuSO4溶液反应的化学方程式为(Cu3P中P的化合价为-3价):11P4+60CuSO4+96H2O═20Cu3P+24H3PO4+60H2SO4,则2molCuSO4能氧化白磷的物质的量是( )
0 170003 170011 170017 170021 170027 170029 170033 170039 170041 170047 170053 170057 170059 170063 170069 170071 170077 170081 170083 170087 170089 170093 170095 170097 170098 170099 170101 170102 170103 170105 170107 170111 170113 170117 170119 170123 170129 170131 170137 170141 170143 170147 170153 170159 170161 170167 170171 170173 170179 170183 170189 170197 203614
| A. | $\frac{1}{20}$mol | B. | $\frac{1}{10}$mol | C. | $\frac{1}{5}$mol | D. | $\frac{2}{5}$mol |
 铜是重要金属,Cu的化合物在科学研究和工业生产中具有许多用途,如CuSO4溶液常用作电解液、电镀液等.请回答以下问题:
铜是重要金属,Cu的化合物在科学研究和工业生产中具有许多用途,如CuSO4溶液常用作电解液、电镀液等.请回答以下问题: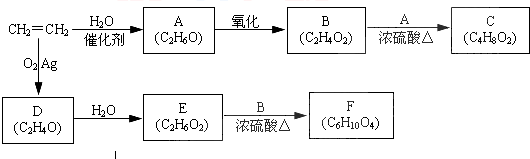
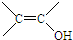 、
、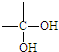 结构非常不稳定,会迅速转变为
结构非常不稳定,会迅速转变为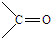
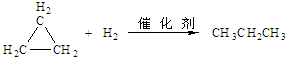
 .
.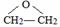 .
.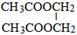 .
.