1.工业上利用CO和水蒸气在一定条件下发生反应制取氢气:
CO(g)+H2O(g)?CO2(g)+H2(g)△H=-41kJ/mol
某小组研究在相同温度下该反应过程中的能量变化.他们分别在体积均为2L的两个恒温恒容密闭容器中加入一定量的反应物,使其在相同温度下发生反应.相关数据如下:
(1)该反应过程中,反应物分子化学键断裂时所吸收的总能量<(填“>”、“=”或“<”)生成物分子化学键形成时所释放的总能量;
(2)容器①中反应达平衡时,CO的转化率为80%;
(3)计算容器②中反应的平衡常数K=2;
(4)下列叙述正确的是ad(填字母序号);
a.平衡时,两容器中H2的体积分数相等
b.容器②中反应达平衡状态时,Q>65.6kJ
c.反应开始时,两容器中反应的化学反应速率相等
d.容器①中,反应的化学反应速率为:v(H2O)=$\frac{0.4}{{t}_{1}}$mol•L-1•min-1
(5)已知:2H2(g)+O2(g)═2H2O(g)△H=-484kJ/mol,写出CO完全燃烧生成CO2的热化学方程式:2CO(g)+O2(g)═2CO2(g)△H=-566KJ/mol.
CO(g)+H2O(g)?CO2(g)+H2(g)△H=-41kJ/mol
某小组研究在相同温度下该反应过程中的能量变化.他们分别在体积均为2L的两个恒温恒容密闭容器中加入一定量的反应物,使其在相同温度下发生反应.相关数据如下:
| 容器编号 | 起始时各物质物质的量/mol | 达到平衡的时间/min | 达平衡时体系能量的变化/kJ | ||||
| CO | H2O | CO2 | H2 | ||||
| ① | 1 | 2.4 | 0 | 0 | t1 | 放出热量:32.8 kJ | |
| ② | 2 | 4.8 | 0 | 0 | t2 | 放出热量:Q | |
(2)容器①中反应达平衡时,CO的转化率为80%;
(3)计算容器②中反应的平衡常数K=2;
(4)下列叙述正确的是ad(填字母序号);
a.平衡时,两容器中H2的体积分数相等
b.容器②中反应达平衡状态时,Q>65.6kJ
c.反应开始时,两容器中反应的化学反应速率相等
d.容器①中,反应的化学反应速率为:v(H2O)=$\frac{0.4}{{t}_{1}}$mol•L-1•min-1
(5)已知:2H2(g)+O2(g)═2H2O(g)△H=-484kJ/mol,写出CO完全燃烧生成CO2的热化学方程式:2CO(g)+O2(g)═2CO2(g)△H=-566KJ/mol.
19.下述实验方案能达到实验目的是( )
| A. |  验证铁钉发生吸氧腐蚀 | |
| B. | 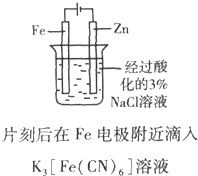 证明Fe电极被保护 | |
| C. | 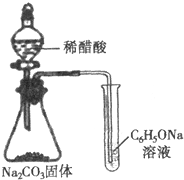 酸性强弱顺序为CH3COOH>H2CO3>C6H5OH | |
| D. | 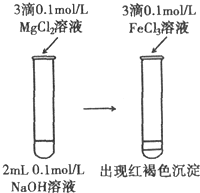 溶解度:Mg(OH)2>Fe(OH)3 |
17.某种氢氧燃料电池的电解液为KOH溶液,下列有关电池的叙述不正确的是( )
| A. | 正极反应式为:O2+2H2O+4e-═4OH- | |
| B. | 该燃料电池的总反应方程式为:2H2+O2═2H2O | |
| C. | 工作一段时间后,电解液中的KOH的物质的量不变 | |
| D. | 工作时溶液中K+向负极移动 |
16.下列关于化学反应中物质或能量变化的判断正确的是( )
| A. | 使电流通过电解质溶液而在阴、阳两极引起氧化还原反应,此过程中电能转化为化学能 | |
| B. | 一定条件下进行的化学反应,只能将化学能转化成光能或热能 | |
| C. | 需要加热才能进行的反应一定是吸热反应,放热反应不需要加热 | |
| D. | 将NaHCO3溶液蒸干后并加热至质量不发生变化,最终所得固体仍为NaHCO3 |
15.已知反应A(g)+3B(g)?2C(g)△H<O,达到平衡后,将气体混合物的反应温度降低,下列叙述正确的是( )
| A. | 正反应速率加大,逆反应速率减小,平衡向正反应方向移动 | |
| B. | 正反应速率减小,逆反应速率加大,平衡向逆反应方向移动 | |
| C. | 正反应速率和逆反应速率都减小,平衡向正反应方向移动 | |
| D. | 正反应速率和逆反应速率都减小,平衡向逆反应方向移动 |
14.废电池进行集中处理的首要原因是( )
| A. | 回收其中的石墨电极 | |
| B. | 回收利用电池外壳的金属材料 | |
| C. | 不使电池中渗露的电解液腐蚀其他物品 | |
| D. | 防止电池中汞、镉和铅等重金属离子对土壤和水源的污染 |
13.书写热化学方程式时要注明物质的状态,其主要原因是( )
| A. | 物质的状态与反应热有关 | B. | 物质的状态与生成物有关 | ||
| C. | 可以具体说明反应进行的情况 | D. | 可以具体说明反应发生的条件 |
12.氮元素的单质和常见的化合物在工、农业生产中用途广泛.
(1)工业上利用分离空气的方法得到氮气.空气各主要成分的沸点如下:
现将空气深度冷却液化,然后缓慢升温,则最先分离出来的气体是N2.
(2)雷雨时空气中的N2转化为NO,生成物NO是无色的气体,难(填“易”或“难”)溶于水;NO在空气中很容易被氧化成NO2,NO2能与水发生化学反应.NO2与水反应的化学方程式为3NO2+H2O=2HNO3+NO.
(3)实验室可用固体NH4Cl与固体Ca(OH)2加热反应制取氨气.
①制取氨气的化学方程式为2NH4Cl+Ca(OH)2$\frac{\underline{\;加热\;}}{\;}$CaCl2+2H2O+2NH3↑;
②要制取标准状况下4.48L的氨气,至少需要称取固体NH4Cl的质量为10.7g.
(4)已知:4NH3+6NO$\frac{\underline{\;催化剂\;}}{\;}$5N2+6H2O.化学研究性学习小组的同学在技术人员的指导下,按下列流程,探究不同催化剂对NH3还原NO反应的催化性能.

若控制其他实验条件均相同,在催化反应器中装载不同的催化剂,将经催化反应后的混合气体,通过一定体积滴有酚酞的稀硫酸溶液(溶液的体积、浓度均相同).
①NH3与稀硫酸溶液反应的离子方程式为NH3+H+=NH4+;;
②为了比较不同催化剂的催化性能,需要测量并记录的数据是溶液显色所需时间.
0 169945 169953 169959 169963 169969 169971 169975 169981 169983 169989 169995 169999 170001 170005 170011 170013 170019 170023 170025 170029 170031 170035 170037 170039 170040 170041 170043 170044 170045 170047 170049 170053 170055 170059 170061 170065 170071 170073 170079 170083 170085 170089 170095 170101 170103 170109 170113 170115 170121 170125 170131 170139 203614
(1)工业上利用分离空气的方法得到氮气.空气各主要成分的沸点如下:
| N2 | O2 | Ar | CO2 |
| -196°C | -183°C | -186°C | -78°C |
(2)雷雨时空气中的N2转化为NO,生成物NO是无色的气体,难(填“易”或“难”)溶于水;NO在空气中很容易被氧化成NO2,NO2能与水发生化学反应.NO2与水反应的化学方程式为3NO2+H2O=2HNO3+NO.
(3)实验室可用固体NH4Cl与固体Ca(OH)2加热反应制取氨气.
①制取氨气的化学方程式为2NH4Cl+Ca(OH)2$\frac{\underline{\;加热\;}}{\;}$CaCl2+2H2O+2NH3↑;
②要制取标准状况下4.48L的氨气,至少需要称取固体NH4Cl的质量为10.7g.
(4)已知:4NH3+6NO$\frac{\underline{\;催化剂\;}}{\;}$5N2+6H2O.化学研究性学习小组的同学在技术人员的指导下,按下列流程,探究不同催化剂对NH3还原NO反应的催化性能.

若控制其他实验条件均相同,在催化反应器中装载不同的催化剂,将经催化反应后的混合气体,通过一定体积滴有酚酞的稀硫酸溶液(溶液的体积、浓度均相同).
①NH3与稀硫酸溶液反应的离子方程式为NH3+H+=NH4+;;
②为了比较不同催化剂的催化性能,需要测量并记录的数据是溶液显色所需时间.