题目内容
20.醋酸钾是有机融雪剂的主要成分,其溶液的冰点可达到-30℃左右.请回答:(1)醋酸盐均可溶于水,以醋酸钾为主要成分的有机融雪剂溶于水后呈碱性,用离子方程式表示其原因CH3COO-+H2O?CH3COOH+OH-.
(2)根据醋酸钾溶液中离子浓度间的关系,判断:
溶液中存在下列关系:c(K+)+c(H+)=c(CH3COO-)+c(OH-);
溶液中离子浓度由大到小的顺序是:c(K+)>c(CH3COO-)>c(OH-)>c(H+),.
分析 (1)醋酸钾是强碱弱酸盐水解呈碱性,离子方程式为:CH3COO-+H2O?CH3COOH+OH-;
(2)根据电荷守恒分析解答,离子浓度的大小是不水解的离子浓度>水解的离子>显性的离子>隐性离子浓度,由此分析解答.
解答 解:(1)醋酸钾是强碱弱酸盐水解呈碱性,离子方程式为:CH3COO-+H2O?CH3COOH+OH-,故答案为:CH3COO-+H2O?CH3COOH+OH-;
(2)醋酸钾溶液根据电荷守恒;c(K+)+c(H+)=c(CH3COO-)+c(OH-);离子浓度大小为:c(K+)>c(CH3COO-)>c(OH-)>c(H+),
故答案为:c(K+)+c(H+);c(CH3COO-)>c(OH-)>c(H+).
点评 本题考查盐的性质,水解的应用,结合电荷守恒分析离子浓度之间的关系,比较容易.

练习册系列答案
相关题目
10.根据所学知识,完成下列问题:
(1)化学反应可视为旧键断裂和新键生成的过程.键能是形成(或拆开)1mol化学键时释放(或吸收)的能量.已知白磷和其燃烧产物P4O6的分子结构如图1所示,现提供以下键能(kJ•mol-1):P-P:198,P-O:360,O-O:498,白磷(P4)燃烧的热化学方程式为P4(s,白鳞)+3O2(g)═P4O6(s)△H=-1638kJ•mol-1.
(2)化学能与电能之间可以相互转化,以Fe,Cu,C(石墨),CuSO4溶液、FeSO4溶液,Fe2(SO4)3溶液、AgNO3溶液为原料,通过原电池反应实现2Fe3++Cu═2Fe2++Cu2+.请你把图2补充完整,使之形成闭合电路,并用元素符号标明电极.电池中电解液时是CuSO4溶液;乙池中电解液是Fe2(SO4)3溶液.(要求:甲乙两池中电解质元素种类始终保持不变)
(3)某市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5μm的悬浮颗粒物)其主要来源为燃煤、机动车尾气等.因此,对PM2.5、SO2、NOx等进行研究具有重要意义.请回答下列问题:
①对PM2.5空气样本用蒸馏水处理,制成待测试样.若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
根据表中数据判断该试样的酸碱性为酸性,试样的pH值=4
②已知气缸中生成NO的反应为:N2(g)+O2(g)?2NO(g)△H>0
若1mol空气含有0.8molN2和0.2molO2,1300℃时在密闭容器内反应达到平衡.测得NO为8×10-4mol.计算该温度下的平衡常数K=4×10-6;汽车启动后,气缸温度越高,单位时间内NO排放量越大,原因是正反应为吸热反应,升高温度,反应速率加快,平衡右移.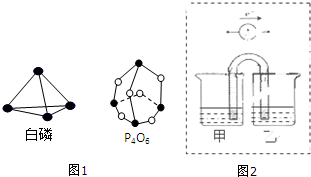
(1)化学反应可视为旧键断裂和新键生成的过程.键能是形成(或拆开)1mol化学键时释放(或吸收)的能量.已知白磷和其燃烧产物P4O6的分子结构如图1所示,现提供以下键能(kJ•mol-1):P-P:198,P-O:360,O-O:498,白磷(P4)燃烧的热化学方程式为P4(s,白鳞)+3O2(g)═P4O6(s)△H=-1638kJ•mol-1.
(2)化学能与电能之间可以相互转化,以Fe,Cu,C(石墨),CuSO4溶液、FeSO4溶液,Fe2(SO4)3溶液、AgNO3溶液为原料,通过原电池反应实现2Fe3++Cu═2Fe2++Cu2+.请你把图2补充完整,使之形成闭合电路,并用元素符号标明电极.电池中电解液时是CuSO4溶液;乙池中电解液是Fe2(SO4)3溶液.(要求:甲乙两池中电解质元素种类始终保持不变)
(3)某市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5μm的悬浮颗粒物)其主要来源为燃煤、机动车尾气等.因此,对PM2.5、SO2、NOx等进行研究具有重要意义.请回答下列问题:
①对PM2.5空气样本用蒸馏水处理,制成待测试样.若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
| 离子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 浓度/mol•L-1 | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
②已知气缸中生成NO的反应为:N2(g)+O2(g)?2NO(g)△H>0
若1mol空气含有0.8molN2和0.2molO2,1300℃时在密闭容器内反应达到平衡.测得NO为8×10-4mol.计算该温度下的平衡常数K=4×10-6;汽车启动后,气缸温度越高,单位时间内NO排放量越大,原因是正反应为吸热反应,升高温度,反应速率加快,平衡右移.

11.下列变化属于物理变化的是( )
| A. | 煤的干馏 | B. | 石油裂解 | ||
| C. | 古代植物变成煤 | D. | 煤焦油中得到苯、甲苯、二甲苯等 |
15.已知反应A(g)+3B(g)?2C(g)△H<O,达到平衡后,将气体混合物的反应温度降低,下列叙述正确的是( )
| A. | 正反应速率加大,逆反应速率减小,平衡向正反应方向移动 | |
| B. | 正反应速率减小,逆反应速率加大,平衡向逆反应方向移动 | |
| C. | 正反应速率和逆反应速率都减小,平衡向正反应方向移动 | |
| D. | 正反应速率和逆反应速率都减小,平衡向逆反应方向移动 |
5.下列物质的结构简式中,书写正确的是( )
| A. | CH2CH2 | B. | CH2=C(CH3)2 | C. | CH3COH | D. | CH3C(CH2)2CH3 |
12.下列有机物中,一氯代物只有一种的是( )
| A. | 苯 | B. | 甲苯 | C. | 丙烷 | D. | 正丁烷 |
9.下列离子方程式中,书写不正确的是( )
| A. | 金属钾与水反应:2K+2H2O═2K++2OH-+2H2↑ | |
| B. | 氯气通入碘化钾溶液中:Cl2+2I-═2Cl-+I2 | |
| C. | 铜片放入稀硝酸中:Cu+4H++2NO3-═Cu2++2NO2↑+2H2O | |
| D. | 醋酸与碳酸钠溶液反应:2CH3COOH+CO32-═2CH3COO-+H2O+CO2↑ |
10.已知:2NO2+2NaOH-→NaNO3+NaNO2+H2O;NO+NO2+2NaOH-→2NaNO2+H2O.将224mL(标况下)NO和NO2的混合气体溶于20mL NaOH溶液中,恰好完全反应并无气体逸出,则NaOH溶液的物质的量浓度为( )
| A. | 1 mol/L | B. | 0.5mol/L | C. | 0.25mol/L | D. | 0.2mol/L |
