10.根据所学知识,完成下列问题:
(1)化学反应可视为旧键断裂和新键生成的过程.键能是形成(或拆开)1mol化学键时释放(或吸收)的能量.已知白磷和其燃烧产物P4O6的分子结构如图1所示,现提供以下键能(kJ•mol-1):P-P:198,P-O:360,O-O:498,白磷(P4)燃烧的热化学方程式为P4(s,白鳞)+3O2(g)═P4O6(s)△H=-1638kJ•mol-1.
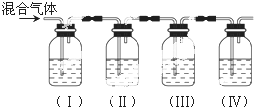
(2)化学能与电能之间可以相互转化,以Fe,Cu,C(石墨),CuSO4溶液、FeSO4溶液,Fe2(SO4)3溶液、AgNO3溶液为原料,通过原电池反应实现2Fe3++Cu═2Fe2++Cu2+.请你把图2补充完整,使之形成闭合电路,并用元素符号标明电极.电池中电解液时是CuSO4溶液;乙池中电解液是Fe2(SO4)3溶液.(要求:甲乙两池中电解质元素种类始终保持不变)
(3)某市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5μm的悬浮颗粒物)其主要来源为燃煤、机动车尾气等.因此,对PM2.5、SO2、NOx等进行研究具有重要意义.请回答下列问题:
①对PM2.5空气样本用蒸馏水处理,制成待测试样.若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
根据表中数据判断该试样的酸碱性为酸性,试样的pH值=4
②已知气缸中生成NO的反应为:N2(g)+O2(g)?2NO(g)△H>0
若1mol空气含有0.8molN2和0.2molO2,1300℃时在密闭容器内反应达到平衡.测得NO为8×10-4mol.计算该温度下的平衡常数K=4×10-6;汽车启动后,气缸温度越高,单位时间内NO排放量越大,原因是正反应为吸热反应,升高温度,反应速率加快,平衡右移.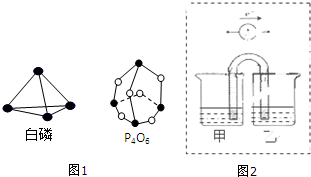
(1)化学反应可视为旧键断裂和新键生成的过程.键能是形成(或拆开)1mol化学键时释放(或吸收)的能量.已知白磷和其燃烧产物P4O6的分子结构如图1所示,现提供以下键能(kJ•mol-1):P-P:198,P-O:360,O-O:498,白磷(P4)燃烧的热化学方程式为P4(s,白鳞)+3O2(g)═P4O6(s)△H=-1638kJ•mol-1.
(2)化学能与电能之间可以相互转化,以Fe,Cu,C(石墨),CuSO4溶液、FeSO4溶液,Fe2(SO4)3溶液、AgNO3溶液为原料,通过原电池反应实现2Fe3++Cu═2Fe2++Cu2+.请你把图2补充完整,使之形成闭合电路,并用元素符号标明电极.电池中电解液时是CuSO4溶液;乙池中电解液是Fe2(SO4)3溶液.(要求:甲乙两池中电解质元素种类始终保持不变)
(3)某市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5μm的悬浮颗粒物)其主要来源为燃煤、机动车尾气等.因此,对PM2.5、SO2、NOx等进行研究具有重要意义.请回答下列问题:
①对PM2.5空气样本用蒸馏水处理,制成待测试样.若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
| 离子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 浓度/mol•L-1 | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
②已知气缸中生成NO的反应为:N2(g)+O2(g)?2NO(g)△H>0
若1mol空气含有0.8molN2和0.2molO2,1300℃时在密闭容器内反应达到平衡.测得NO为8×10-4mol.计算该温度下的平衡常数K=4×10-6;汽车启动后,气缸温度越高,单位时间内NO排放量越大,原因是正反应为吸热反应,升高温度,反应速率加快,平衡右移.

8.咖啡酸具有止血、镇咳、祛痰等疗效,其结构简式为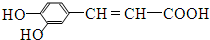 .下列有关咖啡酸的说法中,不正确的是( )
.下列有关咖啡酸的说法中,不正确的是( )
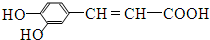 .下列有关咖啡酸的说法中,不正确的是( )
.下列有关咖啡酸的说法中,不正确的是( )| A. | 咖啡酸分子中的所有原子不可能共平面 | |
| B. | 咖啡酸可以发生还原、酯化、加聚、显色等反应 | |
| C. | 1mol咖啡酸可与4 mol Br2发生反应 | |
| D. | 1mol咖啡酸与NaOH溶液反应最多消耗1mol的NaOH |
7.X、Y、Z是三种气态物质,在一定温度下其变化符合如图.下列说法不正确的是( )


| A. | 该反应的化学方程式为X(g)+3Y(g)?2Z(g) | |
| B. | 图Ⅲ中甲表示压强,则纵坐标可表示混合气体中Z的含量或者混合气体的平均摩尔质量 | |
| C. | 若升高温度,该反应的平衡常数减小,Y的转化率降低 | |
| D. | 图Ⅱ中曲线可表示有无催化剂的能量变化曲线 |
5.氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,减少氮的氧化物在大气中的排放是环境保护的重要内容之一.
(1)如图1是1mol NO2气体和1mol CO气体反应生成CO2气体和NO气体过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:NO2(g)+CO(g)═CO2(g)+NO(g)△H=-234kJ•mol-1;
已知:N2 (g)+2NO2 (g)?4NO(g)△H=+292.3kJ•mol-1,
则反应:2NO(g)+2CO(g)?N2(g)+2CO2(g) 的△H=-760.3kJ•mol-1;
(2)一定温度下,在体积为2L的恒容密闭容器中充入20mol NO2和5molO2发生反应:4NO2(g)+O2(g)?2N2O5(g);已知体系中n(NO2)随时间变化如下表:
①写出该反应的平衡常数表达式:K=$\frac{{c}^{2}({N}_{2}{O}_{5})}{{c}^{4}(N{O}_{2}).c({O}_{2})}$,已知:K300℃>K350℃,则该反应是放热反应(填“放热”或“吸热”);
②反应达到平衡后,NO2的转化率为49.6%,若要增大NO2的转化率,可采取的措施有AD
A.降低温度 B.充入氦气,使体系压强增大
C.再充入NO2 D.再充入4mol NO2和1mol O2
③图2中表示N2O5的浓度的变化曲线是C,用O2表示从0~500s内该反应的平均速率v=0.00151mol•L-1•s-1.
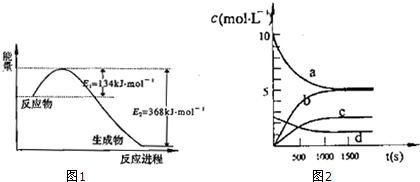
(1)如图1是1mol NO2气体和1mol CO气体反应生成CO2气体和NO气体过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:NO2(g)+CO(g)═CO2(g)+NO(g)△H=-234kJ•mol-1;
已知:N2 (g)+2NO2 (g)?4NO(g)△H=+292.3kJ•mol-1,
则反应:2NO(g)+2CO(g)?N2(g)+2CO2(g) 的△H=-760.3kJ•mol-1;
(2)一定温度下,在体积为2L的恒容密闭容器中充入20mol NO2和5molO2发生反应:4NO2(g)+O2(g)?2N2O5(g);已知体系中n(NO2)随时间变化如下表:
| t(s) | 0 | 500 | 1000 | 1500 |
| n(NO2)(mol) | 20 | 13.96 | 10.08 | 10.08 |
②反应达到平衡后,NO2的转化率为49.6%,若要增大NO2的转化率,可采取的措施有AD
A.降低温度 B.充入氦气,使体系压强增大
C.再充入NO2 D.再充入4mol NO2和1mol O2
③图2中表示N2O5的浓度的变化曲线是C,用O2表示从0~500s内该反应的平均速率v=0.00151mol•L-1•s-1.

4.过氧化氢是重要的氧化剂、还原剂,它的水溶液又称为双氧水,常用作消毒、杀菌、漂白等.某化学兴趣小组取一定量的过氧化氢溶液,准确测定了过氧化氢的含量,并探究了过氧化氢的性质.
Ⅰ.测定过氧化氢的含量
步骤如下并填写下列空白:
(1)将10.00mL密度为ρ g/mL的过氧化氢溶液稀释至250mL.量取稀释后的过氧化氢溶液25.00mL至锥形瓶中,加入稀硫酸酸化,作被测试样.此过程中需要用到的定量仪器250ml容量瓶,滴定管或移液管.
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式如下,请完成该反应方程
2MnO4-+5H2O2+6H+→2Mn2++8H2O+502
(3)滴定时,将高锰酸钾标准溶液注入滴定管中,滴定到达终点的现象是滴入最后一滴高锰酸钾溶液,溶液呈紫红色,且30秒内不褪色
(4)重复滴定二次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为$\frac{0.085cV}{ρ}$.
(5)若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果偏高(填“偏高”“偏低”“不变”).
Ⅱ.探究过氧化氢的性质
该化学小组根据所提供的实验条件设计了两个实验,分别证明了过氧化氢的氧化性和不稳定性.(实验条件:试剂只有过氧化氢溶液、氯水、淀粉碘化钾溶液、二氧化锰,实验仪器及用品可自选.)
请将他们所选的实验试剂和实验现象填入下表:
Ⅰ.测定过氧化氢的含量
步骤如下并填写下列空白:
(1)将10.00mL密度为ρ g/mL的过氧化氢溶液稀释至250mL.量取稀释后的过氧化氢溶液25.00mL至锥形瓶中,加入稀硫酸酸化,作被测试样.此过程中需要用到的定量仪器250ml容量瓶,滴定管或移液管.
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式如下,请完成该反应方程
2MnO4-+5H2O2+6H+→2Mn2++8H2O+502
(3)滴定时,将高锰酸钾标准溶液注入滴定管中,滴定到达终点的现象是滴入最后一滴高锰酸钾溶液,溶液呈紫红色,且30秒内不褪色
(4)重复滴定二次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为$\frac{0.085cV}{ρ}$.
(5)若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果偏高(填“偏高”“偏低”“不变”).
Ⅱ.探究过氧化氢的性质
该化学小组根据所提供的实验条件设计了两个实验,分别证明了过氧化氢的氧化性和不稳定性.(实验条件:试剂只有过氧化氢溶液、氯水、淀粉碘化钾溶液、二氧化锰,实验仪器及用品可自选.)
请将他们所选的实验试剂和实验现象填入下表:
| 实 验 内 容 | 实 验 试 剂 | 实 验 现 象 |
| 探究氧化性 | 取适量碘化钾淀粉溶液于试管中,加入过氧化氢溶液 | 溶液变蓝色 |
| 探究不稳定性 | 取适量过氧化氢溶液于试管中,加热, 用带火星的木条检验 | 产生气泡,木条复燃 |
3.在2L密闭容器内,800%C时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
(1)达平衡的时间是3s,理由是3s后NO物质的量不再发生变化.
(2)图中表示NO2的变化的曲线是b,用O2表示从0=2s内该反应的平均速率v(O2)=0.0015mol/(L•s).
(3)能说明该反应一定达到平衡状态的是bd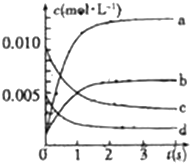
a.v(NO2)=2v(O2)
b.容器内颜色保持不变
c.2V逆 (NO)=v正(O2)
d.容器内压强保持不变
(4)能增大该反应的反应速率是bcd
a.及时分离出NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂.
0 169938 169946 169952 169956 169962 169964 169968 169974 169976 169982 169988 169992 169994 169998 170004 170006 170012 170016 170018 170022 170024 170028 170030 170032 170033 170034 170036 170037 170038 170040 170042 170046 170048 170052 170054 170058 170064 170066 170072 170076 170078 170082 170088 170094 170096 170102 170106 170108 170114 170118 170124 170132 203614
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.01 | 0.008 | 0.007 | 0.007 | 0.007 |
(2)图中表示NO2的变化的曲线是b,用O2表示从0=2s内该反应的平均速率v(O2)=0.0015mol/(L•s).
(3)能说明该反应一定达到平衡状态的是bd

a.v(NO2)=2v(O2)
b.容器内颜色保持不变
c.2V逆 (NO)=v正(O2)
d.容器内压强保持不变
(4)能增大该反应的反应速率是bcd
a.及时分离出NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂.
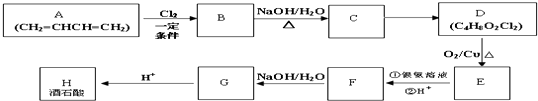
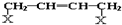
 和
和 

 _
_ 能源与资源是现代社会发展的重要支柱.
能源与资源是现代社会发展的重要支柱.