6.铜锌原电池(如图)工作时,下列叙述正确的是( )
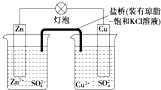

| A. | 正极反应为:Zn-2e-═Zn2+ | B. | 盐桥中的K+移向ZnSO4溶液 | ||
| C. | 在外电路中,电流从负极流向正极 | D. | 电池反应为:Zn+Cu2+═Zn2++Cu |
5.可逆反应N2+3H2?2NH3的正、逆反应速率可用各反应物或生成物浓度的变化来表示.下列各关系中能说明反应已达到平衡状态的是( )
| A. | 3υ正(N2)=υ正(H2) | B. | υ正(N2)=υ逆(NH3) | C. | υ正(N2)=3υ逆(H2) | D. | 2υ正(H2)=3υ逆(NH3) |
4.在一密闭容器中,反应aA(g)═bB(g)达平衡(I).保持温度不变,将容器体积增加一倍,当达到新的平衡(II),实验测得cB(II):cB(I)B=2:5,则下列说法正确的是( )
| A. | 平衡向正反应方向移动 | B. | 物质A的转化率降低 | ||
| C. | 物质B的质量分数增加 | D. | a<b |
3.四种短周期元素在周期表中的相对位置如图所示,下列说法正确的是( )
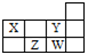

| A. | 1个37W原子中,质子数比中子数多3个 | |
| B. | Y和W处于同一主族,具有相同的最高价态 | |
| C. | Z形成简单阴离子半径小于W形成简单阴离子半径 | |
| D. | X与Y、Z与W每组两种元素间均可形成电子数相等的氢化物 |
2.下列关于Fe2(SO4)3的叙述正确的是(设NA为阿伏加德罗常数的数值)( )
| A. | 1mol/L的 Fe2(SO4)3溶液中含有2NA个Fe3+(不考虑水解) | |
| B. | 1mol的 Fe2(SO4)3和S2-反应可转移2NA个电子 | |
| C. | 在该溶液中,K+、NH4+、I-、SO42-可以大量共存 | |
| D. | 与Cu反应的离子方程式为:Fe3++Cu═Fe2++Cu2+ |
19.研究人员研制出一种锂水电池,可作为鱼雷和潜艇的储备电源.该电池以金属锂和钢板为电极材料,以LiOH为电解质,使用时加入水即可放电.关于该电池的下列说法不正确的是( )
0 169756 169764 169770 169774 169780 169782 169786 169792 169794 169800 169806 169810 169812 169816 169822 169824 169830 169834 169836 169840 169842 169846 169848 169850 169851 169852 169854 169855 169856 169858 169860 169864 169866 169870 169872 169876 169882 169884 169890 169894 169896 169900 169906 169912 169914 169920 169924 169926 169932 169936 169942 169950 203614
| A. | 放电时OH-向正极移动 | B. | 放电时正极上有氢气生成 | ||
| C. | 水既是氧化剂又是溶剂 | D. | 总反应为:2Li+2H2O═2LiOH+H2↑ |

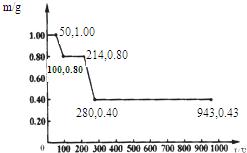 (1)用甲烷制氢是一种廉价的制氢方法.有关的热化学方程式如下:
(1)用甲烷制氢是一种廉价的制氢方法.有关的热化学方程式如下: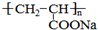 )是一种强吸水树脂.由某烃A合成聚丙烯酸钠的流程如图:
)是一种强吸水树脂.由某烃A合成聚丙烯酸钠的流程如图: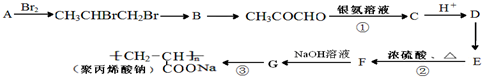
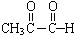 +2Ag(NH3)2OH$\stackrel{△}{→}$
+2Ag(NH3)2OH$\stackrel{△}{→}$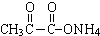 +3NH3+2Ag↓+H2O.
+3NH3+2Ag↓+H2O.