题目内容
19.研究人员研制出一种锂水电池,可作为鱼雷和潜艇的储备电源.该电池以金属锂和钢板为电极材料,以LiOH为电解质,使用时加入水即可放电.关于该电池的下列说法不正确的是( )| A. | 放电时OH-向正极移动 | B. | 放电时正极上有氢气生成 | ||
| C. | 水既是氧化剂又是溶剂 | D. | 总反应为:2Li+2H2O═2LiOH+H2↑ |
分析 锂水电池中,自发的氧化还原反应是金属锂和水之间反应生成氢氧化锂和氢气的过程,根据原电池的工作原理以及电极反应特点和规律来回答.
解答 解:A、原电池中,阴离子移向原电池的负极,即放电时OH-向负极移动,故A错误;
B、放电时正极上是水中的氢离子得电子,所以会有氢气生成,故B正确;
C、金属锂和水之间反应生成氢氧化锂和氢气,该反应中,水是氧化剂,在电池中还可以担当溶剂,故C正确;
D、锂水电池中,自发的氧化还原反应是金属锂和水之间反应生成氢氧化锂和氢气,即总反应为:2Li+2H2O=2LiOH+H2↑,故D正确.
故选A.
点评 本题考查电化学的热点-锂离子电池,根据总反应式判断出正负极和阴阳极的反应,从化合价变化的角度分析.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.与图象有关的叙述,正确的是( )
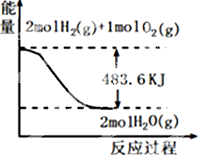

| A. | 表示1mol H2(g)完全燃烧生成水蒸气吸收241.8 kJ热量 | |
| B. | 表示的热化学方程式为:H2(g)+$\frac{1}{2}$ O2(g)=H2O(g)△H=-241.8 kJ•mol-1 | |
| C. | H2O(g)的能量低于H2(g)和O2(g)的能量之和 | |
| D. | 表示2 mol H2(g)所具有的能量一定比2 mol气态水所具有的能量多483.6 kJ |
7.化学与生活密切相关.据了解同学们的家中常备如下生活用品:碘酒、食盐、食醋、84消毒液(内含NaClO),利用上述用品你不能完成的任务是( )
| A. | 除去保温瓶中的水垢 | B. | 检验自来水中是否含有Cl- | ||
| C. | 检验买来的奶粉中是否加有淀粉 | D. | 洗去白色衣服上的番茄汁 |
14.下列关于${\;}_{6}^{12}$C、${\;}_{6}^{13}$C、${\;}_{6}^{14}$C的说法正确的是( )
| A. | 它们的化学性质完全不同 | B. | 它们是碳元素的三种同位素 | ||
| C. | 它们是碳元素的三种单质 | D. | 它们是碳元素的同素异形体 |
4.在一密闭容器中,反应aA(g)═bB(g)达平衡(I).保持温度不变,将容器体积增加一倍,当达到新的平衡(II),实验测得cB(II):cB(I)B=2:5,则下列说法正确的是( )
| A. | 平衡向正反应方向移动 | B. | 物质A的转化率降低 | ||
| C. | 物质B的质量分数增加 | D. | a<b |
11.在一个固定体积的密闭容器中加入2molA,发生可逆反应:2A(g)?2B(g)+C(g).该反应达到平衡的标志是( )
| A. | 容器内压强是开始时的1.5倍 | |
| B. | 容器内A、B、C物质的量浓度之比为2:2:1 | |
| C. | 单位时间消耗0.2 mol A 同时生成0.1 mol C | |
| D. | 容器内各物质的浓度不随时间变化 |
9.下列实验操作不能达到预期目的是( )
| 实验目的 | 操作 | |
| A | 比较水和乙醇中羟基氢的活泼性 | 用金属钠分别与水和乙醇反应 |
| B | 证明HOCH2CHO中含有醛基 | 滴加酸性KMnO4溶液,看紫红色是否褪去 |
| C | 确定磷、砷两元素非金属性的强弱 | 测定同温同浓度的Na3PO4和Na3AsO4水溶液的pH |
| D | 除去苯中混有的苯酚 | 向混合液中加入NaOH溶液,充分反应后,分液 |
| A. | A | B. | B | C. | C | D. | D |
 .
.
 .
.