3.下列有关物品的用途或性质说法错误的是( )
| A. | 纯净的SiO2是现代光学和光纤制品的基本原料,制造光导纤维离不开它 | |
| B. | 硅是良好的半导体材料,也是信息技术的关键材料,制造光电池离不开它 | |
| C. | Cl2的水溶液具有酸性,Cl2通入紫色石蕊溶液中,溶液只变红 | |
| D. | 用坩埚钳夹住一小块铝箔在酒精灯上加热至融化,但融化的铝并不滴落,原因是表面生成了致密的氧化物薄膜 |
2.下列各组物质互为同分异构体的是( )
| A. | 苯甲醇和甲基苯苯酚 | B. | 乙醇和乙醚 | ||
| C. | 丁二烯和2-丁烯 | D. | 乙醇和乙二醇 |
1.下列反应中,硫酸不作氧化剂的是( )
| A. | 2HBr+H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$Br2+SO2↑+2H2O | |
| B. | Ca3(PO4)2+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$2CaSO4+Ca(H2PO4)2 | |
| C. | 2Al+3H2SO4═Al2(SO4)3+3H2↑ | |
| D. | 2KMnO4+5H2S+3H2SO4═K2SO4+2MnSO4+5S↓+8H2O |
20.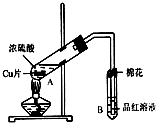 某研究小组用如图所示装置进行铜与浓硫酸反应的实验研究.
某研究小组用如图所示装置进行铜与浓硫酸反应的实验研究.
(1)写出试管B中的实验现象品红溶液褪色.
(2)写出A中反应的化学方程式Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O
(3)B试管口的棉花应沾有的试剂是NaOH.
(4)反应后有铜剩余,若不补充浓硫酸,要使铜片溶解,继续向A试管中加入H2O2,发现铜片又溶解,反应的离子方程式为:Cu+H2O2+2H+=Cu2++2H2O.或者可以加Fe2O3、NaNO3(填写两种属于不同类别物质的化学式),也能使铜片溶解.
(5)小组成员向反应后的溶液中加入足量的氧化铜,使剩余的硫酸全部转化为硫酸铜,过滤后,将滤液加热浓缩,冷却结晶制得硫酸铜晶体(CuSO4•xH2O).小组成员采用加热法测定该晶体里结晶水x的值.
下面是其中一次实验的数据:
根据上表数据计算判断x的实侧值比理论值(x=5)偏小(填“偏大”、“偏小”),这次实验中产生误差的原因可能是AD(填序号)
A.硫酸铜晶体中含有不挥发的杂质 B.实验前晶体表面有湿存水
C.加热时有晶体飞溅出去 D.加热失水后露置在空气中冷却.
 某研究小组用如图所示装置进行铜与浓硫酸反应的实验研究.
某研究小组用如图所示装置进行铜与浓硫酸反应的实验研究.(1)写出试管B中的实验现象品红溶液褪色.
(2)写出A中反应的化学方程式Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O
(3)B试管口的棉花应沾有的试剂是NaOH.
(4)反应后有铜剩余,若不补充浓硫酸,要使铜片溶解,继续向A试管中加入H2O2,发现铜片又溶解,反应的离子方程式为:Cu+H2O2+2H+=Cu2++2H2O.或者可以加Fe2O3、NaNO3(填写两种属于不同类别物质的化学式),也能使铜片溶解.
(5)小组成员向反应后的溶液中加入足量的氧化铜,使剩余的硫酸全部转化为硫酸铜,过滤后,将滤液加热浓缩,冷却结晶制得硫酸铜晶体(CuSO4•xH2O).小组成员采用加热法测定该晶体里结晶水x的值.
下面是其中一次实验的数据:
| 坩埚质量 | 坩埚与晶体的总质量 | 加热后坩埚与固体总质量 |
| 11.7g | 22.7g | 18.9g |
A.硫酸铜晶体中含有不挥发的杂质 B.实验前晶体表面有湿存水
C.加热时有晶体飞溅出去 D.加热失水后露置在空气中冷却.
19.下列有关垃圾处理的方法不正确的是( )
| A. | 垃圾处理常用的方法是卫生填埋、焚烧、堆肥 | |
| B. | 将垃圾分类回收是垃圾处理的发展方向 | |
| C. | 填埋垃圾不需处理,只深埋即可 | |
| D. | 焚烧垃圾产生大量污染空气的物质,故不易采用此方法 |
18.已知以下化学键的键能:H-H 436kJ/mol,Cl-Cl 243kJ/mol,H-Cl 431kJ/mol.下列叙述正确的是( )
| A. | Cl-Cl键比H-H键的键能小,是因为Cl原子比H原子的非金属性强 | |
| B. | H2(g)与Cl2(g)反应生成2 molHCl(g),反应的△H=183 kJ/mol | |
| C. | H2(g)与Cl2(g)反应生成2 molHCl(g),反应的△H=-183 kJ/mol | |
| D. | H2(g)与Cl2(g)反应生成1 molHCl(g),反应的△H=-183 kJ/mol |
17.具有如下电子排布的原子,其相应元素一定属于同一主族的是( )
| A. | 最外层电子排布为1s2的原子和最外层电子排布为2s2的原子 | |
| B. | 2p轨道上有2个未成对电子的原子和3p轨道上有2个未成对电子的原子 | |
| C. | 3p轨道上只有1个空轨道的原子和4p轨道上只有1个空轨道的原子 | |
| D. | 电子排布式为1s2的原子和外围电子排布式为2s22p6的原子 |
16.下列实施中,能说明HNO2是弱电解质的是( )
| A. | 用HNO2溶液做导电性试验,灯光较暗 | |
| B. | HNO2是共价化合物 | |
| C. | HNO2溶液不与氯化钠反应 | |
| D. | 常温下,0.1mol.L-1HNO2溶液的pH为2.15 |
15.下列物质中,物质的量最多的是( )
| A. | 4℃时40ml水 | B. | 0.8mol硫酸 | ||
| C. | 9.03×1022个氧分子 | D. | 54g铝 |
14.下列除杂方案正确的是(括号内为除杂试剂)( )
0 169473 169481 169487 169491 169497 169499 169503 169509 169511 169517 169523 169527 169529 169533 169539 169541 169547 169551 169553 169557 169559 169563 169565 169567 169568 169569 169571 169572 169573 169575 169577 169581 169583 169587 169589 169593 169599 169601 169607 169611 169613 169617 169623 169629 169631 169637 169641 169643 169649 169653 169659 169667 203614
| A. | NaOH溶液中混有Ba(OH)2 (CuSO4) | B. | Cu(NO3)2中混有AgNO3 (Cu粉) | ||
| C. | CO中混有CO2(炽热的炭) | D. | CO2中混有HCl气体 (NaOH溶液) |