8.下列关于18O示踪原子的踪迹判断错误的是( )
| A. | 2KMnO4+5H218O2+3H2SO4═K2SO4+2MnSO4+518O2+8H2O | |
| B. | CH3COOH+H18OC2H5$→_{△}^{浓硫酸}$CH3CO18OC2H5+H2O | |
| C. | CH3CH218OH+CuO$\stackrel{△}{→}$CH3CHO+Cu+H218O | |
| D. | C6H518OH+NaOH→C6H518ONa+H2O |
6.下列变化过程中,同时有离子键、极性键、非极性键的断裂和形成的是( )
| A. | 2NH4HCO3=2NH3+CO2+2H2O | B. | 2NaOH+Cl2=NaCl+NaClO+H2O | ||
| C. | 2Na2O2+2CO2=2Na2CO3+O2 | D. | H2+Cl2=2HCl |
5.下列说法正确的( )
| A. | 水结冰后体积膨胀的原因是由于水分子内存在氢键造成的 | |
| B. | F2、Cl2、Br2、I2由于组成结构相似,相对分子质量逐渐增大,分子间作用力逐渐增大,所以熔沸点逐渐升高 | |
| C. | 根据元素周期表的知识判断51Sb是一种可以作为半导体材料的非金属元素 | |
| D. | 碳元素有多种核素,如12C、13C、14C、C60它们互为同位素 |
4.下列说法正确的是( )
| A. | 所有物质中均存在化学键 | |
| B. | 非金属元素间形成的化合物一定是共价化合物 | |
| C. | 离子化合物中可能含非极性共价键 | |
| D. | 有共价键的化合物一定是共价化合物 |
3.下列氢化物中,按稳定性由强到弱的顺序排列的是( )
| A. | HI、HBr、HCl、HF | B. | HCl、PH3、H2S、SiH4 | ||
| C. | H2O、H2S、HCl、HBr | D. | HF、H2O、NH3、CH4 |
2.下列叙述中,不属于氮的固定的方法是( )
| A. | 根瘤菌把氮气变为硝酸盐 | B. | 氮气和氢气合成氨 | ||
| C. | 从液态空气中分离氮气 | D. | 氮气和氧气合成一氧化氮 |
1.A、B两种烃,含碳的质量分数相同,下列关于A和B的叙述中,正确的是( )
| A. | 烃A和B的实验式相同 | |
| B. | 烃A和B一定是同分异构体 | |
| C. | 烃A和B不可能是同系物 | |
| D. | 烃A和B各取1 mol,完全燃烧时生成CO2的质量一定相等 |
20.将质量相等的铁片和铜片插入氯化钠溶液中,铜片与电源的正极相连,铁片与电源的负极相连,以I=1A的恒定电流强度进行电解,下列有关说法正确的是( )
| A. | 阳极上产生能够使湿润淀粉碘化钾试纸变蓝的气体 | |
| B. | 电解一段时间后,电解池的温度升高10℃,此时铁片上析出气体的速率加快 | |
| C. | 电解时钠离子向铜片电极方向移动 | |
| D. | 电解一段时间后溶液中会出现蓝色沉淀,总反应为:Cu+2H2O$\frac{\underline{\;通电\;}}{\;}$Cu(OH)2↓+H2↑ |
19.某同学按如图所示的装置进行试验.A、B为两种常见金属,它们的硫酸盐可溶于水.当K闭合时,在交换膜处SO42-从右向左移动.下列分析错误的是( )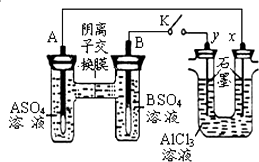
0 169051 169059 169065 169069 169075 169077 169081 169087 169089 169095 169101 169105 169107 169111 169117 169119 169125 169129 169131 169135 169137 169141 169143 169145 169146 169147 169149 169150 169151 169153 169155 169159 169161 169165 169167 169171 169177 169179 169185 169189 169191 169195 169201 169207 169209 169215 169219 169221 169227 169231 169237 169245 203614

| A. | 金属活动性A强于B | |
| B. | 反应初期,y电极的电极反应为:2Cl--2e-=Cl2↑ | |
| C. | 反应初期,x电极周围出现白色沉淀,后来电极附近沉淀溶解 | |
| D. | 电解一段时间后将AlCl3溶液倒入烧杯并搅拌可得到偏铝酸盐溶液 |
 铁(26Fe)是地球上分布最广的金属之一,约占地壳质量的5.1%,居元素分布序列中的第四位,仅次于O、Si和Al.请结合所学知识回答下列问题:
铁(26Fe)是地球上分布最广的金属之一,约占地壳质量的5.1%,居元素分布序列中的第四位,仅次于O、Si和Al.请结合所学知识回答下列问题: