19.钾元素的核素${\;}_{19}^{39}$K中,中子数与质子数之差为( )
| A. | 1 | B. | 19 | C. | 20 | D. | 39 |
18.X、Y、Z、R是中学化学常见的4种主族元素,原子序数依次增大.Y在周期表前20号元素中原子半径最大;X、Y可以形成YX型离子化合物,且离子核外电子数相等;Z、R可以形成共价分子RZ,两原子最外层均达到8电子结构,R显+1价.回答下列问题:
(1)Y的单质与水反应的化学方程式是2K+2H2O=2KOH+H2↑.
(2)R元素在周期表中位于第戊周期ⅦA族.
(3)根据原子结构理论预测:按X、Z、R顺序,原子核外电子层数依次递增,原子半径逐渐增大,得电子能力逐渐减弱,非金属性逐渐减弱,所以X、Z、R三种元素的非金属性由强及弱的顺序是Cl>Br>I(填写元素符号).
(4)为了证明这一结论,甲同学设计了如下实验:
乙同学分析后认为:用甲同学的实验设计比较R、Z的非金属性不够严谨,你认为他的理由可能是实验I结束后Cl2可能剩余.
丙同学为了比较R、Z的非金属性,在甲同学方案的基础上补充设计了如下实验:
向Y、Z、R简单离子的混合溶液中,加入少许CCl4,滴加少量X单质的水溶液,振荡,观察CCl4层的颜色.
丙同学的设计依据是在含有I-、Br-离子溶液中加入少量Cl2,还原性强的物质先被氧化.
(1)Y的单质与水反应的化学方程式是2K+2H2O=2KOH+H2↑.
(2)R元素在周期表中位于第戊周期ⅦA族.
(3)根据原子结构理论预测:按X、Z、R顺序,原子核外电子层数依次递增,原子半径逐渐增大,得电子能力逐渐减弱,非金属性逐渐减弱,所以X、Z、R三种元素的非金属性由强及弱的顺序是Cl>Br>I(填写元素符号).
(4)为了证明这一结论,甲同学设计了如下实验:
| 序号 | 实验内容 | 实验现象 | 用离子方程式解释现象 |
| 实验Ⅰ | 向YZ的水溶液中,加入少许CCl4,逐滴滴加X单质的水溶液,振荡. | CCl4层颜色变成橙红色 | 发生反应的离子方程式是Cl2+2Br-=2Cl-+Br2. |
| 实验Ⅱ | 向上述溶液中加入少量YR的水溶液,振荡. | CCl4层颜色变成紫红色 | 发生反应的离子方程式是Br2+2I-=2Br-+I 2. |
丙同学为了比较R、Z的非金属性,在甲同学方案的基础上补充设计了如下实验:
向Y、Z、R简单离子的混合溶液中,加入少许CCl4,滴加少量X单质的水溶液,振荡,观察CCl4层的颜色.
丙同学的设计依据是在含有I-、Br-离子溶液中加入少量Cl2,还原性强的物质先被氧化.
17.四种短周期元素W、X、Y、Z的原子序数依次增大,其原子的最外层电子数之和为19,W和X元素原子内质子数之比为1:2,X2+和Z-离子的电子数之差为8.下列说法不正确的是( )
| A. | 与W相邻的同主族元素可制成重要的半导体材料 | |
| B. | 元素的原子半径从大到小的顺序是X、Y、Z | |
| C. | WZ4分子中W、Z 原子最外层均达到8电子结构 | |
| D. | W、Y、Z元素最高价氧化物对应的水化物中酸性最强的是H2YO4 |
16.下列叙述正确的是( )
| A. | NaHCO3与石灰水反应当n(NaHCO3):n[Ca(OH)2]=1:1时HCO3-完全转化为CaCO3 | |
| B. | CO2通入石灰水中,当n(CO2):n[Ca(OH)2]=1:1时,能得到澄清溶液 | |
| C. | AlCl3溶液与烧碱溶液反应,当n(OH-):n(Al3+)=1:1时铝元素以AlO2-形式存在 | |
| D. | Cl2与FeBr2溶液反应,当n(Cl2):n(FeBr2)=1:1时,溶液中存在Fe2+ |
15.依据物质的相关数据,可以推断物质的结构和性质.下列推断不合理的是( )
| A. | 依据原子序数,推断该元素原子的核外电子数 | |
| B. | 依据相对分子质量,推断物质常温下的溶解度 | |
| C. | 依据气体的摩尔质量,推断相同状况下不同气体密度的大小 | |
| D. | 依据元素原子的最外层电子数,推测其可能的最高正价和最低化合价 |
12.下列说法错误的是( )
| A. | Li、Be、B原子最外层电子数依次增多 | |
| B. | P、S、Cl最高正化合价依次升高 | |
| C. | F-、Cl-、Br-还原性依次减弱 | |
| D. | Na、K、Rb的金属性依次增强 |
11.几种短周期元素的原子半径及主要化合价如下表:
下列叙述正确的是( )
| 元素代号 | X | Y | Z | W |
| 原子半径/pm | 160 | 143 | 70 | 66 |
| 主要化合价 | +2 | +3 | +5、+3、-3 | -2 |
| A. | 元素的金属性 X<Y | |
| B. | 一定条件下,Z单质与W的常见单质直接生成ZW2 | |
| C. | Y的最高价氧化物对应的水化物能溶于稀氨水 | |
| D. | 一定条件下,W单质可以将Z单质从其氢化物中置换出来 |
10.下列反应的离子方程式正确的是( )
0 168141 168149 168155 168159 168165 168167 168171 168177 168179 168185 168191 168195 168197 168201 168207 168209 168215 168219 168221 168225 168227 168231 168233 168235 168236 168237 168239 168240 168241 168243 168245 168249 168251 168255 168257 168261 168267 168269 168275 168279 168281 168285 168291 168297 168299 168305 168309 168311 168317 168321 168327 168335 203614
| A. | 金属铝溶于稀硝酸中:2Al+6H+=2A13++3H2↑ | |
| B. | 碳酸钡与稀硫酸反应:Ba2++SO42-=BaSO4↓ | |
| C. | 碳酸氢钠溶液与少量盐酸反应:CO32-+2 H+=H2O+CO2↑ | |
| D. | 碳酸钠溶液缓慢滴入少量稀盐酸:CO32-+H+=HCO3- |
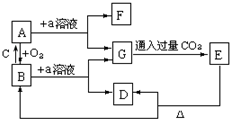 A是一种常见的半导体材料,E是一种白色沉淀.存在下列物质转化关系,据此填写下列空白.
A是一种常见的半导体材料,E是一种白色沉淀.存在下列物质转化关系,据此填写下列空白.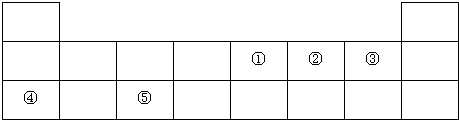
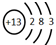 .
.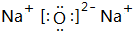 、
、 .(写两个)
.(写两个)