题目内容
16.下列叙述正确的是( )| A. | NaHCO3与石灰水反应当n(NaHCO3):n[Ca(OH)2]=1:1时HCO3-完全转化为CaCO3 | |
| B. | CO2通入石灰水中,当n(CO2):n[Ca(OH)2]=1:1时,能得到澄清溶液 | |
| C. | AlCl3溶液与烧碱溶液反应,当n(OH-):n(Al3+)=1:1时铝元素以AlO2-形式存在 | |
| D. | Cl2与FeBr2溶液反应,当n(Cl2):n(FeBr2)=1:1时,溶液中存在Fe2+ |
分析 A.发生OH-+HCO3-+Ca2+=CaCO3↓+H2O;
B.发生CO2+2OH-+Ca2+=CaCO3↓+H2O;
C.当n(OH-):n(Al3+)=1:1时,碱不足发生3OH++Al3+=Al(OH)3↓;
D.当n(Cl2):n(FeBr2)=1:1时,由电子守恒可知,亚铁离子全部被氧化,溴离子一半被氧化.
解答 解:A.发生OH-+HCO3-+Ca2+=CaCO3↓+H2O,则n(NaHCO3):n[Ca(OH)2]=1:1时HCO3-完全转化为CaCO3,故A正确;
B.发生CO2+2OH-+Ca2+=CaCO3↓+H2O,则当n(CO2):n[Ca(OH)2]=1:1时,溶液变浑浊,生成白色沉淀,故B错误;
C.当n(OH-):n(Al3+)=1:1时,碱不足发生3OH++Al3+=Al(OH)3↓,则铝元素以沉淀形式存在,故C错误;
D.当n(Cl2):n(FeBr2)=1:1时,由电子守恒可知,亚铁离子全部被氧化,溴离子一半被氧化,则溶液中不存在Fe2+,故D错误;
故选A.
点评 本题考查离子反应及计算,为高频考点,把握发生的离子反应为解答的关键,侧重与量有关的离子反应、氧化还原反应先后顺序的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.A、B、C三种短周期元素,A、B在同一周期,A、C的最低价离子分别为A2-、C-,离子半径A2-大于C-,B2+和 C-具有相同的电子层结构.下列判断正确的是( )
| A. | 原子序数由大到小的顺序是C>A>B | |
| B. | 原子最外层电子数由多到少的顺序是B>A>C | |
| C. | 离子半径由大到小的顺序是C->B2+>A2- | |
| D. | 原子半径由大到小的顺序是B>A>C |
7.下列实验一定能证明SO2 存在的是( )
①能使澄清石灰水变浑②能使蓝色石蕊试纸变红③能使品红溶液褪色④通入溴水中能使溴水褪色,在滴加硝酸钡溶液,有白色沉淀生成⑤先通入足量的NaOH溶液,再滴入氯化钡溶液有白色沉淀生成,该沉淀溶于稀盐酸.
①能使澄清石灰水变浑②能使蓝色石蕊试纸变红③能使品红溶液褪色④通入溴水中能使溴水褪色,在滴加硝酸钡溶液,有白色沉淀生成⑤先通入足量的NaOH溶液,再滴入氯化钡溶液有白色沉淀生成,该沉淀溶于稀盐酸.
| A. | 都能证明 | B. | 都不能证明 | C. | ③④⑤都能证明 | D. | 只有④能证明 |
4.下表为元素周期表的一部分,参照元素在表中的位置,请用化学用语回答下列问题:
(1)⑦的最低负价是-2;⑧的最高价含氧酸的化学式为HClO4.
(2)①和⑦两种元素的原子按1:1组成的常见化合物的电子式为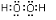 .
.
(3)③、④、⑦、⑧的简单离子半径由大到小的顺序为r (Cl-)>r (O2-)>r (Mg2+)>r (Al3+).
(4)⑤、⑥的单质中更易与①的单质反应的是N2,原因是氮的非金属性比碳强,因而其单质更易与氢气反应.
(5)②、④的最高价氧化物的水化物之间发生反应的离子方程式:Al(OH)3+OH-=AlO2-+2H2O.
(6)用电子式表示③和⑨组成的化合物的形成过程 .
.
(7)海带中含有⑩元素,海带灰中含有该元素的简单阴离子,在硫酸酸化下,可用双氧水将其氧化为单质.写出该反应的离子方程式H2O2+2I-+2H+=I2+2H2O.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | |||||||
| 2 | ⑤ | ⑥ | ⑦ | |||||
| 3 | ② | ③ | ④ | ⑧ | ||||
| 4 | ⑨ | |||||||
| 5 | ⑩ |
(2)①和⑦两种元素的原子按1:1组成的常见化合物的电子式为
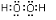 .
.(3)③、④、⑦、⑧的简单离子半径由大到小的顺序为r (Cl-)>r (O2-)>r (Mg2+)>r (Al3+).
(4)⑤、⑥的单质中更易与①的单质反应的是N2,原因是氮的非金属性比碳强,因而其单质更易与氢气反应.
(5)②、④的最高价氧化物的水化物之间发生反应的离子方程式:Al(OH)3+OH-=AlO2-+2H2O.
(6)用电子式表示③和⑨组成的化合物的形成过程
 .
.(7)海带中含有⑩元素,海带灰中含有该元素的简单阴离子,在硫酸酸化下,可用双氧水将其氧化为单质.写出该反应的离子方程式H2O2+2I-+2H+=I2+2H2O.
11.几种短周期元素的原子半径及主要化合价如下表:
下列叙述正确的是( )
| 元素代号 | X | Y | Z | W |
| 原子半径/pm | 160 | 143 | 70 | 66 |
| 主要化合价 | +2 | +3 | +5、+3、-3 | -2 |
| A. | 元素的金属性 X<Y | |
| B. | 一定条件下,Z单质与W的常见单质直接生成ZW2 | |
| C. | Y的最高价氧化物对应的水化物能溶于稀氨水 | |
| D. | 一定条件下,W单质可以将Z单质从其氢化物中置换出来 |
1.下列反应中,反应物总能量低于生成物总能量的是( )
| A. | CaO与H2O反应 | B. | CH4在O2中燃烧 | ||
| C. | NaOH溶液与H2SO4溶液反应 | D. | Ba(OH)2•8H2O晶体与NH4Cl晶体反应 |
8.根据等电子原理,由短周期元素组成的粒子,只要其原子数相同,各原子的最外层电子数之和也相同,可互称为等电子体.以下各组粒子不能互称为等电子体的是( )
| A. | CO和N2 | B. | O3和SO2 | C. | CO2和N2O | D. | N2H4和C2H4 |
5.元素X、Y、Z均为短周期元素且原子序数之和为35,X、Y在同一周期,X+与Z2-具有相同的核外电子层结构.下列推测不正确的是( )
| A. | 三种元素的原子序数 Y>X>Z | |
| B. | 三种元素的原子半径 X>Y>Z | |
| C. | 同周期元素中X的金属性最强 | |
| D. | 同周期元素中Z的最高价氧化物的水化物酸性最强 |
6.下列各化合物的命名中正确的是( )
| A. | CH2=CH-CH=CH2 1,3-二丁烯 | B. | CH3-O-CH3乙醚 | ||
| C. |  | D. |  2-甲基丁烷 2-甲基丁烷 |