9.下列说法中,不正确的是( )
| A. | HCl稳定性比HI好 | |
| B. | CH4的沸点比NH3的沸点低 | |
| C. | Mg失电子能力比Ca弱 | |
| D. | NaCl与NH4Cl含有的化学键类型完全相同 |
8.下列关于物质分类中不正确的是( )
| A. | 纯碱属于碱 | B. | 食盐属于盐 | ||
| C. | 干冰属于分子晶体 | D. | 含有离子键的物质属于离子化合物 |
7.对现代元素周期表的提出做出最重要贡献的科学家是( )
| A. | 门捷列夫(俄国) | B. | 纽兰兹(英国) | C. | 迈耶尔(德国) | D. | 拉瓦锡(法国) |
5.海水资源的利用具有广阔前景.海水中主要离子的含量如下:
利用海水可以提取溴和镁,提取过程如下:
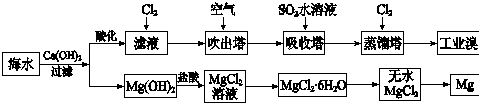
(1)提取溴的过程中,经过2次Br-→Br2转化的目的是对溴元素进行富集,吸收塔中发生反应的化学方程式是SO2+Br2+2H2O=4H++2Br-+SO42-.
(2)Mg(OH)2中加盐酸的反应的离子方程式是Mg(OH)2+2H+=Mg2++2H2O.
(3)写出无水MgCl2得到Mg的化学方程式MgCl2(熔融)$\frac{\underline{\;通电\;}}{\;}$Mg+Cl2↑.
(4)依据上述流程,若将10m3海水中的溴元素转化为工业溴,至少需要标准状况下Cl2的体积为179.2L(忽略Cl2溶解).
| 成分 | 含量/(mg L-1) | 成分 | 含量/(mg L-1) |
| Cl- | 18980 | Ca2+ | 400 |
| Na+ | 10560 | HCO3- | 142 |
| SO42- | 2560 | Br- | 64 |
| Mg2+ | 1272 |

(1)提取溴的过程中,经过2次Br-→Br2转化的目的是对溴元素进行富集,吸收塔中发生反应的化学方程式是SO2+Br2+2H2O=4H++2Br-+SO42-.
(2)Mg(OH)2中加盐酸的反应的离子方程式是Mg(OH)2+2H+=Mg2++2H2O.
(3)写出无水MgCl2得到Mg的化学方程式MgCl2(熔融)$\frac{\underline{\;通电\;}}{\;}$Mg+Cl2↑.
(4)依据上述流程,若将10m3海水中的溴元素转化为工业溴,至少需要标准状况下Cl2的体积为179.2L(忽略Cl2溶解).
4.下表为元素周期表的一部分,参照元素在表中的位置,请用化学用语回答下列问题:
(1)⑦的最低负价是-2;⑧的最高价含氧酸的化学式为HClO4.
(2)①和⑦两种元素的原子按1:1组成的常见化合物的电子式为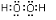 .
.
(3)③、④、⑦、⑧的简单离子半径由大到小的顺序为r (Cl-)>r (O2-)>r (Mg2+)>r (Al3+).
(4)⑤、⑥的单质中更易与①的单质反应的是N2,原因是氮的非金属性比碳强,因而其单质更易与氢气反应.
(5)②、④的最高价氧化物的水化物之间发生反应的离子方程式:Al(OH)3+OH-=AlO2-+2H2O.
(6)用电子式表示③和⑨组成的化合物的形成过程 .
.
(7)海带中含有⑩元素,海带灰中含有该元素的简单阴离子,在硫酸酸化下,可用双氧水将其氧化为单质.写出该反应的离子方程式H2O2+2I-+2H+=I2+2H2O.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | |||||||
| 2 | ⑤ | ⑥ | ⑦ | |||||
| 3 | ② | ③ | ④ | ⑧ | ||||
| 4 | ⑨ | |||||||
| 5 | ⑩ |
(2)①和⑦两种元素的原子按1:1组成的常见化合物的电子式为
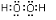 .
.(3)③、④、⑦、⑧的简单离子半径由大到小的顺序为r (Cl-)>r (O2-)>r (Mg2+)>r (Al3+).
(4)⑤、⑥的单质中更易与①的单质反应的是N2,原因是氮的非金属性比碳强,因而其单质更易与氢气反应.
(5)②、④的最高价氧化物的水化物之间发生反应的离子方程式:Al(OH)3+OH-=AlO2-+2H2O.
(6)用电子式表示③和⑨组成的化合物的形成过程
 .
.(7)海带中含有⑩元素,海带灰中含有该元素的简单阴离子,在硫酸酸化下,可用双氧水将其氧化为单质.写出该反应的离子方程式H2O2+2I-+2H+=I2+2H2O.
3.如图是可逆反应X2+3Y2?2Z2 在反应过程中的反应速率(V)与时间(t)的关系曲线,下列叙述正确的是( )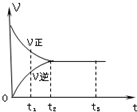

| A. | t1时,只有正反应继续进行 | B. | t2时,反应停止 | ||
| C. | t2-t3,反应不再是可逆反应 | D. | t2-t3,各物质的浓度不再发生变化 |
2. X、Y、Z、Q均为短周期元素,它们在周期表中相对位置如图所示.若X原子的最外层电子是内层电子数的2倍.下列说法中,正确的是( )
X、Y、Z、Q均为短周期元素,它们在周期表中相对位置如图所示.若X原子的最外层电子是内层电子数的2倍.下列说法中,正确的是( )
 X、Y、Z、Q均为短周期元素,它们在周期表中相对位置如图所示.若X原子的最外层电子是内层电子数的2倍.下列说法中,正确的是( )
X、Y、Z、Q均为短周期元素,它们在周期表中相对位置如图所示.若X原子的最外层电子是内层电子数的2倍.下列说法中,正确的是( )| A. | X与Q形成的化合物中含有共价键 | |
| B. | 最高价氧化物对应水化物的酸性:Q比Z弱 | |
| C. | 14X和14Y具有相同的质量数,互为同位素 | |
| D. | Q与O2反应生成的化合物中,Q元素显+6价 |
1.镁和盐酸反应太剧烈,为了减缓反应速率而又不减少产生氢气的量,在盐酸中可加入( )
| A. | NaCl溶液 | B. | NaNO3溶液 | C. | Na2CO3溶液 | D. | CuSO4溶液 |
20.下列化工生产原理错误的是( )
①可以用电解熔融的氯化铝的方法来制取金属铝
②可以用钠加入氯化镁饱和溶液中制取镁
③用热分解法冶炼铁
④湿法炼铜是用锌和硫酸铜溶液反应置换出铜.
0 168140 168148 168154 168158 168164 168166 168170 168176 168178 168184 168190 168194 168196 168200 168206 168208 168214 168218 168220 168224 168226 168230 168232 168234 168235 168236 168238 168239 168240 168242 168244 168248 168250 168254 168256 168260 168266 168268 168274 168278 168280 168284 168290 168296 168298 168304 168308 168310 168316 168320 168326 168334 203614
①可以用电解熔融的氯化铝的方法来制取金属铝
②可以用钠加入氯化镁饱和溶液中制取镁
③用热分解法冶炼铁
④湿法炼铜是用锌和硫酸铜溶液反应置换出铜.
| A. | ②③ | B. | ①③ | C. | ①②③ | D. | ①②③④ |