5.图是元素周期表的一部分,试用化学符号回答下列问题:
(1)在这些元素中,单质的化学性质最不活泼的是Ar(填具体元素符号),其原子结构示意图为 .
.
(2)在这些元素中,③的气态氢化物与⑧的气态氢化物反应的现象为冒白烟,产物的晶体类型为离子晶体.
(3)在这些元素形成的最高价氧化物的水化物中,碱性最强的化合物的电子式为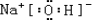 .
.
(4)⑥的单质与②、④形成的某种化合物反应的化学方程式为2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C.
(5)在⑦、⑧两种元素中,非金属性较强的是Cl(填具体元素符号),能证明这一结论的化学方程式为Cl2+H2S=2HCl+S.
(6)科学家借助元素周期表研究合成有特定性质的新物质,如在金属与非金属交界处寻找半导体材料.
| 族 周期 | IA | ⅡA | ⅢA | ⅣA | VA | ⅥA | VIIA | 0族 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
 .
.(2)在这些元素中,③的气态氢化物与⑧的气态氢化物反应的现象为冒白烟,产物的晶体类型为离子晶体.
(3)在这些元素形成的最高价氧化物的水化物中,碱性最强的化合物的电子式为
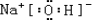 .
.(4)⑥的单质与②、④形成的某种化合物反应的化学方程式为2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C.
(5)在⑦、⑧两种元素中,非金属性较强的是Cl(填具体元素符号),能证明这一结论的化学方程式为Cl2+H2S=2HCl+S.
(6)科学家借助元素周期表研究合成有特定性质的新物质,如在金属与非金属交界处寻找半导体材料.
3.把a L含碳酸铵、氯化铵的溶液分成两等份,一份需用b mol烧碱刚好把氨全部赶出,另一份与氯化钡溶液反应时,消耗c mol氯化钡,由此可知原溶液中Cl-的物质的量浓度是(单位:mol•L-1)( )
| A. | $\frac{b-2c}{a}$ | B. | $\frac{b-2c}{2a}$ | C. | $\frac{2b-c}{a}$ | D. | $\frac{2b-4c}{a}$ |
2.如图是部分短周期元素化合价与原子序数的关系图,下列说法不正确的是( )

| A. | 离子半径:X>Y>Z | |
| B. | 气态氢化物的稳定性:R>W | |
| C. | WX3和水反应形成的化合物是离子化合物 | |
| D. | Y和Z两者最高价氧化物对应的水化物能相互反应 |
1.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 4.6 g NO2与N2O4的混合物中含有的N原子数为0.1NA | |
| B. | 常温常压下,22.4 L NO的分子数为0.1NA | |
| C. | 将0.3mol NO2溶于水,完全反应后,转移的电子数为0.2 NA | |
| D. | 1L0.1mol•L-1 氨水中含有的NH3分子数为0.1NA |
20.下列解释事实的方程式表达不正确的是( )
| A. | 氨水呈碱性:NH3•H2O=NH4++OH- | |
| B. | 碳酸氢钠治疗胃酸过多:HCO3-+H+=CO2↑+H2O | |
| C. | 久置的浓硝酸呈黄色:4HNO3=4NO2↑+O2↑+2H2O | |
| D. | 久置碳酸氢铵有刺激性气味:NH4HCO3=NH3↑+CO2↑+H2O |
19.下列离子在溶液中可以大量共存的一组是( )
| A. | NH4+ Na+ OH- | B. | Na+ H+ SO32- | ||
| C. | K+ NO3- Cl- | D. | Ca2+ NO3- CO32- |
18.下列各组物质的晶体中,晶体类型相同,化学键类型也完全相同的是( )
0 167920 167928 167934 167938 167944 167946 167950 167956 167958 167964 167970 167974 167976 167980 167986 167988 167994 167998 168000 168004 168006 168010 168012 168014 168015 168016 168018 168019 168020 168022 168024 168028 168030 168034 168036 168040 168046 168048 168054 168058 168060 168064 168070 168076 168078 168084 168088 168090 168096 168100 168106 168114 203614
| A. | CO2和SiO2 | B. | CCl4和Fe | C. | CaCl2和HCl | D. | SO3和SO2 |
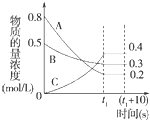 在一定条件下,A气体与B气体反应生成C气体.反应过程中,反应物与生成物的浓度随时间变化的曲线如图.回答下列问题:
在一定条件下,A气体与B气体反应生成C气体.反应过程中,反应物与生成物的浓度随时间变化的曲线如图.回答下列问题: 2C.
2C.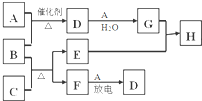 下图涉及的物质所含元素中,除一种元素外,其余均为短周期元素.已知:A、F为无色气体单质,B为能使湿润红色石蕊试纸变蓝的气体,C为黑色氧化物,E为红色金属单质,H为蓝色溶液(部分反应的产物未列出).请回答下列问题:
下图涉及的物质所含元素中,除一种元素外,其余均为短周期元素.已知:A、F为无色气体单质,B为能使湿润红色石蕊试纸变蓝的气体,C为黑色氧化物,E为红色金属单质,H为蓝色溶液(部分反应的产物未列出).请回答下列问题: .
.