题目内容
1.设NA为阿伏加德罗常数的数值,下列说法正确的是( )| A. | 4.6 g NO2与N2O4的混合物中含有的N原子数为0.1NA | |
| B. | 常温常压下,22.4 L NO的分子数为0.1NA | |
| C. | 将0.3mol NO2溶于水,完全反应后,转移的电子数为0.2 NA | |
| D. | 1L0.1mol•L-1 氨水中含有的NH3分子数为0.1NA |
分析 A、NO2与N2O4的最简式均为NO2;
B、常温常压下,气体摩尔体积大于22.4L/mol;
C、NO2与水反应时,3molNO2转移2mol电子;
D、氨水中的主要微粒为NH3•H2O.
解答 解:A、NO2与N2O4的最简式均为NO2,故4.6g混合物中NO2的物质的量为0.1mol,故含有0.1mol氮原子,即0.1NA个,故A正确;
B、常温常压下,气体摩尔体积大于22.4L/mol,故22.4LNO的物质的量小于1mol,故分子个数小于NA个,故B错误;
C、NO2与水的反应:3NO2+H2O=2HNO3+NO,3molNO2转移2mol电子,故0.3molNO2转移0.2mol电子,即0.2NA个,故C正确;
D、氨气溶于水后部分和水反应生成NH3•H2O,故氨水中含有的NH3分子数小于0.1NA,故D错误.
故选AC.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
11.原子的核电荷数小于18的某元素X,其原子的电子层数为n,最外层电子数为2n+1,原子核内质子数为2n2-1.下列有关X的说法中一定正确的是( )
| A. | X位于元素周期表中第2周期ⅤA族 | |
| B. | X元素有-3、+5两种化合价 | |
| C. | X元素在元素周期表中的族序数肯定为奇数 | |
| D. | X元素最高价氧化物对应的水化物可以表示为H3XO4 |
12.已知X、Y元素同周期,且电负性X>Y,下列说法错误的是( )
| A. | X与Y形成化合物时X显负价,Y显正价 | |
| B. | 第一电离能X大于Y | |
| C. | 最高价氧化物对应的水化物的酸性:X强于Y | |
| D. | 气态氢化物的稳定性:HmX强于HmY |
16.下列物质中,不属于同素异形体的一组是( )
| A. | 金刚石和石墨 | B. | 白磷和红磷 | C. | 正丁烷和异丁烷 | D. | O2和O3 |
13.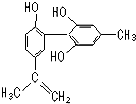 坚决反对运动员服用兴奋剂是保证运动会公平公正的重要举措之一.某种兴奋剂的结构简式如图所示,有关该物质的说法正确的是( )
坚决反对运动员服用兴奋剂是保证运动会公平公正的重要举措之一.某种兴奋剂的结构简式如图所示,有关该物质的说法正确的是( )
 坚决反对运动员服用兴奋剂是保证运动会公平公正的重要举措之一.某种兴奋剂的结构简式如图所示,有关该物质的说法正确的是( )
坚决反对运动员服用兴奋剂是保证运动会公平公正的重要举措之一.某种兴奋剂的结构简式如图所示,有关该物质的说法正确的是( )| A. | 遇FeCl3溶液显紫色,因为该物质与苯酚属于同系物 | |
| B. | 该分子中的所有碳原子不可能共平面 | |
| C. | 滴入KMnO4(H+)溶液,观察紫色变浅,是因为结构中存在碳碳双键 | |
| D. | 1 mol该物质分别与浓溴水和H2反应时,最多消耗Br2和H2分别为4 mol、7 mol |
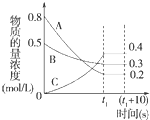 在一定条件下,A气体与B气体反应生成C气体.反应过程中,反应物与生成物的浓度随时间变化的曲线如图.回答下列问题:
在一定条件下,A气体与B气体反应生成C气体.反应过程中,反应物与生成物的浓度随时间变化的曲线如图.回答下列问题: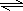 2C.
2C.