4.下列说法中正确的是( )
| A. | 完全由非金属组成的化合物不一定是共价化合物 | |
| B. | 构成分子晶体的粒子一定含有共价键 | |
| C. | 分子晶体的熔点一定比金属晶体的熔点低 | |
| D. | 含有金属离子的晶体一定是离子晶体 |
3.实验测得BeCl2为共价化合物,两个Be-Cl键间的夹角为180°,以下判断正确的是( )
| A. | 由极性键构成的极性分子 | B. | 由极性键构成的非极性分子 | ||
| C. | 由非极性键构成的极性分子 | D. | BeCl2中Be采取sp2杂化 |
2.下列有关说法正确的是( )
| A. | 常温下,0.1mol•L-1 Na2S溶液中存在:c(OH-)=c(H+ )+c(HS-)+c(H2S) | |
| B. | PH=3的醋酸溶液中:c(H+ )=c(CH3COO-)=0.3mol•L-1 | |
| C. | 某溶液中由水电离出的c(OH- )=1×10-a mol•L-1,若a>7时,则该溶液的pH可能为a | |
| D. | pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(Cl-)>c(NH4+ )>c(H+ )>c(OH- ) |
1.25℃时,下列说法正确的是( )
| A. | 0.1mol/LCH3COOH溶液中:c(CH3COO-)=c(H+) | |
| B. | 水离出来的c(H+)=l.0×10-13 mol/L的溶液中,Al3+可能大量存在 | |
| C. | 0.1 mol/LNaHCO3溶液中:c(Na+)=c(HCO3- )+2c(CO3 2-)+c(H2CO3) | |
| D. | O.lmol/L的氨水中滴加稀盐酸至过量,不可能有:c(Cl-)>c(NH4 +)>c(H+)>c(OH-) |
19.硫酸亚铁溶液含有杂质硫酸铜和硫酸铁,为除去杂质,提纯硫酸亚铁,应该加入下列哪种物质( )
| A. | 锌粉 | B. | 镁粉 | C. | 铁粉 | D. | 铝粉 |
18.混凝法是净化水常用的方法,在天然水或污水中加人一定的混凝剂,可使水中的悬浮物变为沉淀而除去.下列物质中可以作为混凝剂的是 ( )
| A. | 氯化钠 | B. | 氯气 | C. | 小苏打 | D. | 明矾 |
16.某化学兴趣小组的同学们将稀硫酸逐渐加入氢氧化铜固体中,至氢氧化铜恰好完全溶解.
(1)该反应的化学方程式是Cu(OH)2+H2SO4═CuSO4+2H2O.
(2)兴趣小组的同学们欲利用上述反应后的剩余溶液探究中和反应的微观本质.
【猜想与假设】
猜想①:中和反应的微观本质是金属阳离子(铜离子)与酸根离子(硫酸根离子)结合生成盐(硫酸铜).
猜想②:中和反应的微观本质是另外两种离子即氢离子和氢氧根离子结合生成了水.
【实验验证】
【反思与评价】
小亮认为不用进行方案l即可直接判断猜想①,理由是稀硫酸与氢氧化铜反应后的溶液呈蓝色,说明铜离子并没有被结合.
0 167191 167199 167205 167209 167215 167217 167221 167227 167229 167235 167241 167245 167247 167251 167257 167259 167265 167269 167271 167275 167277 167281 167283 167285 167286 167287 167289 167290 167291 167293 167295 167299 167301 167305 167307 167311 167317 167319 167325 167329 167331 167335 167341 167347 167349 167355 167359 167361 167367 167371 167377 167385 203614
(1)该反应的化学方程式是Cu(OH)2+H2SO4═CuSO4+2H2O.
(2)兴趣小组的同学们欲利用上述反应后的剩余溶液探究中和反应的微观本质.
【猜想与假设】
猜想①:中和反应的微观本质是金属阳离子(铜离子)与酸根离子(硫酸根离子)结合生成盐(硫酸铜).
猜想②:中和反应的微观本质是另外两种离子即氢离子和氢氧根离子结合生成了水.
【实验验证】
| 方案 | 实验步骤 | 实验现象 | 结论 | 有关反应的化学方程式 |
| 1 | 取少量待测溶液,向其中滴加适量BaCl2溶液 | |||
| 2 | 猜想②正确 | 无 |
小亮认为不用进行方案l即可直接判断猜想①,理由是稀硫酸与氢氧化铜反应后的溶液呈蓝色,说明铜离子并没有被结合.

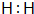 .
. 实验室可用如图所示装置进行多个实验探究,请回答下列问题.
实验室可用如图所示装置进行多个实验探究,请回答下列问题.