15.下列说法错误的是( )
| A. | C2H6和C4H10一定是同系物 | |
| B. | C2H4和C4H8一定是同系物 | |
| C. | 相对分子质量相等的两种物质,不一定是同分异构体 | |
| D. | 烯烃各同系物含碳的质量分数相等 |
14.下列化学用语使用正确的是( )
| A. | 四氯化碳的电子式 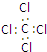 | B. | 乙炔的最简式 CH≡CH | ||
| C. | 聚乙烯的结构简式为 CH2=CH2 | D. | 丙烷的分子结构模型示意图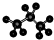 |
13.有机物的种类繁多,但其命名是有规则的.下列有机物命名正确的是( )
| A. | 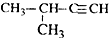 2-甲基-3-丁炔 | B. | 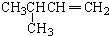 3-甲基丁烯 | C. | 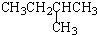 2-甲基丁烷 | D. | 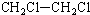 二氯乙烷 |
12.下列说法不正确的是( )
| A. | 石油主要成分都是碳氢化合物 | |
| B. | 煤经气化和液化两个物理变化过程,可变为清洁能源 | |
| C. | 天然气和沼气的主要成分是甲烷 | |
| D. | 75%(体积分数)的乙醇溶液常用于医疗消毒 |
8.N、Cu、H、O、S、Mg是常见的六种元素:
(1)Mg位于元素周期表第三周期第IIA族;N与O的基态原子核外未成对电子个数比为
3:2;Cu的基态原子电子排布式为1s22s22p63s23p63d104s1.
(2)用“>”或“<”填空:
(3)Mg在空气中燃烧可微量生产氮化镁(Mg3N2),Mg3N2(S)溶于足量的稀硫酸可得到两种正盐,在25℃、101kPa下,已知该反应每消耗1mol H2SO4放热akJ,则该反应的热化学方程式为Mg3N2(S)+4H2SO4(aq)=3MgSO4(aq)+(NH4)2SO4(aq)△H=-4akJ/mol.
(4)工业上采取加热条件下用氨气还原氧化铜制取铜,同时得到两种无污染的气体(或蒸汽).写出该反应的化学方程式,并标出电子转移的方向和数目 .
.
(1)Mg位于元素周期表第三周期第IIA族;N与O的基态原子核外未成对电子个数比为
3:2;Cu的基态原子电子排布式为1s22s22p63s23p63d104s1.
(2)用“>”或“<”填空:
| 碱性: Mg (OH)2> Cu(OH)2 | 第一电离能:O< N | 熔点: MgS< MgO | 稳定性: H2S< H2O |
(4)工业上采取加热条件下用氨气还原氧化铜制取铜,同时得到两种无污染的气体(或蒸汽).写出该反应的化学方程式,并标出电子转移的方向和数目
 .
.
7.在加热固体NH4Al(SO4)2•12H2O时,固体质量随温度的变化曲线如图所示:已知A点物质为NH4Al(SO4)2,B点物质为Al2(SO4) 3,下列判断正确的是( )
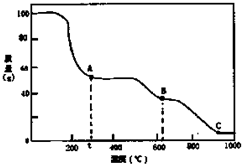

| A. | 0℃→t℃的过程变化是物理变化 | |
| B. | C点物质是工业上冶炼铝的原料 | |
| C. | A→B反应中生成物只有Al2(SO4)3和NH3两种 | |
| D. | Al2(SO4)3能够净水,其原理为:Al3++3OH?Al(OH)3 |
6.下列有关NaHSO3溶液的叙述正确的是( )
0 167042 167050 167056 167060 167066 167068 167072 167078 167080 167086 167092 167096 167098 167102 167108 167110 167116 167120 167122 167126 167128 167132 167134 167136 167137 167138 167140 167141 167142 167144 167146 167150 167152 167156 167158 167162 167168 167170 167176 167180 167182 167186 167192 167198 167200 167206 167210 167212 167218 167222 167228 167236 203614
| A. | 该溶液中,K+、Ca2+、Cl2、Br-可以大量共存 | |
| B. | 与FeCl3反应的离子方程式:SO32-+2 Fe3++H2O═SO42-+2Fe2++2H+ | |
| C. | 和足量Ca(OH)2溶液反应的离子方程式:Ca2++OH-+HSO3-═CaSO3↓+H2O | |
| D. | 能使含I2的淀粉溶液蓝色褪去,说明NaHSO3溶液具漂白性 |
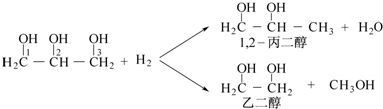
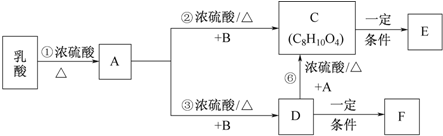
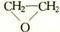 .
. .
. .
. .
.