8.现有常温下水电离出的c(H+)均为1×10-11mol/L的4种溶液:①HCl溶液;②CH3COOH溶液;③NaOH溶液;④氨水.有关上述溶液的比较中,正确的是( )
| A. | 向等体积溶液中分别加水稀释100倍后,溶液的pH:③>④>②>① | |
| B. | 等体积的①、②、③溶液分别与足量铝粉反应,生成H2的量①最小 | |
| C. | ②、③溶液等体积混合后,溶液显碱性 | |
| D. | ①、④溶液混合若pH=7,则消耗溶液的体积:④>① |
6.已知某强酸性的溶液中存在大量的NO3-,下列有关该溶液中还存在的物质叙述正确的是( )
| A. | 铝元素能以Al3+或AlO2-的形式存在 | |
| B. | 铁元素能以Fe2+和Fe3+的形式共存 | |
| C. | 硫元素主要以SO42-的形式存在 | |
| D. | 氯元素能以Cl-或ClO-的形式存在 |
5.下列物质递变规律不能用元素周期律解释的是( )
| A. | 非金属性:C>Si | B. | 碱性:NaOH>Mg(OH)2 | ||
| C. | 酸性:H2SO3>H2CO3 | D. | 还原性:HI>HBr |
4.下列标志的高分子材料的单体,其中一种单体与其他三种单体均不是同系物的是( )
| A. |  HDPE高密度乙烯 | B. |  LDPE低密度乙烯 | C. |  DPP聚丙烯 | D. |  PS聚苯乙烯 |
3.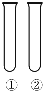 下列①②对应的试剂(或条件)不能完成实验目的是( )
下列①②对应的试剂(或条件)不能完成实验目的是( )
 下列①②对应的试剂(或条件)不能完成实验目的是( )
下列①②对应的试剂(或条件)不能完成实验目的是( )| 实验目的 | 试剂(或条件) | |
| A | 温度对Na2S2O3与H2SO4反应速率的影响 | ①热水浴②冷水浴 |
| B | 用Na块检验乙醇分子存在不同与烃分子里的氢原子 | ①乙醇②煤油 |
| C | 用酸化的AgNO3溶液检验来自水中Cl-能否蒸馏除去 | ①自来水②蒸馏水 |
| D | 用溴水检验苯的同系物种取代基对苯活性有影响 | ①苯②甲苯 |
| A. | A | B. | B | C. | C | D. | D |
2.根据元素周期律,由列事实进行归纳推测,推测不合理的是事实( )
| 事实 | 推测 | |
| A | 12Mg与水反应缓慢,20Ca与水反应较快 | 56Ba(IIA族)与水反应更快 |
| B | Si是半导体材料,同族Ge也是半导体材料 | Ⅳ族的元素都是半导体材料, |
| C | HCl在1500℃时分解,HI在230℃时分解 | HBr的分解温度介于二者之间 |
| D | Si与H2高温时反应,S与H2加热能反应 | P与H2在高温时能反应 |
| A. | A | B. | B | C. | C | D. | D |
1.如图为锌铜显示原电池装置图,下列说法不正确( )


| A. | 电子由Zn极流向Cu极 | |
| B. | 该装置的总反应Zn+Cu2+═Zn2++Cu | |
| C. | 一段时间后,A池带正电荷,B池带负电荷 | |
| D. | 取出盐桥,电流计指针不再偏转 |
20.用灼烧法证明海带中含有碘元素,各步骤选用的实验用品不必都用到( )
| 实验步骤 | 实验用品 | |
| A | 步骤1:将海带灼烧灰化 |  |
| B | 步骤2:将海带灰溶解、过滤 | 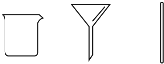 |
| C | 步骤3:氧化滤液中的I- | 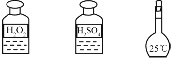 |
| D | 步骤4:检验碘元素 |  |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
19.下列解释事实的方程式不正确的是( )
0 166915 166923 166929 166933 166939 166941 166945 166951 166953 166959 166965 166969 166971 166975 166981 166983 166989 166993 166995 166999 167001 167005 167007 167009 167010 167011 167013 167014 167015 167017 167019 167023 167025 167029 167031 167035 167041 167043 167049 167053 167055 167059 167065 167071 167073 167079 167083 167085 167091 167095 167101 167109 203614
| A. | 铝热法炼铁:2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3 | |
| B. | 工业进行“氮的固定”:N2+3H2$?_{催化剂}^{高温、高压}$2NH3 | |
| C. | 铅蓄电池充电时阴极反应:PbSO4(s)+2e-=Pb(s)+SO42-(aq) | |
| D. | 用铜和稀硝酸制备硝酸铜:Cu+4H++2NO3-=Cu2++2NO2↑+2H2 |