题目内容
20.用灼烧法证明海带中含有碘元素,各步骤选用的实验用品不必都用到( )| 实验步骤 | 实验用品 | |
| A | 步骤1:将海带灼烧灰化 |  |
| B | 步骤2:将海带灰溶解、过滤 | 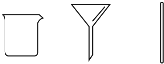 |
| C | 步骤3:氧化滤液中的I- | 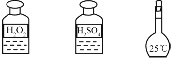 |
| D | 步骤4:检验碘元素 |  |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
分析 A、灼烧固体物质需在坩埚中进行,需要酒精灯加热;
B、溶解需要烧杯和玻璃棒,过滤需要漏斗;
C、容量瓶是配制一定物质的量浓度溶液的仪器,氧化碘离子不需要容量瓶;
D、淀粉遇碘变蓝,需要胶头滴管和试管进行检验.
解答 解:A、灼烧海带时使用三角架、泥三角、坩埚、坩埚钳、酒精灯,故A正确;
B、海带灰溶解、过滤时使用烧杯、普通漏斗、玻璃棒、铁架台,故B正确;
C、氧化碘离子时不需要使用容量瓶,故C错误;
D、取少量含碘溶液需要胶头滴管个试管,利用淀粉溶液检验,故D正确,故选C.
点评 本题主要考查的是实验室中常见仪器的使用以及简单的化学实验操作,难度不大,熟练记忆各种仪器的使用方法是解决本题的关键.

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案
相关题目
10.下列关于元素的说法正确的是( )
| A. | 元素周期表中元素种类最多的周期是第6周期 | |
| B. | 第IA族元素均为碱金属元素 | |
| C. | 原子最外层电子数为2的元素一定位于第ⅡA族 | |
| D. | 元素周期表中元素种类最多的族是第Ⅷ族 |
11.在 2L的密闭容器中,一定条件下发生化学反应:2NO(g)+2CO(g)?N2(g)+2CO2(g)△H=-746.4kJ/mol
起始反应时NO和CO为4mol,10s达到化学平衡,测得N2为1mol.下列说法中正确的是( )
起始反应时NO和CO为4mol,10s达到化学平衡,测得N2为1mol.下列说法中正确的是( )
| A. | 反应前5 s内,用NO表示的平均反应速率为0.1 mol•L-1•S-1 | |
| B. | 达到平衡后,CO2的浓度与CO的浓度不同 | |
| C. | 当v正(CO)=2v逆(N2)时反应达到平衡 | |
| D. | 达到平衡后,升高温度,正反应速率将减小,逆反应速率将增大 |
8.化合物A、B是中学常见的物质,其阴阳离子可从下表中选择
(1)若A的水溶液为酸性,往B的水溶液加Al有气体产生,A、B的水溶液混合后,只产生不溶于稀硝酸的白色沉淀,①B的化学式为Ba(OH)2;
②A、B溶液混合后加热能产生气体的反应的离子方程式为H++SO42-+NH4++Ba2++2OH-$\frac{\underline{\;\;△\;\;}}{\;}$BaSO4↓+NH3↑+2H2O.
(2)若A的水溶液为浅绿色,B的焰色反应呈黄色.向A的水溶液中加入稀盐酸无明显现象,再加入B后溶液变黄,但A、B的水溶液混合后无明显变化.则
①A为FeI2;
②经分析上述过程中溶液变黄的原因可能有两种:
I仅有I-被氧化成I2使溶液呈黄色ⅡI-、Fe2+均被氧化使溶液呈黄色;
③请用一简易方法证明上述溶液变黄的原因取少量变黄溶液于试管中,滴加几滴KSCN溶液,若变红则Ⅱ合理,否则Ⅰ合理.
| 阳离子 | K+ Na+ NH+4 Fe2+ Ba2+ Cu2+ |
| 阴离子 | OH- I- NO3- AlO2- HCO3- HSO4- |
②A、B溶液混合后加热能产生气体的反应的离子方程式为H++SO42-+NH4++Ba2++2OH-$\frac{\underline{\;\;△\;\;}}{\;}$BaSO4↓+NH3↑+2H2O.
(2)若A的水溶液为浅绿色,B的焰色反应呈黄色.向A的水溶液中加入稀盐酸无明显现象,再加入B后溶液变黄,但A、B的水溶液混合后无明显变化.则
①A为FeI2;
②经分析上述过程中溶液变黄的原因可能有两种:
I仅有I-被氧化成I2使溶液呈黄色ⅡI-、Fe2+均被氧化使溶液呈黄色;
③请用一简易方法证明上述溶液变黄的原因取少量变黄溶液于试管中,滴加几滴KSCN溶液,若变红则Ⅱ合理,否则Ⅰ合理.
15. 25℃时某些弱酸的电离平衡常数如表所示:
25℃时某些弱酸的电离平衡常数如表所示:
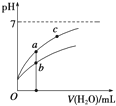
常温下,稀释CH3COOH、HClO两种酸时,溶液的pH随加水量变化的曲线如如图所示,下列说法正确的是( )
 25℃时某些弱酸的电离平衡常数如表所示:
25℃时某些弱酸的电离平衡常数如表所示:| CH3COOH | HClO | H2CO3 |
| K(CH3COOH) =1.8×10-5 | K(HClO) =3.0×10-8 | K(H2CO3)a1=4.4×10-7 K(H2CO3)a2=4.7×10-11 |
| A. | 相同浓度的CH3COONa和NaClO的混合溶液中,各离子浓度的大小关系是:c(Na+)>c(ClO-)>c(CH3COO-)>c(OH-)>c(H+) | |
| B. | 图象中a、c两点所处的溶液中$\frac{c({P}^{-})}{c(HP).c(O{H}^{-})}$相等(HP代表CH3COOH或HClO) | |
| C. | 图象中a点酸的浓度大于b点酸的浓度 | |
| D. | 向NaClO溶液中通入少量二氧化碳的离子方程式为:2ClO-+CO2+H2O═2HClO+CO${\;}_{3}^{2-}$ |
5.下列物质递变规律不能用元素周期律解释的是( )
| A. | 非金属性:C>Si | B. | 碱性:NaOH>Mg(OH)2 | ||
| C. | 酸性:H2SO3>H2CO3 | D. | 还原性:HI>HBr |
12.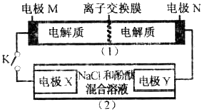 如图装置(1)为一种可充电电池的示意图,其中的离子交换膜只允许K+通过,该电池充、放电的化学方程式为2K2S2+KI3$?_{放电}^{充电}$K2S4+3KI.
如图装置(1)为一种可充电电池的示意图,其中的离子交换膜只允许K+通过,该电池充、放电的化学方程式为2K2S2+KI3$?_{放电}^{充电}$K2S4+3KI.
装置(2)为电解池的示意图.当闭合开关K时,X附近溶液先变红,下列说法正确的是( )
 如图装置(1)为一种可充电电池的示意图,其中的离子交换膜只允许K+通过,该电池充、放电的化学方程式为2K2S2+KI3$?_{放电}^{充电}$K2S4+3KI.
如图装置(1)为一种可充电电池的示意图,其中的离子交换膜只允许K+通过,该电池充、放电的化学方程式为2K2S2+KI3$?_{放电}^{充电}$K2S4+3KI.装置(2)为电解池的示意图.当闭合开关K时,X附近溶液先变红,下列说法正确的是( )
| A. | K+从右到左通过离子交换膜 | |
| B. | 电极M的反应式:I3-+2e-=3I- | |
| C. | 电极X的反应式:4OH--4e-═O2↑+2H2O | |
| D. | 当电极Y有0.2mole-转移时,产生0.1molCl2 |
9.如图是部分短周期元素原子序数与最外层电子数之间的关系图,下列说法中正确的是( )


| A. | 元素对应的离子半径:Z>M>R>W | |
| B. | 简单氢化物的沸点:W>R>Y>X | |
| C. | M、N、R、W的简单离子均能促进水的电离 | |
| D. | Z、X、R、W的最高价氧化物对应的水化物均能与N的单质反应 |