题目内容
2.根据元素周期律,由列事实进行归纳推测,推测不合理的是事实( )| 事实 | 推测 | |
| A | 12Mg与水反应缓慢,20Ca与水反应较快 | 56Ba(IIA族)与水反应更快 |
| B | Si是半导体材料,同族Ge也是半导体材料 | Ⅳ族的元素都是半导体材料, |
| C | HCl在1500℃时分解,HI在230℃时分解 | HBr的分解温度介于二者之间 |
| D | Si与H2高温时反应,S与H2加热能反应 | P与H2在高温时能反应 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.同一主族元素,元素的金属性随着原子序数增大而增强,元素的金属性越强,其与水反应越剧烈;
B.处于金属和非金属分界线处的元素具有金属性和非金属性;
C.元素的非金属性越强,其氢化物的稳定性越强;
D.元素的非金属性越强,其与氢气化合越容易.
解答 解:A.同主族金属元素由上至下金属性增强,与水反应剧烈程度增强,金属性Ba>Ca>Mg,Ca与水反应较快则Ba与水反应更快,故A正确;
B.半导体材料通常位于元素周期表中金属元素和非金属元素的分界处,Si和Ge处于金属和非金属分界线处,能作半导体,但C和Pb不能作半导体,所以第IVA族元素并不都是半导体材料,故B错误;
C.同主族非金属元素由上至下非金属性减弱,气态氢化物的热稳定性减弱,非金属性Cl>Br>I,所以HBr的分解温度介于二者之间,故C正确;
D.同周期非金属元素从左到右非金属性增强,与氢气化合难度减小,非金属性S>P>Si,所以 P与H2在高温时能反应,故D正确;
故选B.
点评 本题考查元素周期律的应用,涉及同一主族、同一周期元素性质递变规律,明确原子结构与元素性质的关系是解本题关键,熟练掌握碱金属族、卤族及第三周期元素性质递变规律,题目难度不大.

练习册系列答案
相关题目
13.短周期元素X、Y、Z、W的原子序数依次增大,X、Y、Z的原子序数之和是W的2倍,X、Z在周期表中的相对物质如图所示,X的最低负价绝对值与其原子的最外层电子数相等.下列说法正确的是( )
| X | |||
| Z |
| A. | 离子半径:r(Y)>r(Z)>r(W) | |
| B. | Z的简单离子能破坏水的电离平衡 | |
| C. | XWm与YWn中化学键类型相同(m、n为正整数) | |
| D. | 元素Z的简单气态氢化物的热稳定性比W的强 |
10.短周期元素甲、乙、丙、丁的原子序数依次增大,甲和乙形成的气态化合物的水溶液显碱性,乙位于第VA族,甲和丙同主族,丁原子最外层电子数与电子层数相等.则下列说法正确的是( )
| A. | 离子半径:丙>丁>乙 | |
| B. | 单质的还原性:丁>丙>甲 | |
| C. | 乙、丙、丁的最高价氧化物对应的水化物能相互反应 | |
| D. | 甲、乙、丙的氧化物均只有一种 |
14.下列说法不正确的是( )
| A. |  的分子式为C17H24O3 的分子式为C17H24O3 | |
| B. | 结构为…-CH=CH-CH=CH-CH=CH-CH=CH-…的高分子化合物,其单体是乙炔 | |
| C. | 有机硅聚醚(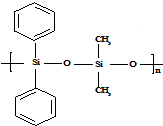 )可由单体 )可由单体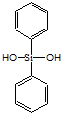 和 和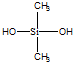 缩聚而成 缩聚而成 | |
| D. | 等质量的甲醇、甲醛、甲醚完全燃烧时的耗氧量依次递增 |
12.下列物质属于共价化合物的是( )
| A. | H2O | B. | I2 | C. | NH4Cl | D. | CaCl2 |




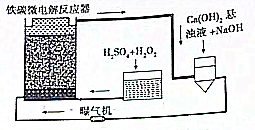 铁碳微电解技术是近年来处理各种污水的一种重要方法,其装置如图所示.
铁碳微电解技术是近年来处理各种污水的一种重要方法,其装置如图所示.