题目内容
5.下列物质递变规律不能用元素周期律解释的是( )| A. | 非金属性:C>Si | B. | 碱性:NaOH>Mg(OH)2 | ||
| C. | 酸性:H2SO3>H2CO3 | D. | 还原性:HI>HBr |
分析 A.同一主族元素,非金属性随着原子序数增大而减弱;
B.元素的金属性越强,其最高价氧化物的水化物碱性越强;
C.元素的非金属性越强,其最高价氧化物的水化物酸性越强;
D.元素的非金属性越强,其氢化物的还原性越弱.
解答 解:A.同一主族元素,非金属性随着原子序数增大而减弱,C、Si属于同一主族元素且原子序数Si>C,所以非金属性C>Si,故A不选;
B.元素的金属性越强,其最高价氧化物的水化物碱性越强,金属性Na>Mg,所以碱性NaOH>Mg(OH)2,故B不选;
C.元素的非金属性越强,其最高价氧化物的水化物酸性越强,非金属性S>C,所以酸性:H2SO4>H2CO3,但H2SO3不是S元素的最高价含氧酸,所以不能用元素周期律解释H2SO3>H2CO3,故C选;
D.元素的非金属性越强,其氢化物的还原性越弱,非金属性Br>I,所以还原性:HI>HBr,故D不选;
故选C.
点评 本题考查元素周期律的应用,明确同一主族、同一周期元素性质递变规律是解本题关键,易错选项是C,注意亚硫酸不是S元素的最高价含氧酸,为易错点.

练习册系列答案
 孟建平名校考卷系列答案
孟建平名校考卷系列答案
相关题目
15.电解普通水(H2O)和重水(D2O)的混合物,通电一段时间后,两极共生成气体18.5g,其体积为33.6L(标况下),在所生成的气体中重氢和普通氢的原子个数比为( )
| A. | 2:3 | B. | 2:5 | C. | 1:2 | D. | 1:3 |
16.关于沉淀溶解平衡和溶度积常数,下列说法不正确的是( )
| A. | Ksp只与难溶电解质的性质和温度有关,而与溶液中的离子浓度无关 | |
| B. | 将饱和Na2SO4溶液加入到饱和石灰水中,有白色沉淀产生,说明Ksp[Ca(OH)2]大于Ksp[CaSO4] | |
| C. | 已知25℃时,Ksp[Fe(OH)3]=4.0×10-38,该温度下反应Fe(OH)3+3H+?Fe3++3H2O的平衡常数K=4.0×104 | |
| D. | 已知25℃时,Ksp[Mg(OH)2]=1.8×10-11,在MgCl2溶液中加入氨水调混合液的pH=11,产生沉淀,则此时溶液中的c(Mg2+)=1.8×10-5mol•L-1 |
13.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 0.1 mol ${\;}_{8}^{16}$OD- 离子含有的质子、中子数均为1.0NA | |
| B. | 含有4.6 g钠元素的过氧化钠和氧化钠的混合物中,所含离子总数为0.3NA | |
| C. | 3.6 g石墨中,含有共价键数为0.3NA | |
| D. | 标准状况下,4.48 L己烷含有的分子数为0.2NA |
20.用灼烧法证明海带中含有碘元素,各步骤选用的实验用品不必都用到( )
| 实验步骤 | 实验用品 | |
| A | 步骤1:将海带灼烧灰化 |  |
| B | 步骤2:将海带灰溶解、过滤 |  |
| C | 步骤3:氧化滤液中的I- |  |
| D | 步骤4:检验碘元素 |  |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
10.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | pH=l的溶液中:Ca2+、Fe2+、NO3- | |
| B. | $\frac{Kw}{c(O{H}^{-})}$=10-2的溶液中:Na+、NH4+、Cl- | |
| C. | c(Fe3+)=0.1 mol.L-1的溶液中:K+、SCN-、SO42- | |
| D. | 由水电离的c(H+)=1×10-14 mol.L-1的溶液中:Na+、AlO2-、CO32- |
17.下列解释实验事实的方程式中,不准确的是( )
| A. | 在CH3COONa 溶液中滴入无色酚酞,溶液变红:CH3COO-+H2O?CH3COOH+OH- | |
| B. | 在Mg(OH)2白色悬浊液中滴入饱和FeCl3溶液,悬浊液变红褐:3Mg(OH)2+2Fe3+═2Fe(OH)3↓+3Mg2+ | |
| C. | 在NaHSO3溶液中滴加紫色石蕊溶液,溶液变红:NaHSO3═Na++H++SO32- | |
| D. | 在稀H2SO4酸化的KMnO4溶液中滴入双氧水,溶液褪色:2MnO4-+5H2O2+6H+═2Mn2++5O2↑+8H2O |
14.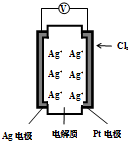 右图所示的原电池可测量空气中Cl2的含量(原电池的电解质是含有自由移动Ag+的固体物质).下列分析不正确的是( )
右图所示的原电池可测量空气中Cl2的含量(原电池的电解质是含有自由移动Ag+的固体物质).下列分析不正确的是( )
 右图所示的原电池可测量空气中Cl2的含量(原电池的电解质是含有自由移动Ag+的固体物质).下列分析不正确的是( )
右图所示的原电池可测量空气中Cl2的含量(原电池的电解质是含有自由移动Ag+的固体物质).下列分析不正确的是( )| A. | 电子由Ag电极经外电路流向Pt电极 | |
| B. | 空气中c(Cl2)越大,Ag极消耗速率越快 | |
| C. | 正极反应:Cl2+2e-+2Ag+═2AgCl | |
| D. | 原电池工作时电解质中Ag+数目减少 |
15.下列化学用语表示正确的是( )
| A. | KF的电子式: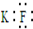 | |
| B. | 异丁烷的结构简式:CH3CH2CH2CH3 | |
| C. | 硫离子的结构示意图: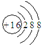 | |
| D. | 氢氧化钡的电离方程式:Ba(OH)2=Ba2++(OH-)2 |