8.常温下1体积pH=2.5的盐酸与10体积某一元强碱溶液恰好完全反应,则该碱溶液的pH等于( )
| A. | 9.0 | B. | 9.5 | C. | 1 0.5 | D. | 1 1.0 |
7.标准状况下,将VLH2S气体通入a Lb mo l/L的 NaOH 溶液中,下列对所得溶液的描述不正确的是( )
| A. | 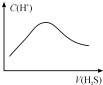 随着 H2S气体的通入,溶液中由水电离出的c(H+)有如图变化关系 | |
| B. | 当$\frac{V}{22.4}$=a b时,所得溶液中存在:c(OH-)+c(S2-)=c(H+)+c(H2S) | |
| C. | 当$\frac{V}{11.2}$=a b时,所得溶液中存在:c(Na+)>c(S2-)>c(OH-)>c(HS-)>c( H+) | |
| D. | 当$\frac{V}{22.4}$<a b<$\frac{V}{11.2}$时,所得溶液中一定存在:c(Na+)=c(S2-)+c(HS-)+c(H2S) |
6.NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 5.6 g铁粉在0.1 mol氯气中充分燃烧,转移电子数为0.3 NA | |
| B. | 1 2.5 mL1 6 mol•L-1浓硫酸与足量铜反应,转移电子数为0.2 NA | |
| C. | 7.8 gNa2S和Na2O2 的混合物中含有的阴离子数等于0.1 NA | |
| D. | 0.5 mol氧单质含有NA个O2 |
5.以下实验或操作不能达到目的是( )
| A. | 用溴水鉴别苯、乙醇、四氯化碳 | |
| B. | 准确称取4.0 gNaOH溶于9 6 mL水得质量分数为4.0%的溶液 | |
| C. | 为除去苯中的少量苯酚,向混合物中加入适量的溴水后过滤 | |
| D. | 用激光笔检验淀粉溶液的丁达尔现象 |
4.为了确定某样品是否被氧化,所选试剂(括号内物质)不正确的是( )
| A. | FeCl2(NH4SCN溶液) | B. | KI(淀粉溶液) | ||
| C. | 白磷(紫色石蕊试液) | D. | Na2SO3( BaCl2 溶液) |
2.某学生在配制一定物质的量浓度氢氧化钠时,结果所配溶液浓度偏高,其原因可能是( )
| A. | 所用氢氧化钠已经潮解 | |
| B. | 向容量瓶中加水未到刻度线 | |
| C. | 有少量氢氧化钠溶液残留在烧杯里 | |
| D. | 用带游码的托盘天平称2.4 gNaOH时误用了“左码右物”方法 |
1.为使Fe2+、Fe3+、Zn2+较完全地形成氢氧化物沉淀,溶液的酸碱度分别为pH 7.7、pH 4.5、pH 6.6.某硫酸锌酸性溶液中含有少量Fe2+,Fe3+杂质离子,为除去这些离子制得纯净的ZnSO4,应加入的试剂是( )
| A. | NaOH溶液 | B. | 氨水 | C. | KMnO4,ZnCO3 | D. | H2O2,ZnO |
20.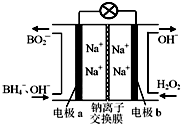 以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,其工作原理如图所示.下列说法正确的是( )
以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,其工作原理如图所示.下列说法正确的是( )
 以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,其工作原理如图所示.下列说法正确的是( )
以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,其工作原理如图所示.下列说法正确的是( )| A. | 电池放电时Na+从b极区移向a极区 | |
| B. | 该电池的负极反应为:BH4-+8OH--8e-═BO2-+6H2O | |
| C. | 电极a采用MnO2,MnO2既作电极材料又有催化作用 | |
| D. | 每消耗3 mol H2O2,转移的电子为3 mol |
19.下列实验装置设计正确的是( )
0 166905 166913 166919 166923 166929 166931 166935 166941 166943 166949 166955 166959 166961 166965 166971 166973 166979 166983 166985 166989 166991 166995 166997 166999 167000 167001 167003 167004 167005 167007 167009 167013 167015 167019 167021 167025 167031 167033 167039 167043 167045 167049 167055 167061 167063 167069 167073 167075 167081 167085 167091 167099 203614
| A. | 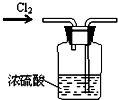 干燥氯气 | B. |  稀释浓硫酸 | ||
| C. |  实验室制氨气 | D. | 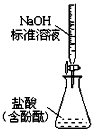 测定盐酸浓度 |