题目内容
3.溶液的配制过程能引起浓度偏高的是( )①用1g 98%的浓硫酸加4g水配成1:4的硫酸;
②配制一定物质的量浓度的硫酸溶液时,定容后,塞好塞子倒转摇匀后,发现液面低于刻度线;
③在100mL无水乙醇中加入2g碘片溶解后配成2%的碘酒溶液;
④在80mL水中加入18.4m o l/L的硫酸20mL,配制3.68mol/L的硫酸溶液;
⑤质量分数为5x%和x%的两种氨水等体积混合配成3x%的氨水;
⑥10%的硫酸和90%的硫酸等体积混合配制5 0%的硫酸溶液.
| A. | ①③⑤ | B. | ②④⑤ | C. | ③④⑥ | D. | ④⑤⑥ |
分析 ①硫酸溶液中,浓度越大其密度越大,根据质量和密度之间的关系确定其体积关系;
②根据C=$\frac{n}{V}$来分析误差,如果n偏大或V偏小都导致配制溶液浓度偏高;
③由于乙醇的密度为0.78g/mL,故在100mL无水乙醇中加入2g碘片,所得溶液的质量小于100g.
④硫酸溶液中,浓度越大其密度越大,根据C=$\frac{n}{V}$来分析溶液浓度;
⑤氨水溶液中,浓度越大其密度越小,根据等质量两种不同质量分数的同种溶液混合时,溶质质量分数为:两种质量分数加起来除以2,如果不等质量混合,溶质质量分数就偏向于质量大的溶液的质量分数.
⑥硫酸溶液中,浓度越大其密度越大,根据溶质质量分数的计算公式来求解,混合后溶质质量为混合前两溶液中溶质质量之和,混合后溶液质量为混合前溶液质量之和;
解答 解:①浓硫酸的密度大于1g/mL,水的密度是1g/mL,用1g98%的浓硫酸加4g水配成1:4(体积比)的硫酸,浓硫酸的体积和水的体积比小于1:4,导致配制溶液体积比偏小,故①不选;
②配制一定物质的量浓度的硫酸溶液时,定容后,塞好塞子倒转摇匀后,发现液面低于刻度线,溶质的物质的量和溶液的体积都不变,所以配制溶液浓度不变,故②不选;
③由于乙醇的密度为0.78g/mL,故在100mL无水乙醇中加入2g碘片,所得溶液的质量小于100g,则溶液的质量分数大于2%,故③选;
④浓硫酸溶液密度大于水的密度,在80mL水中加入18.4mol/L的硫酸20mL,溶液体积小于100mL,所以配制浓度高于3.68mol/L,故④选;
⑤5x%的氨水与x%的氨水等质量混合时溶质的质量分数为:$\frac{5x%+x%}{2}$=3x%,如果等体积混合时,由于5x%的氨水的密度小于x%的氨水的密度,则所以x%的氨水的质量大于5x%的氨水的质量,所以混合后溶质质量分数偏向于X%的氨水,故质量分数小于3x%,故⑤不选;
⑥溶质的质量分数分别为90%和10%的两种硫酸溶液等质量混合后,溶液中的溶质的质量分数为$\frac{90%+10%}{2}$=50%,哪种溶液的质量大,就偏向于谁的溶质质量分数,由于90%硫酸溶液的密度大于10%硫酸溶液的密度,所以90%和10%的两种硫酸溶液等体积混合后,90%硫酸溶液的质量大于10%硫酸溶液的质量,所以混合后溶液中的溶质的质量分数大于50%,则配制溶液浓度偏大,故⑥选;
故选C.
点评 本题考查有关误差分析,难度中等.注意形成规律①密度比水大的两种不同浓度溶液混合,等体积混合后所得溶液中溶质的质量分数大于等质量混合后所得溶液中溶质的质量分数(即两种溶液中溶质的质量分数之和的一半).如氢氧化钠、氯化钠溶液等.同理有:②密度比水小的两种不同浓度溶液混合,等体积混合后所得溶液中溶质的质量分数小于等质量混合后所得溶液中溶质的质量分数(即两种溶液中溶质的质量分数之和的一半).如氨水、酒精溶液等.

| A. | 乙炔的燃烧热为1256 kJ•mol-1 | |
| B. | 若生成2 mol液态水,则△H=-2512 kJ•mol-1 | |
| C. | 若形成4 mol碳氧共用电子对,则放出的热量为2512 kJ | |
| D. | 若转移10 mol电子,则消耗2.5 mol O2 |
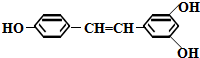 ,仅改变羟基(-OH)在苯环上的位置,且每个苯环上均含有羟基,可得到白藜芦醇的同分异构体甲,则甲可能的结构有( )
,仅改变羟基(-OH)在苯环上的位置,且每个苯环上均含有羟基,可得到白藜芦醇的同分异构体甲,则甲可能的结构有( )| A. | 13种 | B. | 15种 | C. | 17种 | D. | 19种 |

请回答下列问题:
(1)硬质试管中发生的化学方程式为3Fe+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2.
(2)检验实验中所产生气体的方法是将所得的气体在导管出口处点燃,导管上方罩一个干燥的烧杯,若产生淡蓝色的火焰同时烧杯内壁出现水珠,证明产生的气体是氢气.
(3)如果要测量实验中产生的气体体积,可以采用下列实验装置,请将虚线内装置图的导管补充完整.(在答题卡上作图)

(4)某同学对反应后硬质试管中剩余固体物质的成分进行了研究,设计了如下实验.(实验限选试剂:盐酸,NaOH溶液、FeCl3溶液、KMnO4溶液、CuSO4溶液、KSCN溶液)
| 实验操作 | 主要现象 | 结论或解释 |
| 步骤1:取少量固体于试管中,加入足量 ①氯化铁溶液. | 固体减少且剩余, 淡黄色溶液变浅. | 固体中含有金属铁 |
| 步骤2:分离步骤1的剩余固体于另一试管中,加入足量 ②盐酸,将反应后溶液分成甲、乙两份. | 固体全部消失. | 反应的化学方程式 ③ Fe3O4+8HCl=FeCl2+2FeCl3+H2O. |
| 步骤3:在步骤2的甲溶液中加入几滴 ④高锰酸钾溶液. | 紫红色褪去. | 溶液中含有Fe2+. |
| 步骤4:在步骤2的乙溶液中加入几滴⑤KSCN溶液. | 溶液变成红色. | 溶液中含有Fe3+. |
| A. | 乙醇和乙酸均能与钠反应生成氢气 | |
| B. | 煤的干馏、油脂的皂化和石油的分馏都属于化学变化 | |
| C. | 丙烷(C3H8)和乙醇(C2H5OH)均存在同分异构体 | |
| D. | 糖类、油脂、蛋白质均属于高分子化合物 |
| A. | 9.0 | B. | 9.5 | C. | 1 0.5 | D. | 1 1.0 |
| 序号 | 实验目的 | 方法及操作 |
| ① | 比较水和乙醇中羟基氢的活泼性强弱 | 用金属钠分别与水和乙醇反应 |
| ② | 欲证明CH2=CHCHO中含有碳碳双键 | 滴入KMnO4酸性溶液,看紫红色是否褪去 |
| ③ | 证明蛋白质在某些无机盐溶液作用下发生变性 | 向鸡蛋清溶液中加入饱和硫酸铜溶液,有沉淀析出;再把沉淀加入蒸馏水中 |
| ④ | 检验溴乙烷中的溴元素 | 将少量溴乙烷与NaOH溶液混合共热,充分反应并冷却后,向溶液中加稀HNO3酸化,再滴加AgNO3溶液 |
| ⑤ | 判断不同反应的反应速率的大小 | 比较不同反应的反应热数据的大小 |
| A. | ①③④ | B. | ②③④ | C. | ①②④ | D. | ②③⑤ |
| X | |||
| Z |
| A. | 离子半径:r(Y)>r(Z)>r(W) | |
| B. | Z的简单离子能破坏水的电离平衡 | |
| C. | XWm与YWn中化学键类型相同(m、n为正整数) | |
| D. | 元素Z的简单气态氢化物的热稳定性比W的强 |