20.下列说法中不正确的是( )
| A. | 若XY3分子中X原子处于正三角形的中心,则XY3分子为非极性分子 | |
| B. | C2H5OH与C2H5Br相比,前者的沸点远高于后者,其原因是前者的分子间存在氢键 | |
| C. | 同周期ⅠA族元素和ⅦA族元素之间只能形成离子化合物 | |
| D. | 由两种非金属元素组成的化合物分子中只可能有极性键,不会有非极性键 |
18.将下列浓溶液蒸干并灼烧,可以得到原溶质的是( )
| A. | 氯化钠 | B. | 碳酸氢钠 | C. | 偏铝酸钠 | D. | 氯化铁 |
17.常温时,下列各组离子能大量共存的是( )
| A. | Ag+、K+、NO3-、Cl- | B. | Fe3+、NH4+、SO42-、NO3- | ||
| C. | Fe2+、Na+、Cl-、ClO- | D. | H+、I-、SO42-、HCO3- |
15.一密闭容器中盛有甲烷,在隔绝空气条件下长时间加热到1000℃左右,然后恢复至室温(20℃).这时容器内气体的压强是原来甲烷压强的m倍,原来甲烷的密度是容器内气体密度的n倍.下列判断正确的是( )
| A. | m=2,n=4 | B. | m=0.5,n=4 | C. | m=2,n=0.25 | D. | m=0.5,n=0.25 |
14.已知X、Y、Z、W、R是原子序数依次增大的短周期主族元素,X是周期表中原子半径最小的元素,Y元素的最高正价与最低负价的绝对值相等,Z的核电荷数是Y的2倍,W的最外层电子数是最内层电子数的3倍.下列说法不正确的是( )
| A. | 化合物YR4中各原子均满足8电子稳定结构 | |
| B. | 对应原子半径:Z<W<R | |
| C. | W与X、W与Y形成的化合物化学键类型完全相同 | |
| D. | Y的最高价氧化物对应的水化物是弱酸 |
13.锗(Ge)是第32号元素,处于元素周期表中金属区与非金属区的交界线上,下列叙述中正确的是( )
| A. | 锗是一种金属性很强的元素 | B. | 锗化氢(GeH4)稳定性很强 | ||
| C. | 锗酸(H4GeO4)是难溶于水的强酸 | D. | 锗元素位于第四周期第ⅣA族 |
12.从化学键角度分析,下列属于化学变化的是( )
| A. | 蔗糖溶解 | B. | H2SO4溶于水 | C. | NH3溶于水 | D. | 氯化镁受热熔化 |
11.食盐(NaCl)是生活中常用的调味品,HCl是胃酸的主要成分,下列关于两种物质的说法正确的是( )
0 166886 166894 166900 166904 166910 166912 166916 166922 166924 166930 166936 166940 166942 166946 166952 166954 166960 166964 166966 166970 166972 166976 166978 166980 166981 166982 166984 166985 166986 166988 166990 166994 166996 167000 167002 167006 167012 167014 167020 167024 167026 167030 167036 167042 167044 167050 167054 167056 167062 167066 167072 167080 203614
| A. | 炒菜时放入食盐并不破坏NaCl中的化学键 | |
| B. | HCl的电子式是 | |
| C. | NaCl熔化时破坏共价键 | |
| D. | HCl的结构式是H-Cl |
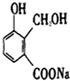
 有一化合物(X)结构简式如图,它与分别与金属钠、氢氧化钠和碳酸氢钠反应时,不可能生成的产物是( )
有一化合物(X)结构简式如图,它与分别与金属钠、氢氧化钠和碳酸氢钠反应时,不可能生成的产物是( )