题目内容
15.一密闭容器中盛有甲烷,在隔绝空气条件下长时间加热到1000℃左右,然后恢复至室温(20℃).这时容器内气体的压强是原来甲烷压强的m倍,原来甲烷的密度是容器内气体密度的n倍.下列判断正确的是( )| A. | m=2,n=4 | B. | m=0.5,n=4 | C. | m=2,n=0.25 | D. | m=0.5,n=0.25 |
分析 甲烷在高温下可分解成炭黑和氢气,CH4$\stackrel{1000℃}{→}$C+2H2,根据阿伏加德罗定律可知:同温同体积下两种气体的物质的量之比等于压强的正比,根据ρ=mv体积不变,密度之比等于气体的质量比计算.
解答 解:一密闭容器中盛有甲烷,假设甲烷的物质的量为amol,甲烷在高温下可分解成炭黑和氢气,CH4$\stackrel{1000℃}{→}$C+2H2,生成2amol氢气,同温同体积下两种气体的物质的量之比等于压强的正比,n(H2):n(CH4)=2a:a=2:1,所以m=2,根据ρ=mv容器体积不变,密度之比等于气体的质量比m(CH4):m(H2)=amol×16g/mol:2a×2g/mol=4:1,所以n=4,
故选A.
点评 本题主要考查了甲烷的性质,掌握同温同体积下两种气体的物质的量之比等于压强的正比,容器体积不变,密度之比等于气体的质量比是解答关键,题目难度不大.

练习册系列答案
相关题目
5.下列有机物的系统名称中,正确的是( )
| A. | 2,4,4-三甲基戊烷 | B. | 4-甲基-2-戊烯 | ||
| C. | 4-甲基-5-乙基庚烷 | D. | 1,2,4-三甲基丁烷 |
6.下列物质中既含有共价键又含离子键的化合物是( )
| A. | NaCl | B. | Al2O3 | C. | NaOH | D. | CH4 |
3.2H、13C、15N、18O、34S等常用作环境分析指示物.下列有关说法正确的是( )
| A. | 34S原子核内中子数为16 | |
| B. | 1H${\;}_{2}^{16}$O和1H${\;}_{2}^{18}$O的相对分子质量不同 | |
| C. | 13C和15N原子的原子序数相差2 | |
| D. | 2H+结合OH-的能力比1H+的更强 |
10.最近科学家研究出一种新的分子,它具有类似足球的空心结构,分子式为12C60,下列有关说法正确的是( )
| A. | 12C60是一种新型化合物 | B. | C60和石墨是碳的同素异形体 | ||
| C. | 12C60具有离子键 | D. | 12C60的摩尔质量是720 |
20.下列说法中不正确的是( )
| A. | 若XY3分子中X原子处于正三角形的中心,则XY3分子为非极性分子 | |
| B. | C2H5OH与C2H5Br相比,前者的沸点远高于后者,其原因是前者的分子间存在氢键 | |
| C. | 同周期ⅠA族元素和ⅦA族元素之间只能形成离子化合物 | |
| D. | 由两种非金属元素组成的化合物分子中只可能有极性键,不会有非极性键 |
4.现有部分短周期元素的原子结构如下表:
(1)写出X的元素符号:N,Z元素原子的质量数为23.
(2)元素Y的最高价氧化物的结构式为O=C=O,Z元素的单质在空气中燃烧产物的电子式 ,用电子式表示X的气态氢化物的形成过程
,用电子式表示X的气态氢化物的形成过程 .
.
(3)Y的最高价氧化物和Z元素的单质在空气中燃烧产物发生反应的化学方程式为2CO2+2Na2O2=2Na2CO3+O2;若反应过程中,转移电子数为6.02×1023,则消耗Y的最高价氧化物的质量为1mol.
| 元素 编号 | 元素原子结构 |
| X | 原子结构示意图为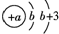 |
| Y | 最外层电子数是次外层电子数的2倍 |
| Z | 原子核内含有12个中子,且其离子的结构示意图为 |
(2)元素Y的最高价氧化物的结构式为O=C=O,Z元素的单质在空气中燃烧产物的电子式
 ,用电子式表示X的气态氢化物的形成过程
,用电子式表示X的气态氢化物的形成过程 .
.(3)Y的最高价氧化物和Z元素的单质在空气中燃烧产物发生反应的化学方程式为2CO2+2Na2O2=2Na2CO3+O2;若反应过程中,转移电子数为6.02×1023,则消耗Y的最高价氧化物的质量为1mol.
5.下列分子的电子式书写正确的是( )
| A. | 氨 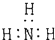 | B. | 四氯化碳  | C. | 氮 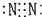 | D. | 二氧化碳 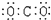 |

 ;
;