19.下列变化过程需加入氧化剂的是( )
| A. | HCl→H2 | B. | Mg→Mg2+ | C. | Cl-→AgCl | D. | CuO→Cu |
16.设NA表示阿伏加德罗常数,下列说法中正确的是( )
| A. | 1mol某气体的体积为22.4L,该气体的状况不一定是标准状况 | |
| B. | 1 mol H2O中含有的质子数为9NA | |
| C. | 2.4g镁由原子变为离子时,失电子为0.1NA | |
| D. | 将1mol CO2气体变成固体,其所含的分子数小于NA |
15.在无色透明的溶液中,可以大量共存的离子组是( )
| A. | MnO4-、Fe2+、K+、Cl- | B. | Ca2+、Na+、Cl-、SO42- | ||
| C. | Ca2+、Cl-、NO3-、K+ | D. | Ca2+、H+、OH-、CO32- |
14.下列离子方程式中正确的是( )
| A. | 稀醋酸与NaOH溶液的反应:H++OH-═H2O | |
| B. | 铜粉与稀硝酸的反应:Cu+2H+═Cu2++H2↑ | |
| C. | 氯气与碘化钾溶液的反应:Cl2+I-═Cl-+I2 | |
| D. | 碳酸钠溶液与足量稀盐酸的反应:CO32-+2H+═CO2↑+H2O |
13.能用OH-+H+═H2O 这个离子方程式表示的化学反应的是( )
| A. | 氢氧化铝和硝酸溶液反应 | B. | Fe(OH)3溶液和硫酸反应 | ||
| C. | 氢氧化钡溶液和稀硫酸 | D. | KOH溶液和稀硝酸反应 |
11.下列说法正确的是( )
①22.4L氧气中一定含有NA个氧分子
②将80gNaOH溶于1L水中,所得溶液中NaOH的物质的量浓度是2mol/L
③18g水在标准状况下的体积为22.4L
④在常温常压下,20mLNH3和60mL氧气所含 分子数之比为1:3.
0 166880 166888 166894 166898 166904 166906 166910 166916 166918 166924 166930 166934 166936 166940 166946 166948 166954 166958 166960 166964 166966 166970 166972 166974 166975 166976 166978 166979 166980 166982 166984 166988 166990 166994 166996 167000 167006 167008 167014 167018 167020 167024 167030 167036 167038 167044 167048 167050 167056 167060 167066 167074 203614
①22.4L氧气中一定含有NA个氧分子
②将80gNaOH溶于1L水中,所得溶液中NaOH的物质的量浓度是2mol/L
③18g水在标准状况下的体积为22.4L
④在常温常压下,20mLNH3和60mL氧气所含 分子数之比为1:3.
| A. | ①②③④ | B. | ①②④ | C. | ②③ | D. | ④ |
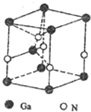 碳、氮元素及其化合物在生产、生活和科学研究等方面有着重要的作用研究它们的结构与性质意义重大.请回答下列有关问题:
碳、氮元素及其化合物在生产、生活和科学研究等方面有着重要的作用研究它们的结构与性质意义重大.请回答下列有关问题: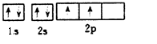 .
.