题目内容
19.下列变化过程需加入氧化剂的是( )| A. | HCl→H2 | B. | Mg→Mg2+ | C. | Cl-→AgCl | D. | CuO→Cu |
分析 需加入氧化剂才能实现,说明题中物质应具有还原性,被氧化,所含元素的化合价应升高,以此解答该题.
解答 解:A.H元素化合价降低,被还原,应加入还原剂,故A错误;
B.Mg元素化合价升高,被氧化,应加入氧化剂才能实现,故B正确;
C.元素化合价不变,不是氧化还原反应,故C错误;
D.Cu元素化合价降低,被还原,应加入还原剂,故D错误.
故选B.
点评 本题考查氧化还原反应,为高考常见题型,侧重于学生的分析能力的考查,明确元素化合价的变化为解答该题的关键,难度不大.

练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案
相关题目
7.${\;}_{\;}^{37}$Cl、${\;}_{\;}^{35}$Cl为不同的核素,下列说法正确的是( )
| A. | ${\;}_{\;}^{37}$Cl2的摩尔质量是74 | |
| B. | 通常情况下,氯气做氧化剂,但氯气也具有还原性 | |
| C. | 35克的${\;}_{\;}^{35}$Cl2含有电子17mol | |
| D. | 常温下,4.48L ${\;}_{\;}^{37}$Cl2含有8NA 个中子(NA 为阿伏加德罗常数) |
7.①-OH ②OH- ③-Br ④NO2 ⑤ ⑥-C6H5 ⑦Br-⑧-COOH ⑨-CH3其中不是官能团的是( )
⑥-C6H5 ⑦Br-⑧-COOH ⑨-CH3其中不是官能团的是( )
 ⑥-C6H5 ⑦Br-⑧-COOH ⑨-CH3其中不是官能团的是( )
⑥-C6H5 ⑦Br-⑧-COOH ⑨-CH3其中不是官能团的是( )| A. | ①③④⑥⑧ | B. | ②④⑥⑦⑨ | C. | ②③⑤⑦⑧ | D. | ①③⑤⑧ |
14.下列离子方程式中正确的是( )
| A. | 稀醋酸与NaOH溶液的反应:H++OH-═H2O | |
| B. | 铜粉与稀硝酸的反应:Cu+2H+═Cu2++H2↑ | |
| C. | 氯气与碘化钾溶液的反应:Cl2+I-═Cl-+I2 | |
| D. | 碳酸钠溶液与足量稀盐酸的反应:CO32-+2H+═CO2↑+H2O |
4.某气态烃1mol能与2mol HCl完全加成,加成后产物分子中的氢原子又可被6mol Cl2完全取代,则此气态烃可能是( )
| A. | CH3C≡CCH3 | B. | CH2=CH2 | C. | CH≡CCH3 | D. | CH2=CHCH3 |
8.以下各微粒中,所有原子都满足最外层为8电子结构的是( )
| A. | H3O+ | B. | BF3 | C. | CO2 | D. | PCl5 |
9.工业上铁的冶炼是在炼铁高炉中进行的,发生的反应是:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,对于该反应,下列说法正确的是( )
| A. | 反应中转移3个电子 | B. | Fe2O3发生还原反应 | ||
| C. | CO被还原 | D. | CO为氧化剂 |
 元素周期表中第ⅦA族元素的单质及其化合物的用途广泛.
元素周期表中第ⅦA族元素的单质及其化合物的用途广泛.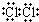 .新制的氯水可用于漂白,工业上将氯气制成漂白粉的目的是漂白粉比次氯酸稳定,便于储存和运输,漂白粉是一种混合物(填“混合物”或“纯净物”)
.新制的氯水可用于漂白,工业上将氯气制成漂白粉的目的是漂白粉比次氯酸稳定,便于储存和运输,漂白粉是一种混合物(填“混合物”或“纯净物”) 钠的化合物在生产生活中应用广泛.
钠的化合物在生产生活中应用广泛.